
| A. | 天然气和沼气的主要成分是甲烷 | |
| B. | 所有糖类物质都有甜味 | |
| C. | 纤维素乙酸酯、油脂和蛋白质在一定条件下都能水解 | |
| D. | 葡萄糖和蔗糖都含有C、H、O三种元素,但不是同系物 |
分析 A.甲烷是天然气和沼气的主要成分;
B.多糖本身无甜味;
C.纤维素乙酸酯、油脂、蛋白质都是有小分子物质经过化学反应形成的,所以能水解;
D.葡萄糖属于单糖,蔗糖属于糖类中的二糖,二者组成通式不同,结构不相似.
解答 解:A.天然气和沼气的主要成分是甲烷,故A正确;
B.单糖、二糖多有甜味,但多糖本身无甜味,故B错误;
C.纤维素乙酸酯在催化作用下发生水解,生成纤维素和乙酸;蛋白质水解最后得到多种氨基酸;在酸性条件下水解为甘油(丙三醇)和高级脂肪酸;在碱性条件下水解为甘油、高级脂肪酸盐,所以纤维素乙酸酯、油脂、蛋白质在一定条件下都能发生水解反应,故C正确;
D.葡萄糖属于单糖,分子式为C6H12O6,蔗糖属于糖类中的二糖,分子式为C12H22O11,二者组成通式不同,结构不相似,不是同系物,故D正确.
故选B.
点评 本题考查有机物的结构与性质和酸雨,为高考常见题型和高频考点,题目难度不大,注意对基础知识的理解掌握与识记.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献.
1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献.| 晶体 | NaCl | KCl | CaO |
| 晶格能/(kJ•mol-1) | 786 | 715 | 3401 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{6(1-x)}{7}$ | B. | $\frac{1-x}{7}$ | C. | $\frac{3x}{4}$ | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
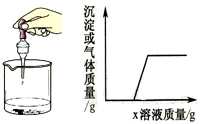 向烧杯中逐滴加入x溶液至过量,反应过程中生成沉淀或气体的质量与加入x溶液的质量关系能用如图所示的曲线表示的是( )
向烧杯中逐滴加入x溶液至过量,反应过程中生成沉淀或气体的质量与加入x溶液的质量关系能用如图所示的曲线表示的是( )| 序号 | 烧杯中的物质 | x溶液 |
| A | 生锈的铁钉 | 稀HCl |
| B | 盐酸与稀硫酸 | BaCl2溶液 |
| C | 镁铝合金 | NaOH溶液 |
| D | AlCl3和MgCl2溶液 | NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c元素的非金属性最强 | |
| B. | 它们均存在两种或两种以上的氧化物 | |
| C. | 只有d与其他元素生成的化合物都是离子化合物 | |
| D. | a、b、c与氢形成的化合物中化学键均为极性共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图为人体在某项生理过程中所发生的化学反应示意图.
如图为人体在某项生理过程中所发生的化学反应示意图.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2的相对分子质量比SiO2的相对分子质量小 | |
| B. | C-O键能小于Si-O键能 | |
| C. | C的原子半径小于Si | |
| D. | 破坏CO2晶体只需克服分子间作用力,破坏SiO2晶体要破坏Si-O共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com