
分析 根据n=$\frac{N}{{N}_{A}}$计算氨气的物质的量,氢原子物质的量为氨气的3倍,每个氨气分子含有10个质子,质子物质的量为氨气的10倍,根据V=nVm计算氨气体积.
解答 解:9.03×1023个氨分子的物质的量为$\frac{9.03×1{0}^{23}}{6.02×1{0}^{23}mo{l}^{-1}}$=1.5mol,在标准状况下的体积为1.5mol×22.4L/mol=33.6L,其中含有H原子为1.5mol×3=4.5mol,含有质子为1.5mol×10=15mol;
故答案为:33.6;4.5;15.
点评 本题考查物质的量有关计算,难度不大,注意掌握以物质的量为中心的有关计算公式,侧重于考查学生的分析能力和计算能力.


科目:高中化学 来源: 题型:选择题
| A. | H2O2的电子式: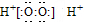 | |
| B. | 氮原子最外层电子轨道表达式: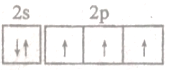 | |
| C. | Cl中子数为18的氯原子结构示意图: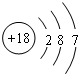 | |
| D. | 碳酸氢钠的电离方程式:NaHCO3?Na++H++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ①③⑤ | C. | ③④⑤ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L苯中含有NA个苯分子 | |
| B. | 14g N2含有的核外电子总数为14NA | |
| C. | 1 mol乙炔分子含3NA个碳碳叁键 | |
| D. | 23g金属钠与足量水反应时失去的电子数是NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠与CuSO4溶液反应:2Na+Cu2+═Cu+2Na+ | |
| B. | 稀H2SO4和Ba(OH)2溶液反应:H++SO42-+Ba2++OH-═BaSO4+H2O | |
| C. | 少量SO2通入苯酚钠溶液中:C6H5O-+SO2+H2O═2C6H5OH+SO32- | |
| D. | 醋酸钠的水解反应:CH3COO-+H3O+═CH3COOH+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
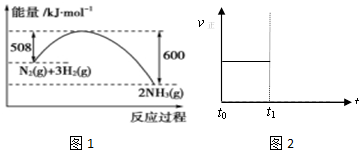
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
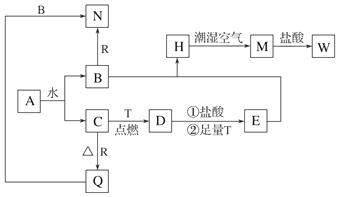
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com