
下列有关沉淀溶解平衡的说法中,正确的是( )
|
| A. | Ksp(AB2)小于Ksp(CD),说明AB2的溶解度小于CD的溶解度 |
|
| B. | 在氯化银的沉淀溶解平衡体系中加入蒸馏水,氯化银的Ksp增大 |
|
| C. | 在碳酸钙的沉淀溶解平衡体系中加入稀盐酸,沉淀溶解平衡不移动 |
|
| D. | 向氯化银沉淀溶解平衡体系中加人碘化钾固体,氯化银沉淀可转化为碘化银沉淀 |
考点:
难溶电解质的溶解平衡及沉淀转化的本质.
专题:
电离平衡与溶液的pH专题.
分析:
A.由于AB2与CD分子组成形式不同,因此不能根据Ksp大小来比较溶解度的大小;
B.KSP只与温度有关,与浓度无关;
C.稀盐酸能与CO32﹣反应,促进碳酸钙的沉淀溶解平衡向正方向移动;
D.由于AgCl与AgI分子组成形式相同,故Ksp越大,溶解度越大,溶解度大的能转化为溶解度小.
解答:
解:A.由于AB2与CD分子组成形式不同,因此不能根据KSP大小来比较溶解度的大小,故A错误;
B.KSP只与温度有关,与浓度无关,所以在氯化银的沉淀溶解平衡体系中加入蒸馏水,氯化银的Ksp不变,B错误;
C.碳酸钙的沉淀溶解平衡为:CaCO3(s)⇌Ca2+(aq)+CO32﹣(aq),加入稀盐酸能与CO32﹣反应,促进碳酸钙的沉淀溶解平衡向正方向移动,故C错误;
D.由于AgCl与AgI分子组成形式相同,故Ksp越大,溶解度越大,溶解度大的能转化为溶解度小的,因为KSP(AgCl)大于KSP(AgI),故AgI的溶解度小,所以氯化银沉淀能转化为AgI黄色沉淀,故D正确;
故选D.
点评:
本题考查了溶解度大小的比较,影响Ksp的因素,沉淀溶解平衡的移动等,题目难度一般.


科目:高中化学 来源: 题型:
关于化学键的下列表述中,正确的是()
A. 共价化合物可能含有离子键
B. 离子化合物中可能含有共价键
C. 离子化合物中只含有离子键
D. 硫酸中含有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,A与B和A与X均可形成10个电子化合物,A的单质常温下为密度最小的气体;B与Z的最外层电子数之比为2:3,常见化合物Y2X2是淡黄色固体,能与水反应生成X的单质,其溶液可使酚酞试液变红.请回答下列问题.
(1)Y的原子结构示意图为; Z在周期表中的位置是;B元素的名称为碳.
(2)化合物Y2X2属于A(填序号).
A.离子化合物 B.共价化合物
(3)A与X和A与Z均能形成18个电子的化合物,此两种化合物发生反应生成Z的化学方程式为.
(4)A的单质与X的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则正极通入(填物质名称);放电时KOH溶液中的OH﹣往负极方向移动(填正或负).
(5)1980年我国首次制成一辆燃氢汽车,乘员12人,以50km/h行驶了40km.为了有效发展民用氢能源,首先必须制得廉价的氢气.下列可供开发、较经济又具有广阔前景的制氢方法是(填写编号)
①光解海水 ②锌和稀硫酸反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
密闭容器中进行下列反应:M(g)+N(g)⇌R(g)+2L,如图所示R%是R的体积分数,t是时间,下列关于该反应的分析正确的是( )
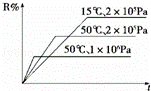
|
| A. | 正反应吸热,L为气体 |
|
| B. | 正反应吸热,L为固体或纯液体 |
|
| C. | 正反应放热,L为气体 |
|
| D. | 正反应放热,L为固体或纯液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
当下列各组物质的总物质的量不变时,使各组分以任意比混合后充分燃烧,消耗氧气的量和生成CO2的物质的量不变的是( )
|
| A. | 乙烯、乙醇、乙醛 | B. | 乙炔、乙醛、乙二醇 |
|
| C. | 甲烷、甲醇、乙酸 | D. | 甲烷、甲酸甲酯、丙二酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示装置进行实验,将液体A逐滴加入到固体B中,下列叙述中不正确的是( )
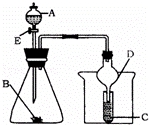
|
| A. | 若A为醋酸,B为贝壳(粉状),C为盛苯酚钠溶液,则C中溶液变浑浊 |
|
| B. | 若A为食盐水,B为电石,C中盛KMnO4溶液,则C中溶液褪色 |
|
| C. | 若A为浓氨水,B为生石灰,C中盛AgNO3溶液,则C中无现象 |
|
| D. | 实验中仪器D可起到防倒吸的作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)⇌CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与 压强的关系如右下图所示.下列说法正确的是()
压强的关系如右下图所示.下列说法正确的是()
A.温度: T1>T2>T3
B.正反应速率: υ(b)>υ(d) υ(a)>υ(c)
C.平衡常数: K(a)>K(c) K(b)=K(d)
D.平均摩尔质量: M(b)>M(d) M(a)<M(c)
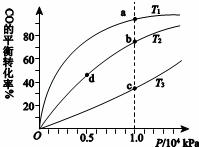
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
下列书写的离子方程式中,正确的是 ( )。
A.高锰酸钾溶液与乙二酸(草酸)反应:2MnO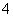 +5C2O
+5C2O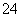 +16H+===2Mn2++10CO2↑+8H2O
+16H+===2Mn2++10CO2↑+8H2O
B.在NH4HSO4溶液中缓慢滴入含等物质的量的NaOH的溶液:NH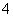 +OH-===NH3·H2O
+OH-===NH3·H2O
C.VO2+与酸性高锰酸钾溶液反应:5VO2++MnO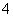 +H2O===5VO
+H2O===5VO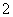 +Mn2++2H+
+Mn2++2H+
D.Fe2+被空气氧化:4Fe2++O2+2H2O===4Fe3++4OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com