
X、Y、Z是三种短周期元素,X和Z的质子数之和与Y的质子数相等,Z的电子层数是X的电子层数的2倍。A、B、C、D、E、F是中学化学中的常见物质,它们由上述三种元素中的一种、两种或三种组成,其中A是能使湿润红色石蕊试纸变蓝的气体,D、E是两种酸,F是一种单质,反应③④均在微生物作用下进行,其转化关系如图所示。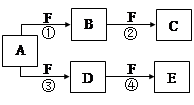
回答下列问题:
(1)A的电子式为 。
(2)A和E反应生成G,C与G中都含有 (填化学键的类型)。
(3)反应③中如果转移的电子为3 mol,则被氧化的A为 mol。
(4)科学家发明了使ZX3直接用于燃料电池的方法,其装置用铂作电极,加入碱性电解质溶液,往一极通入空气,另一电极通入ZX3并使之转化为无污染的气体,试写出负极的电极反应式: 。
(5)由Z、X两元素形成的含10个电子的阳离子可和XSO4-形成一种盐A,若往A的溶液中缓缓滴入稀NaOH溶液至溶液恰好呈中性,则溶液中所含离子浓度由大到小的顺序为: 。
(1) (2分) (2) 共价键(或极性共价键)(2分)(3)0.5(2分)
(2分) (2) 共价键(或极性共价键)(2分)(3)0.5(2分)
(4)2NH3—6e-+6 OH-=N2+6H2O (2分) (5)c(Na+) >c(SO42-) >c(NH4+)>c(H+) = c(OH-)
解析试题分析:根据题意知,X、Y、Z是三种短周期元素,Z的电子层数是X的电子层数的2倍,则X位于第一周期, Z位于第二周期;A是能使湿润红色石蕊试纸变蓝的气体,A为氨气;则X为氢元素,Y和Z中有一种为氮元素,X和Z的质子数之和与Y的质子数相等,若Z为氮元素,则Y为氧元素,若Y为氮元素,则Z为碳元素,结合题给信息及转化关系知,Z为氮元素,Y为氧元素;F为氧气,B为一氧化氮,C为二氧化氮,D为亚硝酸,E为硝酸;(1)A为氨气,电子式为 ;(2)氨气和硝酸反应生成硝酸铵,硝酸铵和二氧化氮均含有的化学键为共价键(或极性共价键);(3)反应③为氨气氧化为亚硝酸,氮元素的化合价由—3价升高到+3价,1mol氨气被氧化转移6mol电子,如果转移的电子为3 mol,则被氧化的A为0.5mol;(4)本题考查氨气燃料电池,根据原电池原理知,氨气发生氧化反应,在负极发生反应,结合题给信息和原子守恒、电荷守恒知,负极反应式为2NH3—6e-+6 OH-=N2+6H2O;(5)由题意知,盐A为NH4HSO4,与氢氧化钠反应至中性,混合液中溶质为硫酸钠、硫酸铵和一水合氨,离子浓度由大到小的顺序为:c(Na+) >c(SO42-) >c(NH4+)>c(H+) = c(OH-)。
;(2)氨气和硝酸反应生成硝酸铵,硝酸铵和二氧化氮均含有的化学键为共价键(或极性共价键);(3)反应③为氨气氧化为亚硝酸,氮元素的化合价由—3价升高到+3价,1mol氨气被氧化转移6mol电子,如果转移的电子为3 mol,则被氧化的A为0.5mol;(4)本题考查氨气燃料电池,根据原电池原理知,氨气发生氧化反应,在负极发生反应,结合题给信息和原子守恒、电荷守恒知,负极反应式为2NH3—6e-+6 OH-=N2+6H2O;(5)由题意知,盐A为NH4HSO4,与氢氧化钠反应至中性,混合液中溶质为硫酸钠、硫酸铵和一水合氨,离子浓度由大到小的顺序为:c(Na+) >c(SO42-) >c(NH4+)>c(H+) = c(OH-)。
考点:考查元素推断、氧化还原反应、燃料电池及离子浓度大小比较。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是由第三周期元素组成的单质中熔点最高的金属,K是一种红棕色气体。
提示:4FeS2+11O2高温,2Fe2O3+8SO2
请填写下列空白:
(1)在周期表中,组成单质G的元素位于第________周期________族。
(2)在反应⑦中氧化剂与还原剂的物质的量之比为________。
(3)在②、③、⑥、⑨中既属于化合反应又属于非氧化还原反应的是________(填序号)。
(4)反应④的离子方程式是_____________________________________。
(5)将化合物D与KNO3、KOH共熔,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾),同时还生成KNO2和H2O。该反应的化学方程式是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
在下图所示的物质转化关系中,A是海水中含量最丰富的盐,B是常见的无色液体,G的水溶液是一种常用的漂白剂,F是地壳中含量最多的金属元素。(反应中生成的水和部分反应条件未列出)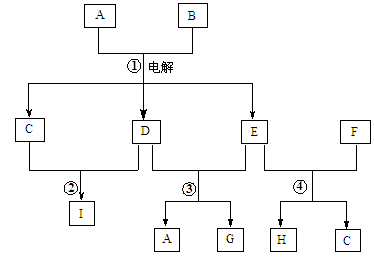
(1)画出A中阴离子的结构示意图 。
(2)反应②在点燃条件下的现象是 。
(3)H转化为F的氢氧化物最好选择的试剂是 。
(4)反应③的离子方程式为 。
(5)反应④的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A~G各物质间的关系如下图,其中B、D为气态单质。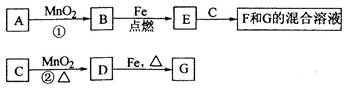
请回答下列问题:(①中MnO2作催化剂,②中MnO2作氧化剂)
(1)物质C和E的名称分别为________________、__________________;
(2)可选用不同的A进行反应①,若能在常温下进行,其化学方程式为_____________;若只能在加热情况下进行,则反应物A应为_____________;
(3)反应②的化学方程式:_______________________________________;
(4)新配制的F溶液应加入_____________以防止其转化为G。检验G溶液中阳离子的常用试剂是_____________,实验现象为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
中学化学中常见的几种物质存在下图所示的转化关系。其中, A是一种黑色粉末状固体,C是一种黄绿色气体,实验室中常用E溶液吸收多余的C。(图中部分产物和反应条件已略去)。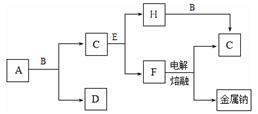
试回答下列问题:
(1)写出A与B的浓溶液反应的化学方程式 。
(2)将B的浓溶液与H的浓溶液混合,立即产生大量气体C,该反应的离子方程式为 。
(3)某课外小组同学用E溶液吸收C,利用下图所示装置向吸收液中持续通入SO2气体。实验过程中观察到如下现象: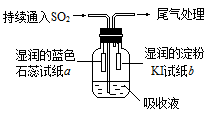
①开始时,溶液上方出现白雾,试纸a变红。甲同学认为是HCl使a变红,乙同学不同意甲的观点,乙同学认为使a变红的是
(写出一种即可)。
②片刻后,溶液上方出现黄绿色气体,试纸b变蓝。用离子方程式解释b变蓝的原因: 。
③最终试纸b褪色。同学们认为可能的原因有两种:一是I2有还原性,黄绿色气体等物质将其氧化成IO3-,从而使蓝色消失;二是 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
如下图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。常温下X和H是固体,B和G是液体,其余均为气体, 1 mol X分解得到A、B、C各1 mol。
试回答下列各题:
(1)写出下列物质的化学式:X________,B________。
(2)写出下列反应的化学方程式:
①H+G―→A+F:__________________________________________________________。
②C+D―→E:__________________________________________________________。
(3)写出下列反应的离子方程式:
G+Cu―→E:___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
中学常见化学反应方程式为:A+B→X+Y+H2O(未配平,反应条件略去),其中,A、B的物质的量之比为1:4。请回答:
(1)若Y为黄绿色气体,该反应的离子方程式为 ,B体现出的化学性质有
(2)若A为常见的非金属单质,B的溶液为某浓酸,反应条件为加热,其反应的化学方程式为
(3)若A为某不活泼的金属单质,实验室常用该反应来制备某种能形成酸雨的气体,该反应中氧化剂与还原剂的物质的量之比为
(4)若A为常见的金属单质,常温下A在B的浓溶液中“钝化”,且A可溶于X溶液中。
①A元素在元素周期表中的位置是
②含amolX的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量恰好相等,则被还原的X的物质的量是
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
如下图表示有关物质之间的转化关系,其中X是一种正盐,Y是一种强酸,C是淡黄色固体,E是常见的金属单质.(反应①⑥⑦⑧⑨中的部分产物已略去).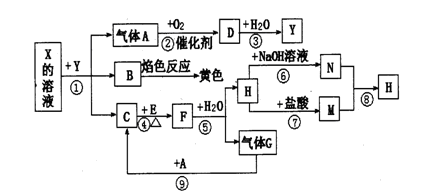
请回答下列问题:
(1)固体C的晶体类型是 ,F的化学式是 。
(2)工业上要实现A—D D—Y的转化需要的设备分别是 、 。
(3)在反应⑨中的氧化剂与还原剂的物质的量之比是 。
(4)反应⑧的离子方程式为 。
(5)正盐X中酸根离子中除氧元素外另一种元素的平均化合价可能为( )。
| A.+4价 | B.-2价 | C. 0价 | D.+2价 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下列实验流程图中,X为第三周期两种重要单质的氧化物的混合物。反应②、④是工业上的重要反应,部分物质及反应条件没有列出。
请回答下列问题:
(1)写出A、E、B的化学式:A________, E___________,B___________。
(2)写出C溶液转化为C固体的过程中,HCl气流的作用:________________________。
(3)写出①、③、④反应的化学方程式,(若是离子反应写离子方程式)
①__________________________________________________;
③__________________________________________________;
④__________________________________________________。
(4)将SO2气体分别通入下列溶液写出对应的实验现象
①BaCl2溶液________________________________;
②Ba(NO3)2溶液_____________________________________;
⑨FeCl3溶液_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com