
【题目】已知A是生产生活中用量最大的金属,B为淡黄色粉末。在常温下C为无色液体,E、G、H、I、J为气体,其中H为黄绿色,其它为无色.J能使湿润的红色石蕊试纸变蓝(图中部分产物已略去)。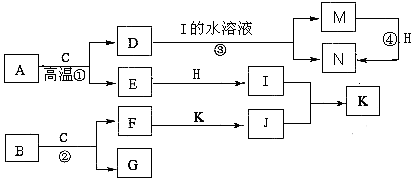
请填写下列空白
(1)写出化学式:M , K。
(2)写出①的化学方程式;写出③的离子方程式。
(3)反应④属于下列何种反应类型______(填字母序号)。
A.化合反应
B.氧化还原反应
C.离子反应
D.置换反应
(4)若要确定③反应后所得溶液中含有M物质,所选试剂为______(填序号)。
A.KSCN溶液和氯水
B.铁粉和KSCN
C.浓氨水
D.酸性高锰酸钾溶液
(5)常温下,H与过量的J反应产生浓厚的白烟,另一生成物是空气的主要成分之一,请写出该反应的化学方程式。
【答案】
(1)FeCl2;NH4Cl
(2)3Fe+4H2O ![]() Fe3O4+4H2;Fe3O4+8H+=Fe2++2Fe3++4H2O
Fe3O4+4H2;Fe3O4+8H+=Fe2++2Fe3++4H2O
(3)A,B,C
(4)D
(5)8NH3+3Cl2= 6NH4Cl+ N2
【解析】由题中所给信息,A是金属铁,常温下C为无色液体只能是水,A能和水蒸气反应生成D(四氧化三铁)和E(氢气)。H为黄绿色,所以H是氯气,I是氯化氢。又有J能使湿润的红色石蕊试纸变蓝也是解本题的突破口,可得J为氨气,所以K为NH4Cl。B为淡黄色粉末,可能是单质硫、过氧化钠、溴化银等,依据转化关系可知B只能是过氧化钠,其和水反应生成G(氧气)和F(氢氧化钠),F(氢氧化钠)和K(NH4Cl)反应生成无色气体J(氨气),
(1)由以上分析可知M为FeCl2 , K为NH4Cl;
(2)反应①是铁与水蒸汽反应生成四氧化三铁和氢气,其化学方程式为3Fe+4H2O ![]() Fe3O4+4H2 ;反应③是四氧化铁溶解于稀盐酸生成氯化铁和氯化亚铁的溶解,反应的离子方程式为Fe3O4+8H+=Fe2++2Fe3++4H2O;
Fe3O4+4H2 ;反应③是四氧化铁溶解于稀盐酸生成氯化铁和氯化亚铁的溶解,反应的离子方程式为Fe3O4+8H+=Fe2++2Fe3++4H2O;
(3)反应④为2Fe2++Cl2=2Fe3++2Cl- , 该反应为化合反应、氧化还原反应、离子反应,所以答案是ABC;
(4)③反应后所得溶液中含有Fe2+ , 可与酸性高锰酸钾溶液发生氧化还原反应而使高锰酸钾溶液褪色,其它选项不能证明,不能排除铁离子的干扰,所以答案是D;
(5)常温下,H与过量的J反应产生浓厚的白烟,另一生成物是空气的主要成分之一,该反应的方程式为8NH3+3Cl2=N2+6NH4Cl。


科目:高中化学 来源: 题型:
【题目】某实验过程如图所示,则图③试管中的现象是( ) 
A.铜片溶解,产生无色气体,该气体遇空气变为红棕色
B.铜片溶解,产生无色气体,该气体遇到空气不变色
C.铜片溶解,放出红棕色有刺激性气味的气体
D.无明显现象,因稀硫酸不与铜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示.下列判断正确的是( ) 
A.原NaOH溶液的浓度为0.1mol/L
B.通入CO2的体积为448mL
C.所得溶液的溶质成分的物质的量之比为(NaOH):(Na2CO3)=1:3
D.所得溶液的溶质成分的物质的量之比为(NaHCO3):(Na2CO3)=2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人类使用金属材料历史悠久。下列说法不正确的是
A. 电解NaCl溶液制备NaB. 电解熔融MgCl2制备Mg
C. 钢体船外镇嵌锌板可起防腐作用D. 青铜器的材质属于含锡合金
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示.下列判断正确的是( ) 
A.原NaOH溶液的浓度为0.1mol/L
B.通入CO2的体积为448mL
C.所得溶液的溶质成分的物质的量之比为(NaOH):(Na2CO3)=1:3
D.所得溶液的溶质成分的物质的量之比为(NaHCO3):(Na2CO3)=2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液里,只含有下列八种离子中的某几种:Mg2+、Na+、H+、Ag+、Cl﹣、 ![]() .已知该溶液能跟金属铝反应,且放出的气体只有氢气,试回答:
.已知该溶液能跟金属铝反应,且放出的气体只有氢气,试回答:
(1)若溶液跟Al反应后有[Al(OH)4]﹣生成,则原溶液一定含有大量的离子,还可能含有大量的离子.
(2)若溶液跟Al反应后有Al3+生成,则原溶液中一定不含有大量离子.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验的说法正确的是( )
A.除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤
B.为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量
C.制备Fe(OH)3胶体,通常是将Fe(OH)3固体溶于热水中
D.某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】字母A﹣F代表六种不同物质,它们之间可发生如图的转化(部分反应中生成物没有全部列出).其中D是一种强酸;E是一种常见金属,有“国防金属”的美誉,可在CO2中燃烧.分析图示回答下列问题: 
(1)A可以是或;
(2)E在CO2中燃烧的化学方程式为;
(3)D与F反应的化学方程式为 , 该反应中D表现了性;
(4)50mL 14molL﹣1物质D的溶液中加入足量的铜,充分反应后共收集到气体2.24L(标准状况下),则被还原的D的物质的量为mol,参加反应的铜的质量为g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知二氧化氮与氨气在一定条件下反应可以生成氮气和水,有关该反应的判断中正确的是( )
A.氨气在反应中得到电子,表现还原性
B.有1molN2生成时,反应中转移电子数为6NA
C.氧化产物与还原产物的质量之比为4:3
D.该反应中各物质均属于非电解质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com