
| A.金属冶炼的本质是将化合态金属还原为游离态,冶炼方法由金属的活泼性决定 |
| B.Cu的湿法冶炼是将金属钠投入到CuSO4溶液中,从而置换出铜 |
| C.Fe通常采用热还原法冶炼,加入石灰石的目的是除去过量的碳 |
| D.由于Al的活泼性强,故工业上采用电解熔融AlCl3的方法生产Al |
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源:不详 题型:单选题
| A.与电源正极相连接的是电解槽的阳极 |
| B.与电源负极相连接的是电解槽的阴极 |
| C.电流从电源的负极沿导线流人电解槽的阴极 |
| D.在电解槽的阳极发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

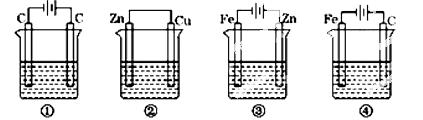
| A.图a中,随着电解的进行溶液中H+的浓度越来越大 |
| B.图b中,Mg电极作电池的负极 |
| C.图c中,发生的反应为Co+Cd2+=Cd+Co2+ |
| D.图d中:K分别与M、N连接,Fe电极均受到保护不会腐蚀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.阳极100g,阴极128g | B.阳极93.6g,阴极121.6g |
| C.阳极91.0g,阴极119.0g | D.阳极86.0g,阴极114.0g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com