
| A. | 熔点:金刚石>晶体硅>冰>干冰 | B. | 电负性:N>O>F | ||
| C. | 熔点:CsCl>MgO>Na>K | D. | 沸点:C2H5SH>C2H5OH>CH3SH |
分析 A.原子晶体熔点大于分子晶体,结合原子晶体中键长越短熔点越高、氢键增大了分子间作用力分析;
B.非金属性越强,电负性越大;
C.离子晶体的熔点较高,碱金属晶体熔点较低,结合离子晶体的晶格能大小分析;
D.含有羟基的分子间存在氢键,其熔点较高.
解答 解:A.原子晶体熔沸点高于分子晶体,原子晶体中键长越短熔点越高,金刚石和硅都是原子晶体、二氧化碳是分子晶体,且C-C键长小于Si-Si,所以熔点金刚石>晶体硅;冰中含有氢键,导致其熔点大于干冰,则熔点:金刚石>晶体硅>冰>干冰,故A正确;
B.同周期自左而右电负性增大,故电负性:N<O<F,故B错误;
C.CsCl、MgO为离子晶体,离子晶体熔沸点与晶格能成正比,晶格能与离子半径成反比、与电荷成正比,则熔点CsCl<MgO,故C错误;
D.C2H5OH分子间存在氢键,其沸点较高,则沸点:C2H5OH>C2H5SH>CH3SH,故D错误;
故选A.
点评 本题考查较为综合,涉及电负性、熔沸点大小比较、氢键等知识,题目难度不大,明确晶格能、氢键对物质沸点影响为解答关键,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 在无色溶液中:NH4+、Fe2+、SO42-、CO32- | |
| B. | 在含大量Ba2+溶液中:NH4+、Na+、Cl-、OH- | |
| C. | 在强碱性溶液中:Na+、K+、SO42-、HCO3- | |
| D. | 在强酸性溶液中:K+、Fe2+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠和冷水反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | AlCl3溶液中加入足量的氨水:Al3++4OH-═AlO2-+2H2O | |
| C. | 将氯气通入水中:Cl2+H2O=Cl-+HClO+H+ | |
| D. | 向Fe(NO3)2溶液中加入稀盐酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 向100mL 3mol/L的NaOH溶液中通入CO2气体后得到溶液M,因CO2通入的量不同,溶液M的组成也不同,若向M中逐滴加入1mol/L盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图所示.
向100mL 3mol/L的NaOH溶液中通入CO2气体后得到溶液M,因CO2通入的量不同,溶液M的组成也不同,若向M中逐滴加入1mol/L盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在离子化合物中也可能含有共价键 | |
| B. | 非金属元素的原子之间形成的化学键一定是共价键 | |
| C. | 含共价键的化合物不一定是共价化合物 | |
| D. | 含离子键的化合物一定是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知该分子中含有四面体结构的碳原子数为a,可在同一直线上的碳原子数最多为b,一定在同一平面内的碳原子数为c,则a、b、c分别为( )
已知该分子中含有四面体结构的碳原子数为a,可在同一直线上的碳原子数最多为b,一定在同一平面内的碳原子数为c,则a、b、c分别为( )| A. | 2、3、5 | B. | 3、3、6 | C. | 2、5、4 | D. | 4、6、4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
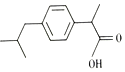
| A. | 布洛芬属于苯的同系物 | B. | 能与NaOH溶液反应 | ||
| C. | 所有原子在同一平面上 | D. | 能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,Ni与CO能形成配合物Ni(CO)4,该分子中σ键与π键个数比为1:1.
,Ni与CO能形成配合物Ni(CO)4,该分子中σ键与π键个数比为1:1.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X与Y形成的化合物可能含有非极性键 | |
| B. | X的单质与Z的单质在暗处能剧烈反应 | |
| C. | 含W的盐溶于水形成的溶液常用于自来水的杀菌消毒 | |
| D. | 离子半径:r(Z-)>r(W3+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com