
【题目】设 NA 为阿伏加德罗常数的值,下列说法中正确的是( )
A.标准状况下,22.4 L 甲苯所含的分子数约为NA
B.室温下,2.8g 乙烯与丙烯的混合物中含碳原子的数目为 0.2NA
C.1 mol C3H8 分子中含有共价键的数目为 9 NA
D.1 mol 氯气和足量甲烷在光照条件下反应可生成 2 NA 个氯化氢分子
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】运用元素周期表分析下列判断,其中错误的是( )
A.铍(Be)的氧化物的水合物可能是两性氧化物
B.硒化氢(![]() )是有色、有毒的气体,比
)是有色、有毒的气体,比![]() 稳定
稳定
C.![]() 的酸性比
的酸性比![]() 的酸性弱
的酸性弱
D.砹(At)为有色固体,HAt不稳定,AgAt感光性强,不溶于一般的酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表为元素周期表的一部分,表中a~f代表六种短周期主族元素。完成下列填空:
a | b | c |
d | e | f |
(1)六种元素中,原子半径最大的是_________ (填元素编号) 。d、e、f三种元素的原子结构上的相同点是________________________________。
(2)若a的气态氢化物的水溶液呈碱性,则a的气态氢化物的电子式是___________;六种元素中,最高价氧化物对应水化物的酸性最强的是_________(填元素符号)。
(3)若f元素的原子L层电子数比M层电子数多1个,则e元素的非金属性比f元素的非金属性_________(选填“强”、“弱’’),能说明这一事实的化学方程式是____________________(任写一个)。
(4)若b为非金属元素,则以下推断正确的是_________(选填编号)。
①a一定是金属元素 ②d一定是金属元素 ③f一定是非金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属铜是被人们认识和利用较早的金属之一,西汉《淮南万毕术》中有“曾青得铁则化为铜”的记载,“曾青”是CuSO4溶液。回答下列问题:
(1)一些铜盐在灼烧时会产生特殊的颜色,原因是___。
(2)CuSO4溶液中,金属阳离子的最高能层符号为___;其中未成对电子数为___。
(3)CuSO4·5H2O可写成[Cu(H2O)4SO4]H2O,其结构如图所示:

①[Cu(H2O)4]2+中O原子的杂化类型为___。1mol[Cu(H2O)4]2+中含有σ键的个数为___(NA表示阿伏加德罗常数的值)。
②CuSO4·5H2O结构中含有的化学键的类型有___,所含元素的电负性大小顺序为___。
(4)金属铜的晶胞结构如图所示。
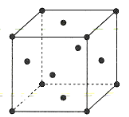
①该晶胞结构中含有由Cu原子构成的正八面体空隙和正四面体空隙,则正八面体空隙数和正四面体空隙数的比为___。
②科研发现硫化铜可以作为一种极为重要的P型半导体,其晶胞结构可以理解为铜晶胞中互不相邻的正四面体形成的空隙被S2-占据,若该晶体的密度为ag·cm-3,则两个最近的S2-之间的距离为___pm(NA表示阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知苯蒸气在激光作用下可以转化为棱晶烷:
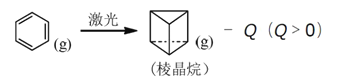
根据上述关系,在相同条件下不能判断( )
A.苯和棱晶烷的稳定性相对大小
B.等质量苯与棱晶烷完全分解为炭黑与氢气所需能量大小
C.等物质的量的苯与棱晶烷分别充分燃烧放出的热量大小
D.一根碳碳双键与两根碳碳单键键能之和大小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列 3 种有机化合物 A: CH2=CH-CH3 B:![]() C:CH3CH2CH2OH
C:CH3CH2CH2OH
(1)写出化合物A、C 中的官能团的名称: _____、 ______。
(2)A在催化剂加热条件下生成聚合物的反应方程式:_____ 。
(3)C物质在一定条件下可转化为A,请写出其化学方程式: _____。
(4)B可与NaOH 溶液反应生成苯酚钠,写出向苯酚钠中通入二氧化碳的化学方程式为:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸钠在不同温度下可以失去部分或全部的结晶水,现有一种碳酸钠晶体(Na2CO3·nH2O)样品,可采用在不同温度下加热样品(温度逐渐升高)来测定其组成。某学生的实验流程如下,以下说法不正确的是( )


A.实验所用定量实验仪器为电子天平
B.灼烧在坩埚中进行
C.操作只在空气中进行冷却
D.流程中有恒重操作
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化铝陶瓷常用于厚膜集成电路,制备氧化铝陶瓷的合成路线如图所示,回答下列问题。
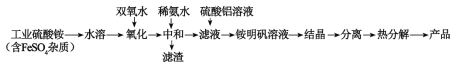
(1)“氧化”步骤发生的离子方程式为:___,使用双氧水作氧化剂优点为___:
(2)“热分解”得到的产物除了氧化铝外,还有NH3、N2、SO2、SO3、H2O生成,则氧化产物和还原产物的物质的量之比为___。
(3)铵明矾晶体的化学式为NH4Al(SO4)2·12H2O,“热分解”步骤中,其各温度段内受热“失重计算值”(失重计算值%=![]() ×100%)如表所示:
×100%)如表所示:
温度区间(℃) | 18→190 | 190→430 | 430→505 | 505→900 |
失重计算值(%) | 39.20 | 7.80 | 13.00 | 26.00 |
通过上述数据经粗略计算可判断,在温度区间___铵明矾基本上失去了全部结晶水。
(4)“结晶”步骤中常采用的操作是___。
(5)合成过程中常使用过量的工业硫酸铵,可利用硫酸铵溶液水解显酸性抑制硫酸铝水解,另外的一个重要作用是___。
(6)通常认为金属离子浓度等于1×10-5mol/L即可认为沉淀完全,试计算常温下“中和”步骤中需要调节溶液pH=___(保留一位小数,已知:Ksp[Fe(OH)3]=8.0×10-38,lg5=0.7)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com