
【题目】在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如图:
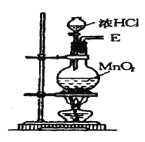
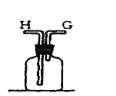
(1)该反应中生成氯气的化学方程式为:__。
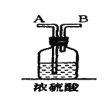
(2)连接上述仪器的正确顺序是:(填各接口处的字母)E接___接___,___接___接___,___接__。___。
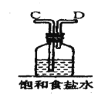
(3)在装置中,①饱和食盐水起的作用是__。
②浓硫酸起的作用是__。
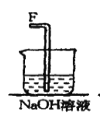
③NaOH溶液的作用是__。
(4)写出工业上用氯气和石灰乳制取漂白粉的化学反应方程式:__。
【答案】MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O CDABHGF 吸收Cl2中HCl 干燥Cl2 吸收末反应的Cl2,防止直接排放到空气中引起污染 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
MnCl2+Cl2↑+2H2O CDABHGF 吸收Cl2中HCl 干燥Cl2 吸收末反应的Cl2,防止直接排放到空气中引起污染 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
【解析】
在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气,反应原理为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,需要固体-液体加热发生装置生成氯气,用饱和食盐水除去氯气中混有的氯化氢气体,通过浓硫酸除去氯气中的水蒸气,并因为氯气密度比空气大,所以用导气管长进短出的集气瓶收集氯气,最后氯气是酸性气体,并且污染空气,所以用碱液来吸收多余的氯气,防止污染空气。
MnCl2+Cl2↑+2H2O,需要固体-液体加热发生装置生成氯气,用饱和食盐水除去氯气中混有的氯化氢气体,通过浓硫酸除去氯气中的水蒸气,并因为氯气密度比空气大,所以用导气管长进短出的集气瓶收集氯气,最后氯气是酸性气体,并且污染空气,所以用碱液来吸收多余的氯气,防止污染空气。
(1)根据分析知二氧化锰跟浓盐酸反应的化学方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)根据分析知仪器的正确顺序是CDABHGF,故答案为:CDABHGF;
(3)根据分析知用饱和食盐水除氯气中的氯化氢杂质气体,用浓硫酸除去氯气中的水蒸气,得到干燥的纯净的氯气,用NaOH溶液作为尾气吸收试剂,吸收氯气防止污染空气,故答案为:①吸收Cl2中HCl,②干燥Cl2,③吸收末反应的Cl2,防止直接排放到空气中引起污染;
(4)工业上用氯气和石灰乳制取漂白粉的化学反应方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O。


科目:高中化学 来源: 题型:
【题目】利用废蚀刻液(含FeCl2、CuCl2及FeCl3)制备碱性蚀刻液[Cu(NH3)4Cl2溶液]和FeCl36H2O的主要步骤:用H2O2氧化废蚀刻液,制备氨气,制备碱性蚀刻液[CuCl2+4NH3=Cu(NH3)4Cl2]、固液分离,用盐酸溶解沉淀并制备FeCl36H2O。下列实验原理和装置不能达到实验目的的是( )

A.用装置甲制备NH3B.用装置乙制备Cu(NH3)4Cl2并沉铁
C.用装置丙分离Cu(NH3)4Cl2溶液和Fe(OH)3D.用装置丁将FeCl3溶液蒸干制备FeCl36H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个容积均为2L的恒容密闭容器中按不同方式投入反应物,发生反应:2CO(g) + 4H2(g)CH3OCH3(g) + H2O(g) △H<0,测得反应的相关数据如下表:
容器1 | 容器2 | 容器3 | |
反应温度T/K | 600 | 600 | 500 |
反应物投入量 | 0.2mol CO 0.4mol H2 | 0.4mol CO 0.8mol H2 | 0.2mol CH3OCH3 0.2mol H2O |
平衡v(CO)/(mol·L-1·s-1) | v1 | v2 | v3 |
平衡n(H2)/(mol) | 0.2 | n2 | n3 |
平衡体系总压强p/Pa | p1 | p2 | p3 |
物质的平衡转化率a | a1(CO) | a2(CO) | a3(CH3OCH3) |
平衡常数K | K1 | K2 | K3 |
下列说法正确的是
A.v1<v2,n2>0.4B.K2=2.5×103,p2>p3
C.2p1<p3,a1(CO) >a2(CO)D.n3<0.4,a2(CO) + a3(CH3OCH3)<1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C、N、S是重要的非金属元素,按要求回答下列问题:
![]() 烟道气中含有的CO和
烟道气中含有的CO和![]() 是重要的污染物,可在催化剂作用下将它们转化为
是重要的污染物,可在催化剂作用下将它们转化为![]() 和
和![]() ,此反应的热化学方程式为______。
,此反应的热化学方程式为______。
已知:![]() ;
;
![]()
![]() 向甲、乙两个均为lL的密闭容器中,分别充入
向甲、乙两个均为lL的密闭容器中,分别充入![]() 和
和![]() ,发生反应:
,发生反应:![]()
![]() 甲容器在温度为T1的条件下反应,达到平衡时
甲容器在温度为T1的条件下反应,达到平衡时![]() 的物质的量为牛
的物质的量为牛![]() ;乙容器在温度为T2的条件下反应,达到平衡时
;乙容器在温度为T2的条件下反应,达到平衡时![]() 的物质的量为
的物质的量为![]() 。则
。则![]() ______
______![]() 填“
填“![]() ”或“
”或“![]() ,甲容器中反应的平衡常数
,甲容器中反应的平衡常数![]() ______
______
![]() 如图所示,A是恒容的密闭容器,B是一个体积可变的充气气囊。保持恒温,关闭
如图所示,A是恒容的密闭容器,B是一个体积可变的充气气囊。保持恒温,关闭![]() ,分别将
,分别将![]() 和
和![]() 通过
通过![]() 、
、 充入A、B中,发生的反应为
充入A、B中,发生的反应为![]() ,起始时A、B的体积相同均为
,起始时A、B的体积相同均为![]() 。
。

![]() 图中正确,且既能说明A容器中反应达到平衡状态,又能说明B容器中反应达到平衡状态的是______。
图中正确,且既能说明A容器中反应达到平衡状态,又能说明B容器中反应达到平衡状态的是______。
a. 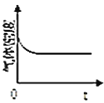 b.
b. 
c.  d.
d. 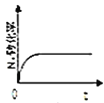
![]() 容器A中反应到达平衡时所需时间
容器A中反应到达平衡时所需时间![]() ,达到平衡后容器的压强变为原来的
,达到平衡后容器的压强变为原来的![]() ,则平均反应速率
,则平均反应速率![]() ______。
______。![]() 用a、t的代数式表示
用a、t的代数式表示![]()
![]() 达到平衡后,
达到平衡后,![]() 的体积分数:甲容器______乙容器
的体积分数:甲容器______乙容器![]() 填“
填“![]() ”、“
”、“![]() ”或”一
”或”一![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯氧磷(POCl3)常用作有机合成的氯化剂、催化剂和阻燃剂等。POCl3遇水会强烈水解,生成H3PO4和HCl。为测定某POCl3样品中Cl元素含量,进行下列实验:
①准确称取30.70 g POCl3样品,置于盛有60.00 mL蒸馏水的水解瓶中摇动至完全水解;
②将水解液配成100.00 mL溶液A,取10.00 mL溶液A于锥形瓶中;
③加入10.00 mL 3.200 mol·L-1 AgNO3标准溶液,并加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖;
④加入指示剂,用0.200 0 mol·L-1 KSCN溶液滴定过量的AgNO3溶液,达到滴定终点时共用去10.00 mL KSCN溶液。
已知:AgSCN是白色沉淀,Ksp(AgSCN)=2×10-12,Ksp(AgCl)=1.8×10-10。
(1) 滴定选用的指示剂是________ (填字母);滴定终点的现象为________。
A. FeCl2 B. NH4Fe(SO4)2 C. 淀粉 D. 甲基橙
(2) 用硝基苯覆盖沉淀的目的是________;若无此操作,所测Cl元素含量将会________ (填“偏大”、“偏小”或“不变”)。
(3) 计算三氯氧磷样品中Cl元素的含量________ (写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置正确且能达到实验目的的是![]()
A.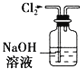 用如图所示装置除去Cl2中含有的少量HCl
用如图所示装置除去Cl2中含有的少量HCl
B.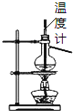 如图所示为石油分馏
如图所示为石油分馏
C.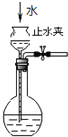 如图所示为检查装置气密性
如图所示为检查装置气密性
D.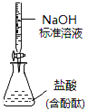 如图所示为测定未知盐酸的浓度
如图所示为测定未知盐酸的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述中,不正确的是

A.装置①中,d为阳极、c为阴极
B.装置②可用于收集H2、NH3、CO2、Cl2、NO2等气体
C.装置③中X若为四氯化碳,可用于吸收氨气,并防止倒吸
D.装置④可用于干燥、收集氨气,并吸收多余的氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂-铜空气燃料电池容量高、成本低,具有广阔的发展前景。该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法不正确的是( )

A.放电时,正极的电极反应式为O2+2H2O+4e-=4OH-
B.放电时,Li+透过固体电解质向Cu极移动
C.通空气时,铜被腐蚀,表面产生Cu2O
D.整个反应过程中,氧化剂为O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从![]() 甲烷
甲烷![]() 甲醛
甲醛![]() 乙酸
乙酸![]() 油脂
油脂![]() 纤维素
纤维素![]() 聚乙烯六种有机物中选择合适的物质,将其标号添在横线上.
聚乙烯六种有机物中选择合适的物质,将其标号添在横线上.
![]() 瓦斯的主要成分是 ______ ;
瓦斯的主要成分是 ______ ;
![]() 可制成食品保鲜膜和保鲜袋的 ______ ;
可制成食品保鲜膜和保鲜袋的 ______ ;
![]() 食醋可做增强食品酸味的调味剂,是因为其中含有 ______ ;
食醋可做增强食品酸味的调味剂,是因为其中含有 ______ ;
![]() 福尔马林溶液可以作为保存动物标本的溶液,是因为其中含有
福尔马林溶液可以作为保存动物标本的溶液,是因为其中含有![]() 的 ______ ;
的 ______ ;
![]() 可用来制造肥皂的原料的是 ______ ;
可用来制造肥皂的原料的是 ______ ;
![]() 纯棉的衣服的化学成分是 ______ .
纯棉的衣服的化学成分是 ______ .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com