
配制FeSO4溶液要加入铁粉,配制SnCl2溶液要加入盐酸,二者原理是否相同?
科目:高中化学 来源: 题型:
根据前四周期元素原子核外电子排布特点,回答下列问题:
(1)外围电子层有2个未成对电子的有________;有3个未成对电子的有________。
(2)未成对电子数与周期数相等的元素有________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有以下物质:①HF,②Cl2,③H2O,④N2,⑤C2H4,⑥C2H6,⑦H2,⑧H2O2,⑨HCN(H—C≡N),其中,只含有极性键的是________;只含有非极性键的是________;既有极性键,又有非极性键的是______________;只有σ键的是______________;既有σ键又有π键的是__________;含有由两个原子的s轨道重叠形成的σ键的是____________;含有由一个原子的s轨道与另一个原子的p轨道重叠形成的σ键的是____________;含有由一个原子的p轨道与另一个原子的p轨道重叠形成的σ键的是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性。将溶液中的Cu2+、Fe2+、Fe3+沉淀为氢氧化物,需溶液的pH分别为6.4、9.6、3.7。现有含FeCl2杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按图示步骤进行提纯:
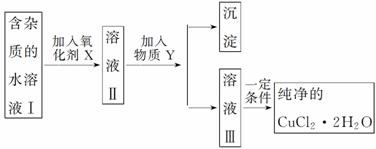
请回答下列问题:
(1)本实验最适合的氧化剂X是________(填字母)。
A.K2Cr2O7 B.NaClO
C.H2O2 D.KMnO4
(2)物质Y是________。
(3)本实验用加碱沉淀法能不能达到目的?__________,原因是________________________________________________________________________。
(4)除去Fe3+的有关离子方程式是___________________________________________。
(5)加氧化剂的目的是_______________________________________________________。
(6)最后能不能直接蒸发结晶得到CuCl2·2H2O晶体?________,应如何操作?________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.将AlCl3溶液和Al2(SO4)3溶液分别加热、蒸干、灼烧,所得固体成分相同
B.配制FeSO4溶液时,将FeSO4固体溶于稀盐酸中,然后稀释至所需浓度
C.用加热的方法可以除去KCl溶液中的Fe3+
D.洗涤油污常用热的碳酸钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列指定反应的离子方程式正确的是( )
A.Cu溶于稀HNO3:Cu+2H++NO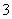 ===Cu2++NO2↑+H2O
===Cu2++NO2↑+H2O
B.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-===Fe(OH)2↓
C.用CH3COOH溶解CaCO3:CaCO3+2H+===Ca2++H2O+CO2↑
D.向NaAlO2溶液中通入过量CO2制Al(OH)3:CO2+AlO +2H2O===Al(OH)3↓+HCO
+2H2O===Al(OH)3↓+HCO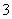
查看答案和解析>>
科目:高中化学 来源: 题型:
下列四种有机物的分子式均为C4H10O。
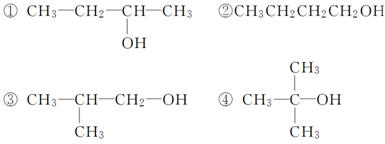
(1)能被氧化成含相同碳原子数的醛的是__________。
(2)能被氧化成酮的是__________。
(3)能发生消去反应且生成两种产物的是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com