
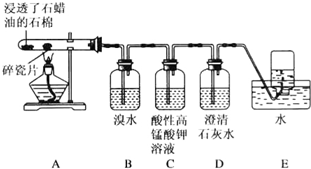
分析 (1)依据原子个数守恒判断甲、乙物质,写出其分子式和结构简式;
(2)乙烯含有碳碳双键,能够与溴发生加成反应;
(3)乙烯具有还原性,能够被酸性高锰酸钾氧化;
(4)二氧化碳与氢氧化钙反应生成碳酸钙沉淀;乙烯与溴若发生取代反应,则必然生成溴化氢,溴化氢溶于水显酸性;
(5)甲烷性质稳定,乙烯含有C=C双键,能发生加成反应和氧化反应,可用溴水除杂,注意除杂时不能引入新的杂质;
(6)有机物含碳量越高,燃烧火焰越明亮,烟越浓.
解答 解:(1)石油裂化属于化学反应,遵循原子个数守恒,C16H34$→_{△}^{催化剂}$C8H18+甲,所以甲分子式为:C8H16;
依据方程式:C8H16$→_{△}^{催化剂}$4乙,结合原子个数守恒可知,乙为:C2H4,为乙烯,结构简式为:CH2=CH2;
故答案为:C8H16;CH2=CH2;
(2)乙烯含有碳碳双键,能够与溴发生加成反应而使溴水褪色,方程式为:CH2=CH2+Br2→CH2Br-CH2Br,
故答案为:溴水褪色;CH2=CH2+Br2→CH2Br-CH2Br;加成反应;
(3)乙烯具有还原性,能够被酸性高锰酸钾氧化发生氧化反应而使高锰酸钾褪色,
故答案为:高锰酸钾褪色;氧化反应;
(4)乙烯与酸性高锰酸钾溶液反应产生二氧化碳,二氧化碳能够与氢氧化钙反应生成碳酸钙沉淀,溶液变浑浊;
乙烯与溴若发生取代反应,则必然生成溴化氢,溴化氢溶于水显酸性;
故答案为:D;乙烯与溴若发生取代反应,则必然生成溴化氢,溴化氢溶于水显酸性;
(5)A.甲烷、乙烯不溶于水,且常温下与水都不反应,不能用于鉴别和除杂;
乙烯含有C=C双键,能与溴水发生加成反应生成二溴乙烷液体,甲烷不与溴水反应,所以可用溴水除去甲烷中混有的乙烯,可以鉴别甲烷与乙烯;
甲烷与高锰酸钾不反应,乙烯能够与高锰酸钾反应使其褪色,可以鉴别二者;但是乙烯被氧化生成和二氧化碳气体,不能用于除杂;
D.甲烷、乙烯都不溶于氢氧化钠溶液,不能用来鉴别和除杂;
故可用来鉴别的是:BC;可用来除杂的是:B;
故答案为:BC;B;
(6)乙烯含碳量高于甲烷,所以燃烧火焰明亮而伴有黑烟;
故答案为:乙烯含碳量高于甲烷.
点评 本题考查了乙烯的制备和性质的检验,熟悉裂化的原理及原子个数守恒规律、乙烯的性质是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题

 TiO2•XH2O↓+4HCl
TiO2•XH2O↓+4HCl查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、K+、Fe2+、Cl- | B. | K+、Fe3+、NO3-、Fe(OH)3(胶体) | ||
| C. | Cl-、SCN-、NH4+、葡萄糖分子 | D. | OH-、Na+、苯酚、Br - |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应①中MnO2和H2SO4都是氧化剂 | |
| B. | 反应①中每析出12.8g S沉淀,转移0.8mol电子 | |
| C. | 金属锌也可用热还原法制备 | |
| D. | 硫酸在生产种可循环使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油裂化的主要目的是为了提高轻质液体燃料的产量 | |
| B. | 煤经过气化和液化两个物理变化,可变为清洁能源 | |
| C. | 冶炼铬可采用铝热法 | |
| D. | 将苦卤浓缩、氧化,鼓入热空气或水蒸气提取海水中的溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
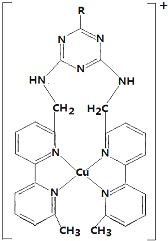 碳、氢、氧 3 种元素组成的有机物A,相对分子质量为 102,含氢的质量分数为9.8%,分子中氢原子个数为氧的 5 倍.
碳、氢、氧 3 种元素组成的有机物A,相对分子质量为 102,含氢的质量分数为9.8%,分子中氢原子个数为氧的 5 倍. 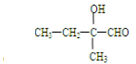 .
.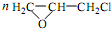 +CH2Cl+nOHCH2CH2OH$\stackrel{一定条件}{→}$
+CH2Cl+nOHCH2CH2OH$\stackrel{一定条件}{→}$ +nHCl
+nHCl查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验操作 | 答案 | 实验现象 |
| ①向鸡蛋清溶液里加入饱和硫酸铵溶液 | A.呈蓝色 B.呈黄色 C、析出白色沉淀 D.出现光亮的银镜 | |
| ②向银氨溶液中加人葡萄糖溶液后水浴加热 | ||
| ③向鸡蛋清溶液里滴加浓硝酸后微热 | ||
| ④向士豆片上滴加碘水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com