
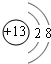
 ,硫离子的结构示意图为
,硫离子的结构示意图为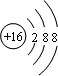 ,二者最外电子层上的电子数都是8,故B正确;
,二者最外电子层上的电子数都是8,故B正确;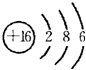 ,电子层数等于其周期数,最外层电子数等于与其族序数相等,所以S元素位于第三周期第VIA族,故D错误;
,电子层数等于其周期数,最外层电子数等于与其族序数相等,所以S元素位于第三周期第VIA族,故D错误;

科目:高中化学 来源:物理教研室 题型:013
A.x-3 B.x+3 C.x+11 D.x-11
查看答案和解析>>
科目:高中化学 来源:2013-2014学年上海市松江区高三上学期期末(一模)考试化学试卷(解析版) 题型:选择题
离子化合物A2B3是由短周期元素A和B形成,已知A3+离子比B2-离子少一个电子层,以下推断正确的是
A.化合物A2B3是氧化铝
B.A3+和B2-最外电子层上的电子数都是8
C.A的最高价氧化物对应的水化物是强电解质
D.元素B是第2周期第VIA族的元素
查看答案和解析>>
科目:高中化学 来源:安徽省蚌埠二中09-10学年高一下学期期中考试 题型:单选题
下列各组原子序数所表示的两种元素,能形成A2B3型离子化合物的是( )
A、7和8 B、8和13 C、11和16 D、2和17
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com