
| A. | ④①③② | B. | ①③④② | C. | ①④③② | D. | ①④②③ |
分析 硫酸铜溶液为蓝色溶液,可以先鉴别出来,然后利用硫酸铜把硫酸铜分别与其它三种物质反应,能生成沉淀的是氯化钡,把氯化钡与剩余的两种物质反应,能生成白色沉淀的是硫酸钠,剩余的为氯化钠,对于硫酸钠和氯化钠,不强调明显先后顺序.四种物质鉴别完毕,以此解答该题.
解答 解:硫酸铜溶液为蓝色,所以硫酸铜可以首先被鉴别出来,然后利用硫酸铜和氯化钡反应,把氯化钡鉴别出来,把剩余两液体分别滴入到氯化钡中,无现象时所加溶液为氯化钠,有沉淀时所加溶液为硫酸钠溶液.所以这四种物质先后被鉴别出的顺序为:硫酸铜溶液、氯化钡溶液、硫酸钠溶液、氯化钠溶液或者是硫酸铜溶液、氯化钡溶液、氯化钠溶液、硫酸钠溶液,即:④①③②或者④①②③.
故选A.
点评 本题考查物质的检验和鉴别,为高考常见题型,侧重于学生实验能力和综合运用化学知识的能力的考查,注意把握物质的性质,题目难度不大.


科目:高中化学 来源: 题型:选择题
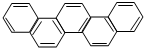 2015年,北京正在申办冬奥会.有一种有机物因其酷似奥林克五环旗,科学家称其为奥林匹克烃,下列有关奥匹克烃的说中正确的是( )
2015年,北京正在申办冬奥会.有一种有机物因其酷似奥林克五环旗,科学家称其为奥林匹克烃,下列有关奥匹克烃的说中正确的是( )| A. | 该物质属于苯的同系物 | |
| B. | 该物质的一氯代物有一种 | |
| C. | 该物质完全燃烧生成水的物质的量小于二氧化碳的物质的量 | |
| D. | 该物质的分子中只含有非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知:CH3CH2OH+NaBr+H2SO4(浓)$\stackrel{△}{→}$ CH3CH2Br+NaHSO4+H2O.
已知:CH3CH2OH+NaBr+H2SO4(浓)$\stackrel{△}{→}$ CH3CH2Br+NaHSO4+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 亚硫酸钠溶液加入稀硝酸:SO32-+2H+=SO2↑+H2O | |
| B. | 将1mol•L-1 NaAlO2溶液和1.5mol•L-1的HCl溶液等体积互相均匀混合:6AlO2-+9H++3H2O=5Al(OH)3↓+Al3+ | |
| C. | 向Al2(SO4)3溶液中加入过量NH3•H2O:Al3++4NH3•H2O=[Al(OH)4]-+4NH4+ | |
| D. | 铵明矾[NH4Al(SO4)2•12H2O]溶液中加入过量Ba(OH)2溶液:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铝是白色胶状沉淀,能凝聚水中的悬浮物,但不能吸附色素 | |
| B. | 不慎将浓碱溶液沾到皮肤上,要立即用大题水冲洗,然后涂上硼酸 | |
| C. | 氮气化学性质通常不活泼,可将炽热的镁粉可放在氮气中冷却 | |
| D. | 酒精灯着火时可用水扑灭 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲、乙、丙溶液中溶质的质量分数均大于5% | |
| B. | 甲溶液中溶质的质量分数小于5%,乙、丙溶液中溶质的质量分数大于5% | |
| C. | 甲溶液中溶质的质量分数小于5%,乙的大于5%,丙的等于5% | |
| D. | 甲、乙、丙溶液中溶质的质量分数均等于5% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S2- | B. | S | C. | SO32- | D. | SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,27g Al3+中含有的电子数目为13 NA | |
| B. | 22.4 L氧气中一定含有2NA个氧原子 | |
| C. | 23gNa和足量的O2完全燃烧条件下转移电子数为NA | |
| D. | 标准状况下,22.4 L乙醇(CH3CH2OH)中含有的氧原子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com