
| A、分子拆成原子 |
| B、物质从液态变到气态 |
| C、物质溶解在水中 |
| D、酸碱中和反应 |
科目:高中化学 来源: 题型:
| A、1.5 mol/L |
| B、1.5 mol/(L?s) |
| C、0.1 mol/L |
| D、0.1 mol/(L?s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同温同压下,相同体积的物质,其物质的量一定相等 |
| B、任何条件下,等物质的量的甲烷和一氧化碳所含的分子数一定相等 |
| C、1 L一氧化碳气体一定比1 L氧气的质量小 |
| D、相同条件下的一氧化碳气体和氮气,若物质的量相等则体积相等,但质量不相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2通入Ba(NO3)2溶液中无沉淀生成,推出SO2通入Ba(NO3)2溶液中无沉淀生成 |
| B、在常温下,Na2CO3+2HCl═2NaCl+CO2↑+H2O,说明HCl酸性强于H2CO3;在高温下,Na2CO3+SiO2═Na2SiO3+CO2↑,说明H2SiO3酸性强于H2CO3 |
| C、H2SO4为强酸,推出HClO4为强酸 |
| D、NH3的沸点高于PH3,推出CH4沸点高于SiH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
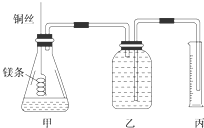
查看答案和解析>>
科目:高中化学 来源: 题型:
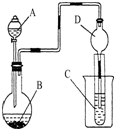
| A、若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色 |
| B、若A为醋酸,B为贝壳,C中盛澄清石灰水,则C中溶液变浑浊 |
| C、实验仪器D主要起到洗气的作用 |
| D、若A为浓氨水,B为生石灰,C中AlCl3溶液,则C中先产生白色沉淀后沉淀又溶解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com