
ЁОЬтФПЁПвбжЊЯТСаЪ§ОнЃК
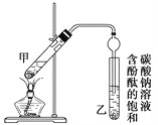
ФГбЇЩњдкЪЕбщЪвжЦШЁввЫсввѕЅЕФжївЊВНжшШчЯТЃК
ЂйХфжЦ2 mLХЈСђЫсЁЂ3 mLввДМ(КЌ18O)КЭ2 mLввЫсЕФЛьКЯШмвКЁЃ
ЂкАДЭМСЌНгКУзАжУ(зАжУЦјУмадСМКУ)ВЂМгШыЛьКЯвКЃЌгУаЁЛ№ОљдШМгШШ3ЁЋ5 minЁЃ
ЂлД§ЪдЙмввЪеМЏЕНвЛЖЈСПВњЮяКѓЭЃжЙМгШШЃЌГЗГіЪдЙмввВЂгУСІеёЕДЃЌШЛКѓОВжУД§ЗжВуЁЃ
ЂмЗжРыГіввЫсввѕЅЃЌЯДЕгЁЂИЩдяЁЃ
(1)ХфжЦЂйжаЛьКЯШмвКЕФЗНЗЈЮЊ____________ЃЛЗДгІжаХЈСђЫсЕФзїгУЪЧ________________ЃЛаДГіжЦШЁввЫсввѕЅЕФЛЏбЇЗНГЬЪНЃК____________ЁЃ
(2)ЩЯЪіЪЕбщжаБЅКЭЬМЫсФЦШмвКЕФзїгУЪЧ(ЬюзжФИ)_________ЁЃ
AЃЎжаКЭввЫсКЭввДМ BЃЎжаКЭввЫсВЂЮќЪеввДМ
CЃЎМѕЩйввЫсввѕЅЕФШмНт DЃЎМгЫйѕЅЕФЩњГЩЃЌЬсИпЦфВњТЪ
(3)ВНжшЂкжаашвЊаЁЛ№ОљдШМгШШЃЌЦфжївЊРэгЩЪЧ_______ЃЛВНжшЂлЫљЙлВьЕНЕФЯжЯѓЪЧ_________ЃЛгћНЋввЪдЙмжаЕФЮяжЪЗжРывдЕУЕНввЫсввѕЅЃЌБиаыЪЙгУЕФвЧЦїга________ЃЛЗжРыЪБЃЌввЫсввѕЅгІДгвЧЦї________________(ЬюЁАЯТПкЗХЁБЛђЁАЩЯПкЕЙЁБ)ГіЁЃ
(4)ИУЭЌбЇЗДИДЪЕбщЃЌЕУГіввДМгыввЫсЕФгУСПКЭЕУЕНЕФввЫсввѕЅЩњГЩСПШчЯТБэЃК

БэжаЪ§ОнxЕФЗЖЮЇЪЧ__________________ЃЛЪЕбщЂйЂкЂнЬНОПЕФЪЧ_____________ЁЃ
ЁОД№АИЁПНЋХЈH2SO4МгШыввДМжаЃЌБпМгБпеёЕДЃЌШЛКѓМгШыввЫс(ЛђЯШНЋввДМгыввЫсЛьКЯКѓдйМгХЈСђЫсВЂдкМгШыЙ§ГЬжаВЛЖЯеёЕД) ДпЛЏМСЁЂЮќЫЎМС CH3COOHЃЋCH3CH2![]() OH
OH![]() CH3CO18OCH2CH3ЃЋH2O BC ДѓЛ№МгШШЛсЕМжТДѓСПЕФдСЯЦјЛЏЖјЫ№ЪЇ вКЬхЗжВуЃЌЩЯВуЮЊЮоЩЋгаЯуЮЖвКЬхЃЌЯТВуЮЊЧГКьЩЋвКЬхЃЌеёЕДКѓЯТВувКЬхбеЩЋБфЧГ ЗжвКТЉЖЗ ЩЯПкЕЙ 1.57ЁЋ1.76 діМгввДМЛђввЫсЕФгУСПЖдѕЅЕФВњСПЕФгАЯь
CH3CO18OCH2CH3ЃЋH2O BC ДѓЛ№МгШШЛсЕМжТДѓСПЕФдСЯЦјЛЏЖјЫ№ЪЇ вКЬхЗжВуЃЌЩЯВуЮЊЮоЩЋгаЯуЮЖвКЬхЃЌЯТВуЮЊЧГКьЩЋвКЬхЃЌеёЕДКѓЯТВувКЬхбеЩЋБфЧГ ЗжвКТЉЖЗ ЩЯПкЕЙ 1.57ЁЋ1.76 діМгввДМЛђввЫсЕФгУСПЖдѕЅЕФВњСПЕФгАЯь
ЁОНтЮіЁП
(1).ХЈСђЫсЕФУмЖШДѓгкввДМЁЂввЫсЃЌЛьКЯЪБвЊАбСђЫсМгШыввДМЁЂввЫсжаЃЛѕЅЛЏЗДгІЕФЛњРэЪЧЫсЭбєЧЛљДМЭбЧтЃЌЙЪЩњГЩЕФѕЅжаКЌга18OЃЛ
(2)БЅКЭЬМЫсФЦШмвКПЩГ§ШЅЛьШыввЫсввѕЅжаЕФввЫсЃЌШмНтввДМЃЌНЕЕЭввЫсввѕЅЕФШмНтЖШВЂгаРћгквКЬхЗжВуЁЃ
(3)ввЫсЁЂввДМвзЛгЗЂЃЛввЫсввѕЅЪЧУмЖШБШЫЎаЁЕФгЭзДвКЬхЃЌФбШмгкЫЎЃЌгаЯуЮЖЃЛгУЗжвКЗЈЗжРыЛЅВЛЯрШмЕФвКЬхЃЛ
(4)діМгввДМЕФСПЃЌЦНКте§ЯђвЦЖЏЃЛЂкЂнгыЂйЯрБШдіМгСЫ1mL ввДМЛђввЫсЃЛ
(1)ЛьКЯЪБХЈСђЫсЯрЕБгкБЛЯЁЪЭЃЌЙЪгІНЋХЈH2SO4МгШыввДМжаЃЌШЛКѓМгШыввЫсЃЌвВПЩЯШНЋввДМгыввЫсЛьКЯКУКѓдйМгШыХЈСђЫсЃЛвђѕЅЛЏЗДгІЫйТЪТ§ЧвЮЊПЩФцЗДгІЃЌЪЙгУХЈСђЫсПЩМгПьѕЅЛЏЗДгІЕФЫйТЪЃЌХЈСђЫсОпгаЮќЫЎадЃЌВЂгаРћгкЦНКтЯђЩњГЩѕЅЕФЗНЯђвЦЖЏЃЛввЫсЁЂввДМдкХЈСђЫсзїгУЯТЩњГЩввЫсввѕЅКЭЫЎЃЌИљОнѕЅЛЏЗДгІЕФЛњРэЪЧЫсЭбєЧЛљДМЭбЧтЃЌЙЪЩњГЩЕФѕЅжаКЌга18OЃЌЗДгІЕФЗНГЬЪНЪЧCH3COOHЃЋCH3CH2![]() OH
OH![]() CH3CO18OCH2CH3ЃЋH2OЃЛ
CH3CO18OCH2CH3ЃЋH2OЃЛ
(2) БЅКЭЬМЫсФЦШмвКПЩГ§ШЅЛьШыввЫсввѕЅжаЕФввЫсЃЌШмНтввДМЃЌНЕЕЭввЫсввѕЅЕФШмНтЖШВЂгаРћгквКЬхЗжВуЃЌЙЪбЁBCЃЛ
(3)гЩБэжаЪ§ОнжЊввДМЕФЗаЕу(78.0 Ёц)гыввЫсввѕЅЕФЗаЕу(77.5 Ёц)КмНгНќЃЌШєгУДѓЛ№МгШШЃЌДѓСПЕФввДМЛсБЛеєЗЂГіРДЃЌЕМжТдСЯЕФДѓСПЫ№ЪЇЃЛѕЅЕФУмЖШаЁгкЫЎЕФУмЖШЃЌЙЪЩЯВуЮЊгЭзДгаЯуЮЖЕФЮоЩЋвКЬхЃЌвђгавЛЖЈСПЕФввЫсЦјЛЏЃЌНјШыввжагыNa2CO3ЗДгІЃЌЙЪЯТВувКЬхКьЩЋБфЧГЃЛНЋЗжВуЕФвКЬхЗжРыПЊБиаыЪЙгУЗжвКТЉЖЗЃЌЗжвКЪБЩЯВувКЬхгІДгЩЯПкЕЙГіЃЛ
(4) діМгввДМЕФСПЃЌЦНКте§ЯђвЦЖЏЃЌЫљвдЪ§ОнxЕФЗЖЮЇЪЧ1.57ЁЋ1.76ЃЛЂкЂнгыЂйЯрБШдіМгСЫ1mL ввДМЛђввЫсЃЌЪЕбщЂйЂкЂнЬНОПЕФЪЧввДМЁЂввЫсгУСПЕФИФБфЖдѕЅВњТЪЕФгАЯьЧщПіЃЌЗжЮіШ§зщЪЕбщЪ§ОнжЊЃЌдіМгввДМЁЂввЫсЕФгУСПЃЌѕЅЕФЩњГЩСПОљЛсдіМгЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЙигкБНЕФа№Ъіе§ШЗЕФЪЧЃЈ ЃЉ
A.БНЕФЗжзгЪНЮЊC6H6ЃЌЫќВЛФмЪЙЫсадKMnO4ШмвКЭЪЩЋЃЌЪєгкБЅКЭЬў
B.ДгБНЕФППтРеЪН(![]() )ПДЃЌБНЗжзгжаКЌгаЬМЬМЫЋМќЃЌгІЪєгкЯЉЬў
)ПДЃЌБНЗжзгжаКЌгаЬМЬМЫЋМќЃЌгІЪєгкЯЉЬў
C.дкДпЛЏМСзїгУЯТЃЌБНгывКфхЗДгІЩњГЩфхБНЃЌЗЂЩњСЫМгГЩЗДгІ
D.БНЗжзгЮЊЦНУце§СљБпаЮНсЙЙЃЌ6ИіЬМдзгжЎМфЕФМлМќЭъШЋЯрЭЌ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁП25ЁцЪБЃЌЯђ0.1mol/LCH3COOHШмвКжаж№НЅМгШыNaOHЙЬЬхЃЌЛжИДжСдЮТЖШКѓШмвКжаЕФЙиЯЕШчЭМЫљЪО(КіТдШмвКЬхЛ§БфЛЏ)ЁЃЯТСагаЙиа№ЪіВЛе§ШЗЕФЪЧЃЈ ЃЉ

A.CH3COOHЕФKa=1.0ЁС10-4.7
B.CЕуЕФШмвКжаЃКc(Na+)ЃОc(CH3COO-)ЃОc(OH-)ЃОc(H+)
C.BЕуЕФШмвКжаЃКc(Na+)ЃЋc(H+)=c(CH3COOH)ЃЋc(OH-)
D.AЕуЕФШмвКжаЃКc(CH3COO-)ЃЋc(H+)ЃЋc(CH3COOH)Ѓc(OH-)=0.1mol/L
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊЃК (1)Fe2O3(s)+![]() C(s)ЃН
C(s)ЃН![]() CO2(g)+2Fe(s)ЃЌІЄHЃН+234.1kJmol-1
CO2(g)+2Fe(s)ЃЌІЄHЃН+234.1kJmol-1
![]() дђ
дђ![]() ЕФІЄHЪЧЃЈ ЃЉ
ЕФІЄHЪЧЃЈ ЃЉ
A.Ѓ824.4 kJmol-1B.Ѓ627.6kJmol-1C.-744.7kJmol-1D.-169.4kJmol-1
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЪвЮТЯТЃЌгУ0.10 molЁЄLЃ1KOHШмвКЕЮЖЈ10.00 mL 0.10 molЁЄLЃ1H2C2O4(ЖўдЊШѕЫс)ШмвКЫљЕУЕЮЖЈЧњЯпШчЭМ(ЛьКЯШмвКЕФЬхЛ§ПЩПДГЩЛьКЯЧАШмвКЕФЬхЛ§жЎКЭ)ЁЃЧыЛиД№ЯТСаЮЪЬтЃК

ЃЈ1ЃЉЕуЂйЫљЪОШмвКжаЃЌKwЃН__________ЁЃ
ЃЈ2ЃЉЕуЂкЫљЪОШмвКжаЕФЕчКЩЪиКуЪНЮЊ______________________________________ЁЃ
ЃЈ3ЃЉЕуЂлЫљЪОШмвКжаДцдк________жжЦНКтЁЃ
ЃЈ4ЃЉЕуЂмЫљЪОШмвКжаЕФЮяСЯЪиКуЪНЮЊ0.10 molЁЄLЃ1ЃН___________________________ЁЃ
ЃЈ5ЃЉЕуЂнЫљЪОШмвКжаИїРызгХЈЖШЕФДѓаЁЫГађЮЊ________________________________ЁЃ
ЃЈ6ЃЉЩЯЪі5ЕуЫљЪОШмвКжаЃЌЫЎЕФЕчРыГЬЖШзюДѓЕФЪЧ_______ЃЌзюаЁЕФЪЧ________(гУађКХЛиД№)ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвдШлШкЕФЬМЫсбЮЃЈK2CO3ЃЉЮЊЕчНтвК,ХнФФјЮЊЕчМЋ,бѕЛЏЯЫЮЌВМЮЊИєФЄЃЈНідЪаэвѕРызгЭЈЙ§ЃЉПЩЙЙГЩжБНгЬМШМСЯЕчГи,ЦфНсЙЙШчЭМЫљЪОЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ
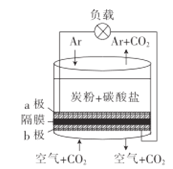
A.ИУЕчГиЙЄзїЪБ,CO32-ЭЈЙ§ИєФЄвЦЖЏЕНaМЋ
B.ШєaМЋЭЈШыПеЦј,ИКдиЭЈЙ§ЕФЕчСїНЋдіДѓ
C.bМЋЕФЕчМЋЗДгІЪНЮЊ2CO2+O2-4e- =2CO32-
D.ЮЊЪЙЕчГиГжајЙЄзї,РэТлЩЯашвЊВЙГфK2CO3
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСабЁЯюжаЕФдвђЛђНсТлгыЯжЯѓВЛЖдгІЕФЪЧЃЈ ЃЉ
бЁЯю | ЯжЯѓ | двђЛђНсТл |
A | дкH2O2жаМгШыMnO2ЃЌФмМгЫйH2O2ЕФЗжНтЫйТЪ | MnO2НЕЕЭСЫЗДгІЫљашЕФЛюЛЏФм |
B | Яђ5mL 0.005molЁЄL-1FeCl3ШмвКжаМгШы5mL0.010molЁЄL-1KSCNШмвКЃЌШмвКГЪКьЩЋЃЌдйЕЮМг1ml1 molЁЄL-1KClШмвКЃЌШмвКбеЩЋБфЧГ | діДѓЩњГЩЮяХЈЖШЃЌЦНКтЯђФцЗДгІЗНЯђвЦЖЏ |
C | НЋЪЂгаNO2ЦјЬхЕФУмБеШнЦїНўХндкШШЫЎжаЃЌШнЦїФкЦјЬхбеЩЋБфЩю | 2NO2ЃЈgЃЉ |
D | дкУмБеШнЦїжагаЗДгІЃКA+xBЃЈgЃЉ | ШєAЮЊЦјЬхЁЂx>1 |
A.AB.BC.CD.D
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
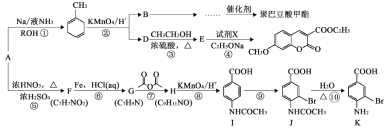
ЁОЬтФПЁПЗМЯуЬўAЃЈC7H8ЃЉЪЧживЊЕФгаЛњЛЏЙЄдСЯЃЌгЩAжЦБИОлАЭЖЙЫсМзѕЅКЭвНвЉжаМфЬхKЕФКЯГЩТЗЯпЃЈВПЗжЗДгІЬѕМўТдШЅЃЉШчЭМЫљЪОЃК
вбжЊЃКЂй![]()
Ђк![]()
Ђл![]() ЃЈШѕМюадЃЌвзбѕЛЏЃЉ
ЃЈШѕМюадЃЌвзбѕЛЏЃЉ
ЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉAЕФУћГЦЪЧ____________ЃЌIКЌгаЕФЙйФмЭХЪЧ_______________________ЁЃ
ЃЈ2ЃЉЂкЕФЗДгІРраЭЪЧ______________ЃЌЂнЕФЗДгІРраЭЪЧ__________________ЁЃ
ЃЈ3ЃЉBЁЂЪдМСXЕФНсЙЙМђЪНЗжБ№ЮЊ____________________ЁЂ____________________ЁЃ
ЃЈ4ЃЉАЭЖЙЫсЕФЛЏбЇУћГЦЮЊ2-ЖЁЯЉЫсЃЌгаЫГЪНКЭЗДЪНжЎЗжЃЌАЭЖЙЫсЗжзгжазюЖрга_____ИідзгЙВЦНУцЃЌЗДЪНАЭЖЙЫсЕФНсЙЙМђЪНЮЊ__________________________ЁЃ
ЃЈ5ЃЉЕкЂпЂтСНИіВНжшЕФФПЕФЪЧ______________ЁЃ
ЃЈ6ЃЉМШФмЗЂЩњвјОЕЗДгІгжФмЗЂЩњЫЎНтЗДгІЕФЖўдЊШЁДњЗМЯуЛЏКЯЮяWЪЧFЕФЭЌЗжвьЙЙЬхЃЌWЙВга_______жжЃЌЦфжаБНЛЗЩЯжЛгаСНжжВЛЭЌЛЏбЇЛЗОГЕФЧтдзгЧвЪєгкѕЅРрЕФНсЙЙМђЪНЮЊ___________________ЁЃ
ЃЈ7ЃЉНЋгЩBЁЂМзДМЮЊЦ№ЪМдСЯжЦБИОлАЭЖЙЫсМзѕЅЕФКЯГЩТЗЯпВЙГфЭъећЃЈЮоЛњЪдМСМАШмМСШЮбЁЃЉЁЃ________________
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЕэЗлЫЎНтЕФВњЮяЃЈC6H12O6ЃЉгУЯѕЫсбѕЛЏПЩвджЦБИВнЫсЃЌзАжУШчЭМ1ЫљЪОЃЈМгШШЁЂНСАшКЭвЧЦїЙЬЖЈзАжУОљвбТдШЅЃЉЃКЪЕбщЙ§ГЬШчЯТЃК
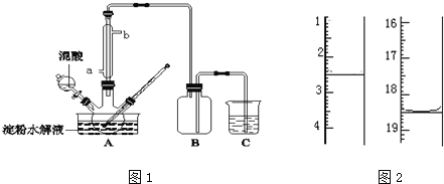
ЂйНЋ1ЃК1ЕФЕэЗлЫЎШщвКгыЩйаэСђЫсЃЈ98%ЃЉМгШыЩеБжаЃЌЫЎдЁМгШШжС85ЁцЁЋ90ЁцЃЌБЃГж30minЃЌШЛКѓж№НЅНЋЮТЖШНЕжС60ЁцзѓгвЃЛ
ЂкНЋвЛЖЈСПЕФЕэЗлЫЎНтвКМгШыШ§ОБЩеЦПжаЃЛ
ЂлПижЦЗДгІвКЮТЖШдк55ЁЋ60ЁцЬѕМўЯТЃЌБпНСАшБпЛКТ§ЕЮМгвЛЖЈСПКЌгаЪЪСПДпЛЏМСЕФЛьЫсЃЈ65%HNO3гы98%H2SO4ЕФжЪСПБШЮЊ2ЃК1.5ЃЉШмвКЃЛ
ЂмЗДгІ3hзѓгвЃЌРфШДЃЌМѕбЙЙ§ТЫКѓдйжиНсОЇЕУВнЫсОЇЬхЃЌЯѕЫсбѕЛЏЕэЗлЫЎНтвКЙ§ГЬжаПЩЗЂЩњЯТСаЗДгІЃК
C6H12O6+12HNO3Ёњ3H2C2O4+9NO2Ёќ+3NOЁќ+9H2O
C6H12O6+8HNO3Ёњ6CO2+8NOЁќ+10H2O
3H2C2O4+2HNO3Ёњ6CO2+2NOЁќ+4H2O
ЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉЪЕбщЂйМгШы98%СђЫсЩйаэЕФзїгУЪЧЃК_________ЃЛ
ЃЈ2ЃЉЪЕбщжаШєЛьЫсЕЮМгЙ§ПьЃЌНЋЕМжТВнЫсВњСПЯТНЕЃЌЦфдвђЪЧ_________ЃЛ
ЃЈ3ЃЉМьбщЕэЗлЪЧЗёЫЎНтЭъШЋЫљгУЕФЪдМСЮЊ_________ЃЛ
ЃЈ4ЃЉВнЫсжиНсОЇЕФМѕбЙЙ§ТЫВйзїжаЃЌГ§ЩеБЁЂВЃСЇАєЭтЃЌЛЙБиаыЪЙгУЪєгкЙшЫсбЮВФСЯЕФвЧЦїга_________ЃЛ
ЃЈ5ЃЉНЋВњЦЗдкКуЮТЯфФкдМ90ЁцвдЯТКцИЩжСКужиЃЌЕУЕНЖўЫЎКЯВнЫсЃЎгУKMnO4БъзМШмвКЕЮЖЈЃЌИУЗДгІЕФРызгЗНГЬЪНЮЊЃК2MnO4Љ+5H2C2O4+6H+=2Mn2++10CO2Ёќ+8H2OГЦШЁИУбљЦЗ0.12gЃЌМгЪЪСПЫЎЭъШЋШмНтЃЌШЛКѓгУ0.020molLЉ1ЕФЫсадKMnO4ШмвКЕЮЖЈжСжеЕуЃЈдгжЪВЛВЮгыЗДгІЃЉЃЌДЫЪБШмвКбеЩЋБфЛЏЮЊ_________ЃЌЕЮЖЈЧАКѓЕЮЖЈЙмжаЕФвКУцЖСЪ§ШчЭМ2ЫљЪОЃЌдђИУВнЫсОЇЬхбљЦЗжаЖўЫЎКЯВнЫсЕФжЪСПЗжЪ§ЮЊ_________ЁЃ
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com