
【题目】回收利用炼铜工业产生的排放物,既能节约资源,又能保护环境.
(1)用足量氨水吸收尾气中的SO2后,再加入硫酸,可获得SO2和(NH4)2SO4两种产品.相关反应的化学方程式为________、________.
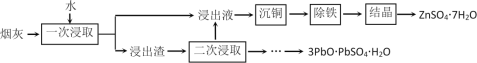
(2)烟灰中金属元素以硫酸盐和氧化物形态存在,其中锌、铅的含量最大,其次为铜、铁等.烟灰的回收利用工艺如下:
①“沉铜”可得到单质铜,该步骤应加入的试剂是________.
② “一次浸取”铜浸出率较低,原因是烟灰中部分铜元素以________(填化学式)残留在浸出渣中,“二次浸取”应选择_________(填化学式)作浸取剂.
(3)从贵金属阳极泥中可提取粗银.电解法精炼粗银时采用AgNO3和HNO3的混合液作电解液,阴极的主要电极反应式为________.阴极还有少量副反应发生,产生的气体遇空气迅速变为红棕色,该副反应的电极反应式为________.
【答案】(1)SO2+2NH3·H2O=(NH4)2SO3+H2O(2分) (生成物写NH4HSO3也得分)
(NH4)2SO3+H2SO4=(NH4)2SO4+SO2↑+H2O (2分)
(2)①锌粉(或铁粉) (3分) ② CuO (2分) H2SO4(2分)
(3)Ag++e—=Ag(2分) NO3—+4H++3e—=NO↑+2H2O (3分)
【解析】
试题(1)氨水吸收尾气中的SO2后生成亚硫酸铵,方程式为SO2+2NH3·H2O=(NH4)2SO3+H2O。亚硫酸铵与硫酸反应生成硫酸铵、SO2和水,因此再加入硫酸,可获得SO2,反应的化学方程式为(NH4)2SO3+H2SO4=(NH4)2SO4+SO2↑+H2O。
(2)①由于最终要获得硫酸锌晶体,因此根据不能引入杂质可判断“沉铜”时应该加入还原剂锌。
② 由于烟灰中部分铜以氧化物氧化铜的形成存在,而氧化铜不溶于水,所以“一次浸取”铜浸出率较低。氧化铜不溶于水,但可溶于稀硫酸中,则“二次浸取”应选择H2SO4作浸取剂。
(3)电解法精炼粗银时采用AgNO3和HNO3的混合液作电解液,阴极是溶液中的银离子放电,则主要电极反应式为Ag++e—=Ag。阴极还有少量副反应发生,产生的气体遇空气迅速变为红棕色,这说明应该是溶液中的硝酸根得到电子转化为NO,NO被氧化为红棕色NO2,因此该副反应的电极反应式为NO3—+4H++3e—=NO↑+2H2O。


科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题。(除特别注明外,其他一律用化学式表示)

(1)在这些元素中,化学性质最不活泼的元素的原子结构示意图为____________。
(2)元素E的最高价氧化物的电子式是________________。
(3)某元素二价阳离子的核外有10个电子,该元素是____________(填元素名称)。
(4)G、H、I形成的气态氢化物稳定性由强到弱的顺序: _________________。
(5)H、J、K的最高价氧化物的水化物的酸性由强到弱的顺序: ______________。
(6)元素B的最高氧化物的水化物的电子式是______________,化合物类型为________________(填“离子化合物”或“共价化合物”)。
(7)元素I的氢化物的结构式为____________;该氢化物常温下和元素K的单质反应的化学方程式为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组设计实验制备Ca(NO2)2,实验装置如图所示(夹持装置已略去)。已知:2NO+CaO2==Ca(NO2)2;2NO2+CaO2==Ca(NO3)2。下列说法不正确的是
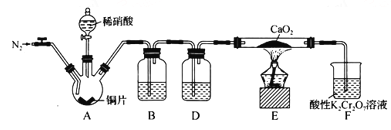
A. 通入N2是为了排尽装置中的空气
B. 装置B、D中的试剂可分别为水和浓硫酸
C. 将铜片换成木炭也可以制备纯净的亚硝酸钙
D. 借助装置A及氢氧化钠溶液和稀硫酸可以分离CO2和CO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组用下图装置进行实验,试回答:
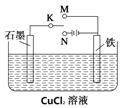
(1)若开始时K接M,则该装置为________(填“原电池”或“电解池”),铁极上的电极反应式为__________________。
(2)若开始时K接N,则石墨极为______极(填“正”、“负”、“阳” 或“阴”),石墨电极的电极反应式为______________________,铁极上的现象为_____________,若反应过程中有0.2mol的电子发生转移,则铁电极上产生物质的质量为________g,石墨极上产生的物质在标准状况下的体积为_____________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,若VL甲烷中含有的氢原子个数为b,则阿伏加德罗常数可表示为 ( )
A. Vb/22.4 B. 22.4b/V C. Vb/5.6 D. 5.6b/V
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在空气中的自由离子附着在分子或原子上形成的空气负离子被称为“空气维生素”。O22—就是一种空气负离子,则O22—的摩尔质量为
A. 32g B. 34g C. 32g/mol D. 34g·mol—1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com