
核黄素又称维生素B2,可促进发育和细胞再生,有利于增进视力,减轻眼睛疲劳,核黄素分子的结构为:

已知: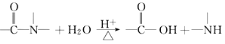
有关核黄素的下列说法中,不正确的是( )
A.该化合物的分子式为C17H22N4O6
B.酸性条件下加热水解,有CO2生成
C.酸性条件下加热水解,所得溶 液加碱后有NH3生成
D.能发生酯化反应
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源:2016届湖北省高三5月模拟四理综化学试卷(解析版) 题型:简答题
四川含有丰富的矿产资源,钒矿、硫铁矿、铜矿等七种矿产储量位居全国前列。回答下列问题:
(1)钒在元素周期表中的位置为 ,V3+的价电子排布图为 。
(2)钒的某种氧化物的晶胞结构如图1所示,其晶体的化学式为
(3)V2O5常用作SO2 转化为SO3的催化剂。SO2 分子中键角 120°(填“>”、“<”或“=”); SO3的三聚体环状结构如图2所示,该结构中S—O键长有两类,一类键长约140pm,另一类键长约为160pm,较短的键为 (填图2中字母),该分子中含有 个σ键。
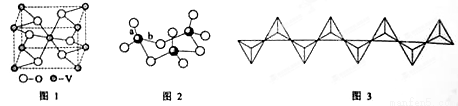
(4)V2O5 溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为 ,例举与VO43-空间构型相同的一种阳离子和一种阴离子 (填化学式);也可以得到偏钒酸钠,其阴离子呈如图3所示的无限链状结构,则偏钒酸钠的化学式为 。
(5)硫能形成很多种含氧酸,如H2SO3、H2SO4。硫的某种含氧酸分子式为H2S2O7,属于二元酸,已知其结构中所有原子都达到稳定结构,且不存在非极性键,试写出其结构式 (配位键须注明)。
(6)利用铜萃取剂M,通过如下反应实现铜离子的富集:

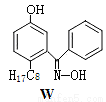
M与W(分子结构如图)相比,M的水溶性小,更利于Cu2+的萃取。M水溶性小的主要原因是
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三高考打靶测试理综化学试卷(解析版) 题型:实验题
(14分)ClO2在常温下是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11℃,易溶于水,是常见的消毒剂。工业上常用二氧化硫还原氯酸钠(NaClO3)的方法制备ClO2,某学生拟用下图所示装置模拟工业制取并收集少量ClO2。
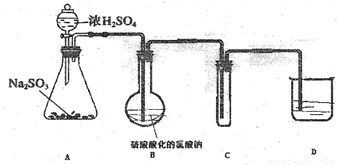
(1)下列制备气体所用装置与A装置相同的是_______________;
a.用过氧化氢与二氧化锰制氧气
b.用铜与浓硫酸制二氧化硫
c.用硫化亚铁与稀硫酸制硫化氢
d.只用浓氨水制氨气
(2)实验前,要检验装置的气密性,通常先___________________,将导气管插入盛有水的烧杯中,微热锥形瓶,若导管未端产生气泡,并在停止微热后,___________________,说明装置不漏气。
(3)二氧化硫与氯酸钠的反应需在75~90℃进行,为此,B装置必须添加温度控制装置,除酒精灯外,还需要的玻璃仪器有烧杯、_________;写出B中产生二氧化氯的离子方程式_________________;
(4)C装置放在冰水浴中,其原因是_________________;
(5)用氢氧化钠溶液吸收ClO2,反应后可得到NaClO2与NaClO3混合液。
已知:NaClO2饱和溶液在较低温度时析出晶体NaClO2·3H2O,在较高温度时析出晶体 NaClO2;NaClO在高温时溶解度很大。
则从该混合溶液中获得晶体NaClO2的操作步骤为:①蒸发浓缩结晶;②_________;③洗涤干燥。
(6)碘量法可以检测水中ClO2的浓度,步骤如下:
①取1L水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝;(ClO2全部转化为NaClO2)
②用1.0×10-3 mol•L-1的Na2S2O3溶液滴定,消耗Na2S2O3溶液10.00mL;(已知:2S2O32-+I2═S4O62-+2I-)
确定操作②达到滴定终点的现象是_________________________________;
经计算,水样中ClO2的浓度是__________mg•L-1,若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果____________;(填“偏高”、“偏低”或“不变”)
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高三全真模拟理综化学试卷(解析版) 题型:选择题
NA为阿伏加罗常数的值,下列说法中正确的是( )
A.44gCO2和N2O的混合物中含有的氧原子数为1.5NA
B.2L0.5mol/L亚硫酸氢钠溶液中含有的HSO3-离子数为NA
C.氢氧化钠与氯气反应时,生成0.1molNaCl转移的电子数为0.1NA
D.一定条件下在密闭容器中2molSO2与2molO2充分反应,最终的气体分子数为3NA
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三考前热身理综化学试卷(解析版) 题型:实验题
某实验室小组偶然发现将镁条插入饱和NaHCO3溶液中,镁条表面出现大量气泡。为了探究产生此现象的原因,该小组设计实验探究如下:
(1)用固体NaHCO3配置饱和NaHCO3溶液的操作过程 。
饱和NaH CO3溶液pH=8.4,用离子方程式表示
CO3溶液pH=8.4,用离子方程式表示  。
。
(2)请完成以下实验设计(镁条已擦去氧化膜且表面积大致相同。表中不要留空格):
序号 | 实验操作 | 实验现象 | 实验结论 |
1 | 将镁条投入5ml蒸馏水 | 微量气泡 | |
2 | 将镁条投入5ml饱和NaHCO3溶液中 | Mg与NaHCO3溶液剧烈反应 | |
3 | 将镁条投入5ml pH= NaOH溶液中 | 现象不明显 | Mg与NaOH溶液较难反应 |
(3)对于反应②中产生的气体(不考虑水蒸气),请你完成假设二和假设三:
假设一:只有CO2;假设二:只有 ;假设三:
(各1分)
为检验其中是否含有CO2,写出实验步骤和结论。
实验步骤 | 想象和结论 |
大试管中加入擦去氧化膜的镁条
|
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三考前模拟理综化学试卷(解析版) 题型:推断题
高分子化合物 PPTA 树脂、PF 树脂、脲醛树脂合成路线如下。

已知:I.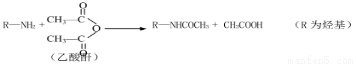
II. (尿素)氮原子上的氢原子可以像苯酚上的氢原子那样与甲醛发生加成反应,并缩聚成高分子。
(尿素)氮原子上的氢原子可以像苯酚上的氢原子那样与甲醛发生加成反应,并缩聚成高分子。
(1)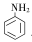 →B 的反应类型是____________________。
→B 的反应类型是____________________。
(2)条件a选择的化学试剂是____________________。
(3)E中有两种不同化学环境的氢原子,PPTA 树脂的结构简式是____________________。
(4)W中只有一种含氧官能团。下列说法正确的是____________。
a.Y分子中只有一种官能团
b.M与HCHO 互为同系物
c.W的沸点高于C2H6
(5)Y→W 时,条件ⅰ、ⅱ转化的官能团分别是____________、____________。
(6)合成脲醛树脂的化学方程式是___________________。
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三考前模拟理综化学试卷(解析版) 题型:选择题
有四种短周期元素 A、B、C、D,其中 A、B、C 在周期表中所处的位置如图所示,且它们的质子数之和为 32。D 元素原子的最外层电子数为次外层电子数的 2 倍。则下列说法正确的是( )
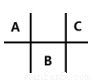
A.元素D形成的气态氢化物的空间结构一定是正四面体
B.A、B 两种元素的气态氢化物均能不它们的最高价氧化物对应的水化物发生反应,且反应类型相同
C.DB2 、DC4中每个原子都满足8电子稳定结构
D.四种元素形成的气态氢化物中,C元素形成的氢化物的稳定性最高
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二6月月考化学试卷(解析版) 题型:选择题
下列实验不能达到预期目的的是
①实验室用无水乙醇加热至170 ℃,可制得乙烯
②只用新制氢氧化铜悬浊液(可以加热)可将乙醇、乙醛、乙酸三种液体区别出来
③在混有杂质苯酚的苯中,加入适量溴水,过滤后得到纯净的苯
④在10%的NaOH溶液中滴入2%的CuSO4溶液至过量,再加入乙醛溶液加热至沸腾,溶液中有砖红色沉淀产生
⑤用饱和Na2CO3溶液除去乙酸乙酯中混有的乙酸
⑥将溴乙烷与NaOH溶液共热几分钟后冷却,滴入AgNO3溶液,观察沉淀颜色,可用来检验溴乙烷中溴元素的存在
A.①②④⑤ B.②③⑤⑥ C.①④⑤⑥ D.①③④⑥
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二6月月考化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.一定温度、压强下,气体体积由其分子的大小决定
B.一定温度、压强下,气体体积由其物质的量的多少决定
C.气体摩尔体积是指1mol任何气体所占的体积为22.4L
D.不同的气体,若体积不等,则它们所含的分子数一定不等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com