
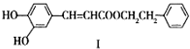 不饱和酯类化合物在药物、涂料等方面应用广泛.
不饱和酯类化合物在药物、涂料等方面应用广泛. .
.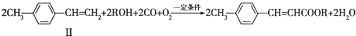
 (写1种);由Ⅳ生成Ⅱ的反应条件为氢氧化钠的醇溶液、加热.
(写1种);由Ⅳ生成Ⅱ的反应条件为氢氧化钠的醇溶液、加热.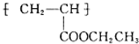 可用于制备涂料.其单体的结构简式为CH2=CHCOOCH2CH3.利用类似反应①的方法,仅以乙烯为有机原料合成该单体,涉及的反应方程式为CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3CH2OH,2CH2=CH2+2CH3CH2OH+2CO+O2$\stackrel{一定条件}{→}$2CH2=CHCOOCH2CH3+2H2O.
可用于制备涂料.其单体的结构简式为CH2=CHCOOCH2CH3.利用类似反应①的方法,仅以乙烯为有机原料合成该单体,涉及的反应方程式为CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3CH2OH,2CH2=CH2+2CH3CH2OH+2CO+O2$\stackrel{一定条件}{→}$2CH2=CHCOOCH2CH3+2H2O. 分析 (1)由化合物I的结构可知,含有的含氧官能团为羟基、酯基,碳碳双键能与溴发生加成反应,酚羟基的、邻位、对位可以与溴发生取代反应;
(2)酚羟基能与氢氧化钠发生中和反应,酯基能与氢氧化钠发生反应;
(3)Ⅱ中含有9个C原子、10个H原子,据此确定化学式;能和氢气发生加成反应的有苯环和碳碳双键;
(4)化合物Ⅱ可由芳香族化合物Ⅲ或Ⅳ分别通过消去反应获得,但只有Ⅲ能与Na反应产生H2,说明Ⅲ中含有醇羟基,且羟基连接碳原子相邻的碳原子上含有H原子;Ⅳ是卤代烃,卤代烃和氢氧化钠的醇溶液、加热发生消去反应;
(5)聚合物 可用于制备涂料,其单体为丙烯酸乙酯,利用类似反应①的方法,仅以乙烯为有机物原料合成该单体,醇为乙醇,根据反应①书写反应方程式.
可用于制备涂料,其单体为丙烯酸乙酯,利用类似反应①的方法,仅以乙烯为有机物原料合成该单体,醇为乙醇,根据反应①书写反应方程式.
解答 解:(1)由化合物I的结构可知,含有的含氧官能团为羟基、酯基,碳碳双键能与溴发生加成反应,酚羟基的、邻位、对位可以与溴发生取代反应,1mol化合物Ⅰ最多能与4molBr2发生反应,
故答案为:羟基、酯基;4;
(2)酚羟基能与氢氧化钠发生中和反应,酯基能与氢氧化钠发生反应,化合物Ⅰ与NaOH反应的化学方程式: ,
,
故答案为: ;
;
(3)Ⅱ中含有9个C原子、10个H原子,其化学式为C9H10;能和氢气发生加成反应的有苯环和碳碳双键,1mol化合物Ⅱ能与4mol H2恰好完全反应生成饱和烃类化合物,
故答案为:C9H10;4;
(4)化合物Ⅱ可由芳香族化合物Ⅲ或Ⅳ分别通过消去反应获得,但只有Ⅲ能与Na反应产生H2,说明Ⅲ中含有醇羟基,且羟基连接碳原子相邻的碳原子上含有H原子,结构简式为 ;Ⅳ是卤代烃,卤代烃和氢氧化钠的醇溶液、加热条件下发生消去反应,
;Ⅳ是卤代烃,卤代烃和氢氧化钠的醇溶液、加热条件下发生消去反应,
故答案为: ;氢氧化钠的醇溶液、加热;
;氢氧化钠的醇溶液、加热;
(5)聚合物 可用于制备涂料,其单体为丙烯酸乙酯,结构简式为CH2=CHCOOCH2CH3,利用类似反应①的方法,仅以乙烯为有机物原料合成该单体,醇为乙醇,根据反应①书写反应方程式,该反应方程式为:CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3CH2OH,2CH2=CH2+2CH3CH2OH+2CO+O2$\stackrel{一定条件}{→}$2CH2=CHCOOCH2CH3+2H2O,
可用于制备涂料,其单体为丙烯酸乙酯,结构简式为CH2=CHCOOCH2CH3,利用类似反应①的方法,仅以乙烯为有机物原料合成该单体,醇为乙醇,根据反应①书写反应方程式,该反应方程式为:CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3CH2OH,2CH2=CH2+2CH3CH2OH+2CO+O2$\stackrel{一定条件}{→}$2CH2=CHCOOCH2CH3+2H2O,
故答案为:CH2=CHCOOCH2CH3;CH2=CH2+H2O$\stackrel{一定条件}{→}$CH3CH2OH,2CH2=CH2+2CH3CH2OH+2CO+O2$\stackrel{一定条件}{→}$2CH2=CHCOOCH2CH3+2H2O.
点评 本题考查有机物的结构与性质、有机物的推断与合成等,熟练掌握官能团的结构与性质,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯聚合为聚乙烯高分子材料符合绿色化学原子经济性要求 | |
| B. | 银制品久置干燥空气中因电化学腐蚀而使表面变暗 | |
| C. | 重金属盐能使蛋白质变性,所以误食重金属盐会中毒 | |
| D. | 在合成洗涤剂中添加酶制剂可以提高洗涤效果 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

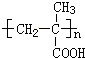 .
.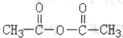 )作用制得.水杨酸的结构简式是
)作用制得.水杨酸的结构简式是 ,水杨酸可以看作羧酸类有机物,也可看作酚类有机物.
,水杨酸可以看作羧酸类有机物,也可看作酚类有机物.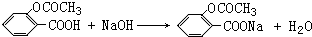 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钾投入水中 | B. | 镁条放入冷水中 | ||
| C. | KSCN溶液滴加到FeCl3溶液中 | D. | 氯水滴加到KI淀粉溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述实验中,只有一个氧化还原反应 | |
| B. | 实验①中 产物是Cl2 和HMnO4 | |
| C. | 实验①中浓盐酸不仅仅体现酸性 | |
| D. | 实验②可证明Fe2+既有氧化性又有还原性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com