
【题目】NA代表阿伏加德常数,下列说法正确的是
A. 在同温同压时,相同体积的任何气体单质所含的原子数目相同
B. 2g氢气所含原子数目为NA
C. 在常温常压下,11.2L氮气所含的原子数目为NA
D. 17g氨气所含电子数目为10NA
科目:高中化学 来源: 题型:
【题目】已知A(g)+B(g)![]() C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
830℃时,向一个2L的密闭容器中充入0.2mol的A和0.8mol的B,反应初始4s内A的平均反应速率v(A)=0.005 mol/(L·s)。下列说法正确的是
A. 4s时c(B)为0.78 mol/L
B. 该反应AH>0
C. 830℃达平衡时,A的转化率为20%
D. 1200℃时反应C(g)+D(g)![]() A(g)+B(g)的平衡常数为2.5
A(g)+B(g)的平衡常数为2.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由硫酸钾、硫酸铝和硫酸组成的混合溶液,其中c(H+)=0.2mol/L,c(Al3+)=0.2mol/L,c(SO42-)=0.5mol/L,则c(K+)为( )
A. 0.1mol/L B. 0.2mol/L C. 0.3mol/L D. 0.4mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若NA表示阿伏加德罗常数,下列说法中,正确的是
A.1 mol Cl2作为氧化剂得到的电子数为NA
B.在0 ℃,101 kPa时,22.4 L氢气中含有NA个氢原子
C.25 ℃,1.01×105 Pa,64 g SO2中含有的原子数为3 NA
D.NA个一氧化碳分子和0.5 mol甲烷的质量比为7∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。
I.将NaOH 溶液与NH4Cl 溶液混合生成NH3·H2O,从而验证NaOH 的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理? 并说明理由:_____。
II.根据下图所示装置图回答以下问题。
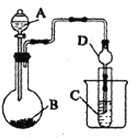
(1)利用如图装置可以验证非金属性的变化规律。图中A装置名称是_______。干燥管D的作用是___________。
(2)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫: 烧瓶中发生反应的离子方程式为_________。装置C中的实验现象为有淡黄色沉淀生成,离子方程式为_________。
(3)若要用此装置证明酸性: HNO3>H2CO3>H2SiO3进而证明非金属性: N>C>Si,从以下所给物质中选出甲同学设计的实验所用到物质:
①稀HNO3溶液②稀盐酸 ③碳酸钙 ④Na2SiO3 溶液 ⑤SiO2
试剂A与C分别为______(填序号);试管中发生反应的离子方程式为________。有同学认为此实验不能说明N、C、Si的非金属性强弱,你认为原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L电子层上有2对成对电子;E+原子核外有3层电子且各层均处于全满状态.请填写下列空白.
(1)E元素基态原子的核外电子排布式为 .
(2)B、C、D三种元素的第一电离能数值由小到大的顺序为(填元素符号),其原因为 .
(3)B2A4是重要的基本石油化工原料.B2A4分子中B原子轨道的杂化类型为;1mol B2A4分子中含molσ键.
(4)已知D、E能形成晶胞如图所示的两种化合物 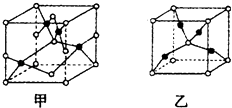 ,化合物的化学式,甲为 , 乙为;高温时,甲易转化为乙的原因为 .
,化合物的化学式,甲为 , 乙为;高温时,甲易转化为乙的原因为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是中学化学中常见物质的转化关系,部分物质和反应条件略去。
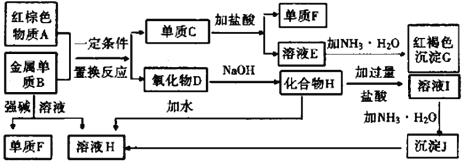
(1)如果把红棕色物质A换成黑色磁性晶体,推测出来的物质是完全一致的,请写出黑色磁性晶体与过量盐酸反应的化学方程式_______________________________。
(2)写出单质B与强碱溶液反应的离子方程式:_______________________________。把溶液Ⅰ中的阳离子完全转化为沉淀J为什么加氨水而不加氢氧化钠_______________。
(3)溶液E中加入氨水时,先生成白色沉淀L,写出生成L的离子方程式:_________________________。白色沉淀L最终变为红褐色沉淀G,写出L变为G的化学反应方程式_________________________。
(4)保存E溶液时候为什么要加入单质C,用离子方程式解释_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质制备的说法错误的是( )
A.我国古代就已采用加热胆矾或绿矾的方法制取硫酸
B.电解氯化镁溶液可以得到金属镁
C.钠可用于从钛的氯化物中置换出金属钛
D.工业上以氯气和石灰乳为原料制造漂白粉
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com