
一定量的CuS和Cu2S的混合物投入足量的HNO3中,收集到气体V L(标准状况),向反应后的溶液中(存在Cu2+和SO42一)加入足量NaOH,产生蓝色沉淀,过滤、洗涤、灼烧,得到CuO 12 g,若上述气体为NO和NO2的混合物,且体积比为1∶1,则V可能为
A.12.2 L B.14.5 L C.15.8 L D.16.4 L
【答案】A
【解析】
试题分析:1 mol CuS与HNO3失8 mol e-,1 mol Cu2S与HNO3失10 mol e-。若混合物中仅含有CuS,反应失电子(12/80)×8=1.2 mol;若原混合物中仅含有Cu2S,反应失电子(12/80)×10=1.5 mol,则混合物在反应中失去电子数1.2 mol< n(e-)<1.5 mol。而生成1 mol混合气体得到电子数为(5-4)×1/2+(5-2)×1/2=2 mol,由电子守恒可知,生成气体的的体积(1.2/2)×22.4 L < V <1.5/2×22.4 L,即13.44L<V<16.8L,选A。
考点:考查氧化还原反应。


科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.使用滴定管时,滴定管必须用待装液润洗2~3次
B.滴定操作中,若用待测液润洗锥形瓶,将导致测定结果偏高
C.用10 mL的量筒量取8.58 mL 0.10 mol·L-1的稀盐酸
D.稀释浓硫酸时,将浓硫酸缓缓加入水中,并不 断用玻璃棒搅拌
断用玻璃棒搅拌
查看答案和解析>>
科目:高中化学 来源: 题型:
用Cu(OH)2胶体做电泳实验时,阴极附近蓝色加深,往此胶体中加入下列物质时,都不发生凝聚的是
①硫酸镁溶液 ②硅酸胶体 ③氢氧化铁胶体 ④葡萄糖溶液
A.①② B.②③
C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
化学已渗透到人类生活的各个方面。下列说法错误的是
A.阿司匹林具有解热镇痛作用
B.可以用Si3N4、Al2O3制作高温结构陶瓷制品
C.禁止使用四乙基铅作汽油抗爆震剂,可减少汽车尾气污染
D.在入海口的钢铁闸门上装一定数量的铜块可防止闸门被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25 ℃时,几种物质的溶度积常数为AgCl~1.8×10-10;AgBr~7.7×10-13,AgI~8.51×10-16,下列有关说法错误的是( )
A.三种物质在常温下溶解度最小的是AgI
B.饱和AgCl溶液中,c(Ag+)≈1.34×10-5 mol/L
C.将氯化银置于饱和KI溶液中,固体慢慢会由白色转化为黄色
D.将浓度均为1×10-6 mol/L的AgNO3溶液、KBr溶液等体积混合会生成沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
溴酸银(AgBrO3)溶解度随温度变化的曲线如图所示,下列说法错误的是( )
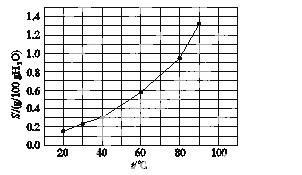
A.溴酸银的溶解是放热过程
B.温度升高时溴酸银溶解速率加快
C.60 ℃时溴酸银的Ksp约等于6×10-4
D.若硝酸钾中含有少量溴酸银,可用重结晶方法提纯
查看答案和解析>>
科目:高中化学 来源: 题型:
四氯化钛(TiCl4)是制取航天航空工业材料——钛合金的重要原料。由钛铁矿(主要成分是FeTiO3)制备TiCl4等产品的一种工艺流程示意图如下:

(1)往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性。该过程中有如下反应发生:
Fe+2Fe3+===3Fe2+
2TiO2+(无色)+Fe+4H+===2Ti3+(紫色)+Fe2++2H2O
Ti3+(紫色)+Fe3++H2O===TiO2+(无色)+Fe2++2H+
加入铁屑的作用是____________________________________________ ______________
______________
________________________________________________________________________。
(2)在②→③工艺过程中需要控制条件以形成TiO2·nH2O溶胶,该溶胶的分散质颗粒直径大小在________范围。
 (3)若把③中制得的固体TiO2·nH2O用酸清洗除去其中的杂质,还可制得钛白粉。已知25 ℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+Fe3++3H2O的平衡常数K=________。
(3)若把③中制得的固体TiO2·nH2O用酸清洗除去其中的杂质,还可制得钛白粉。已知25 ℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+Fe3++3H2O的平衡常数K=________。
(4)已知:TiO2(s)+2Cl2(g)===TiCl4(l)+O2(g)
ΔH=+140 kJ·mol-1
2C(s)+O2(g)===2CO(g) ΔH=-221 kJ·mol-1
写出④中TiO2和焦炭、氯气反应生成液态TiCl4和CO气体的热化学方程式:________。
(5)上述工艺具有成本低、可用低品位矿物为原料等优点。依据绿色化学理念,该工艺流程中存在的不足之处是__________________(只要求写出一项)。
(6)依据下表信息,要精制含少量SiCl4杂质的TiCl4,可采用________方法。
| TiCl4 | SiCl4 | |
| 熔点/℃ | -25.0 | -68.6 |
| 沸点/℃ | 136.4 | 57.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
溴酸银(AgBrO3)溶解度随温度变化曲线如图所示,下列说法错误的是( )

A.溴酸银的溶解时放热过程
B.温度升高时溴酸银溶解速度加快
C.60 ℃时溴酸银的Ksp约等于6×10-4
D.若硝酸钾中含有少量溴酸银,可用重结晶方法提纯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com