
 现有如下两个反应:①NaOH+HCl═NaCl+H2O;②2H2+O2═2H2O.
现有如下两个反应:①NaOH+HCl═NaCl+H2O;②2H2+O2═2H2O.分析 (1)酸碱中和反应和活泼金属与酸的反应都是放热反应;要构成原电池必须能自发的氧化还原反应;
(2)要构成原电池必须能自发的氧化还原反应;
(3)锌失电子为负极,铜是正极,正极上铜离子得电子生成Cu.
解答 解:(1)酸碱中和反应和活泼金属与酸的反应都是放热反应,所以两个反应都是放热反应;要构成原电池必须能自发的氧化还原反应,NaOH+HCl=NaCl+H2O是非氧化还原反应,而Fe+H2SO4=FeSO4+H2↑是氧化还原反应,
故答案为:放热;①不能,②能;
(2)反应①NaOH+HCl═NaCl+H2O是酸碱中和反应,属于复分解反应,不是氧化还原反应,不能设计为原电池;
故答案为:反应①不是氧化还原反应,不能设计为原电池;
(3)由图可知,锌失电子为负极,负极发生氧化反应,电极反应式为:Zn-2e-═Zn2+;铜是正极,发生还原反应,电极反应式为:Cu2++2e-═Cu.
故答案为:Zn-2e-═Zn2+;Cu2++2e-═Cu.
点评 本题考查原电池原理,侧重考查电极反应式书写、原电池原理等知识点,电解质溶液中阴阳离子移动方向是学习难点,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| 实验方案 |  | 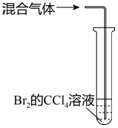 |  |  |
| 目的 | A.比较乙醇分子中羟基氢原子和水分子中氢原子的活泼性 | B.除去乙烯中的二氧化硫 | C.制银氨溶液 | D.证明碳酸酸性强于苯酚 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HF、HCl、HBr、HI的热稳定性依次减弱,酸性依次减弱 | |
| B. | 熔融状态下能导电的化合物一定含离子键;金属与非金属元素形成的化合物一定是离子化合物 | |
| C. | NCl3分子中所有的原子均为8电子稳定结构 | |
| D. | NaHSO4晶体中阴、阳离子的个数是1:2且熔化时破坏的是离子键和共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2的消耗速率与NO的生成速率相等 | |
| B. | 容器内气体的密度不随时间变化而变化 | |
| C. | NO2和O2的消耗速率之比为2:1 | |
| D. | 混合气体的质量不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 试验编号 | T/K | 大理石规格 | HNO3浓度mol/L | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | 实验①和②探究HNO3 浓度对该反应速率的影响; (II)实验①和____探究温度对该反应速率的影响; (III)实验①和____探究大理石规格(粗、细)对该反应速率的影响. |
| ② | 298 | 粗颗粒 | 1.00 | |
| ③ | 308 | 粗颗粒 | 2.00 | |
| ④ | 298 | 细颗粒 | 2.00 |

 此空删去.
此空删去.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间的转化关系如图所示(反应条件己略去).下列有关物质的推断正确的是( )
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间的转化关系如图所示(反应条件己略去).下列有关物质的推断正确的是( )| 甲 | 乙 | 丙 | 丁 | |
| A | N2 | NO | NO2 | O2 |
| B | CO32- | HCO3- | CO2 | H+ |
| C | Cl2 | FeCl3 | FeCl2 | Fe |
| D | Al3+ | Al(OH)3 | AlO2- | NH3•H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| SrSO4 | BaSO4 | SrCO3 | |
| Ksp | 3.2×10-7 | 1.1×10-10 | 1.6×10-10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与C60中普通碳原子的化学性质不同 | |
| B. | 与14N含的中子数相同 | |
| C. | 与12C为相同核素 | |
| D. | 与12C互为同位素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com