
【题目】某Na2CO3、NaAlO2的混合溶液中逐滴加入1molL1的盐酸,测得溶液中的CO32、HCO3、AlO2、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示。则下列说法正确的是( )(已知:H2CO3的电离平衡常数K1 = 4.3×107,K2 = 5.6×1011;Al(OH)3的酸式电离平衡常数K=6.3×1013)

A. a曲线表示的离子方程式为:AlO2+4H+ = Al3+ + 2H2O
B. M点时生成的CO2为0.05 mol
C. 原混合溶液中的CO32与AlO2的物质的量之比为1:2
D. V1:V2=1:4
【答案】D
【解析】A、根据H2CO3和Al(OH)3的电离平衡常数,得H+能力大小:AlO2->CO32->HCO3-,滴加盐酸发生:AlO2-+H++H2O=Al(OH)3↓,继续滴加盐酸发生CO32-+H+=HCO3-、HCO3-+H+=CO2↑+H2O、Al(OH)3+3H+=Al3++3H2O,因此a曲线表示的是AlO2-+H++H2O=Al(OH)3↓,故A错误;B、根据图像,M点是CO32-完全转化成HCO3-,即发生CO32-+H+=HCO3-,没有CO2产生,故B错误;C、根据A选项分析,a线发生AlO2-+H++H2O=Al(OH)3↓,AlO2-全部转化成Al(OH)3,消耗H+的物质的量50×10-3×1mol=0.05mol,则n(AlO2-)=0.05mol,b线发生CO32-+H+=HCO3-,CO32-全部转化成HCO3-,消耗H+的物质的量为(100-50)×10-3×1mol=0.05mol,则n(CO32-)=0.05mol,原溶液中CO32-和AlO2-的物质的量之比为0.05:0.05=1:1,故C错误;D、当加入V1mL盐酸时,溶液中n(HCO3-)=n(CO32-)=0.025mol,因此共消耗盐酸的体积为V1=(0.05+0.025)×1000/1mL=75mL,当盐酸体积为V2时,溶液中溶质为NaCl和AlCl3,根据元素守恒,因此n(HCl)=n(Na+)+3n(Al3+)=[0.05×2+0.05+3×0.05]mol=0.3mol,则V2=0.3×1000/1mL=300mL,因此V1:V2=75:300=1:4,故D正确。


科目:高中化学 来源: 题型:
【题目】处理含铬废水的方法较多
Ⅰ.某工业废水中主要含有Cr3+,同时还含有少量的Cu2+、Fe2+、Fe3+和Al3+等,且酸性较强。为回收利用,通常采用如下流程处理:

已知: Cr(OH)3―→NaCrO2―→Na2CrO4―→Na2Cr2O7
请回答:
(1)操作Ⅰ的名称为____________,上述操作Ⅰ、Ⅱ、Ⅲ相同,进行该实验操作所需要的主要玻璃仪器除烧杯、漏斗外,还有__________。
(2)滤渣Ⅰ的主要成分为________(写化学式),试剂乙的名称为__________。
(3)加入试剂甲的目的是____________________________________________________。
(4)废水处理流程中生成滤渣Ⅲ的离子方程式为________________________________。
Ⅱ.酸性条件下,六价铬主要以Cr2O![]() 形式存在。工业上用以下方法处理含Cr2O
形式存在。工业上用以下方法处理含Cr2O![]() 的废水:①往废水中加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,还原Cr2O
的废水:①往废水中加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,还原Cr2O![]() ;③经过一段时间,最后有Cr(OH)3和Fe(OH)3沉淀产生过滤回收沉淀,废水达到排放标准。
;③经过一段时间,最后有Cr(OH)3和Fe(OH)3沉淀产生过滤回收沉淀,废水达到排放标准。
(5) 在②步中,电解法除铬的原理是(写出涉及的主要电极反应式和离子方程式)_____________________________________________________________。
(6)已知某含Cr2O![]() 的酸性工业废水中铬元素的含量为104.5 mg·L-1,处理后铬元素最高允许排放浓度为0.5 mg·L-1。处理该废水1 000 m3并达到排放标准至少消耗铁的质量为________kg。
的酸性工业废水中铬元素的含量为104.5 mg·L-1,处理后铬元素最高允许排放浓度为0.5 mg·L-1。处理该废水1 000 m3并达到排放标准至少消耗铁的质量为________kg。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. CH(CH2CH3)3的名称是3-甲基戊烷
B. ![]() 和
和![]() 、
、![]() 和
和![]() 都属于同一种物质
都属于同一种物质
C. 乙醛和丙烯醛(![]() )不是同系物,与氢气充分反应后产物也不是同系物
)不是同系物,与氢气充分反应后产物也不是同系物
D. 向苯中加入酸性高锰酸钾溶液震荡后静置,观察到液体分层,且上、下层均无色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能将氯化铁、氯化铵和氯化钠三种溶液区别开的一种试剂是 ( )
A. KSCN溶液 B. BaCl2溶液
C. AgNO3溶液 D. NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组同学为了探究“在相同的温度和压强下、相同体积的任何气体都含有相同数目和分子”,他们设计了如下实验装置并记录相关实验数据。
实验装置:
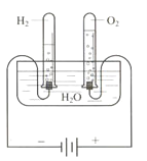
部分实验数据:
温度 | 压强 | 时间 | 水槽中H2O的质量 | H2体积 | O2体积 |
30℃ | 101 kPa | 0 | 300 g | 0 | 0 |
30℃ | 101 kPa | 4分钟 | 298.2 g | 1.243 L |
请回答下列问题:
(1)4分钟时H2、O2物质的量分别是 mol、 mol。
(2)该温度下,气体摩尔体积是 。
(3)假设电解H2O速率相同,2分钟时试管内收集到的H2的体积是 mL。
(4)根据以上实验得出如下结论,其中不正确的是 。
A. 气体摩尔体积与气体的温度相关
B. 在该实验条件下,3 mol O2的气体摩尔体积为74.58 L/mol
C. 同温、同压下,2 mol O2和2 mol CO和CO2混合气体的体积相同
D. 该实验条件下,O2的密度为1.287 g/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:

下列说法正确的是
A. 反应开始到10s,用Z表示的反应速率为0.158mol/(L·s)
B. 反应开始到10s,Y的转化率为79.0%
C. 反应开始到10s,X的物质的量浓度减少了0.79mol/L
D. 反应的化学方程式:X(g)+Y(g)![]() Z(g)
Z(g)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com