
分析 ${\;}_{1}^{1}{H}_{2}$、${\;}_{1}^{2}{H}_{2}$、${\;}_{1}^{3}{H}_{2}$的相对分子质量分别为2,4,6,依据m=nM计算解答;
依据阿伏伽德罗定律可知:相同条件下气体体积之比等于物质的量之比,计算相同条件下等质量的三种气体${\;}_{1}^{1}{H}_{2}$、${\;}_{1}^{2}{H}_{2}$、${\;}_{1}^{3}{H}_{2}$即可解答;
解答 解:${\;}_{1}^{1}{H}_{2}$、${\;}_{1}^{2}{H}_{2}$、${\;}_{1}^{3}{H}_{2}$的相对分子质量分别为2,4,6,
依据m=nM,则取1mol${\;}_{1}^{1}{H}_{2}$、${\;}_{1}^{2}{H}_{2}$、${\;}_{1}^{3}{H}_{2}$,质量分别为2g;4g;6g,质量之比为1:2:3;
依据n=$\frac{m}{M}$,相同条件下等质量的三种气体${\;}_{1}^{1}{H}_{2}$、${\;}_{1}^{2}{H}_{2}$、${\;}_{1}^{3}{H}_{2}$的物质的量之比为$\frac{1}{2}$:$\frac{1}{4}$:$\frac{1}{6}$=6:3:2;
故答案为:1:2:3;6:3:2;
点评 本题考查了有关物质的量计算,明确以物质的量为核心的有关计算公式,熟悉阿伏伽德罗定律是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
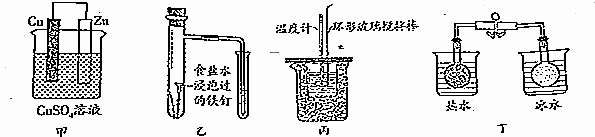
| A. | 图甲所示的实验:根据溶液颜色变化可比较Zn、Cu的金属活动性 | |
| B. | 图乙所示的实验:根据小试管中液面的变化判断铁钉发生析氢腐蚀 | |
| C. | 图丙所示的实验:根据温度计读数的变化用浓硫酸和Na0H反应测定中和热 | |
| D. | 图丁所示的实验:根据两烧瓶中气体颜色的变化判断2N02(g)?N20(g)是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4种 | B. | 6种 | C. | 8种 | D. | 10种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 | Cu | Zn | S |
| 1 | 10.3% | 5.0% | 1.2% |
| 2 | 11.5% | 4.9% | 1.8% |
| 3 | 12.4% | 10.3% | 0.9% |
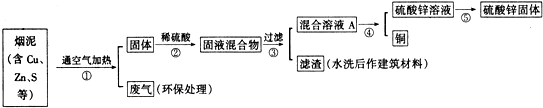
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.186 | 0.143 | 0.089 | 0.104 | 0.074 |
| 主要化合价 | +1 | +3 | +2 | +6、-2 | -2 |
| A. | B元素不能形成共价化合物 | |
| B. | 离子半径大小A+>D2- | |
| C. | A和E形成的化合物中只可能含离子键 | |
| D. | B和E的化合物不能溶于氨水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com