
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ⑤ | ||||||
| 3 | ② | ③ | ④ | ⑥ |
 ;
;分析 (1)由元素在周期表中的位置可知,①为Li、②为Na、③为Mg、④为Al、⑤为F、⑥为Cl;
(2)同周期自左而右元素金属性减弱;
(3)元素非金属性越强,对应氢化物越稳定;
(4)④的最高价氧化物对应的水化物为氢氧化铝;
(5)③为Mg,原子核外有12个电子,有3个电子层,各层电子数为2、8、2;
(6)镁与盐酸反应生成氯化镁与氢气;
(7)碳酸氢钠加热分解得到碳酸钠,用加热方法除去碳酸钠中含有碳酸氢钠杂质.
解答 解:(1)由元素在周期表中的位置可知,①为Li、②为Na、③为Mg、④为Al、⑤为F、⑥为Cl,故答案为:Mg;
(2)同周期自左而右元素金属性减弱,故金属性:Na>Mg>Al,故答案为:Na;
(3)同主族自上而下元素非金属性减弱,元素非金属性越强,对应氢化物越稳定,故氢化物稳定性:HF>HCl,故答案为:HF;
(4)④的最高价氧化物对应的水化物为Al(OH)3,故答案为:Al(OH)3;
(5)③为Mg,原子核外有12个电子,有3个电子层,各层电子数为2、8、2,原子结构示意图为 ,故答案为:
,故答案为: ;
;
(6)镁与盐酸反应生成氯化镁与氢气,反应离子方程式为:Mg+2H+=Mg2++H2↑,故答案为:Mg+2H+=Mg2++H2↑;
(7)碳酸氢钠加热分解得到碳酸钠,用加热方法除去碳酸钠中含有碳酸氢钠杂质,故答案为:加热.
点评 本题考查元素周期表与元素周期律的应用,比较基础,需要学生熟练掌握短周期元素,侧重对基础知识的巩固.


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验用品 | 溶液温度 | 中和热 | ||
| t1 | t2 | △H | ||
| ① | 50 mL0.55 mol•L-1NaOH溶液 | 20℃ | 23.3℃ | |
| 50 mL0.5 mol•L-1HCl溶液 | ||||
| ② | 50 mL0.55 mol•L-1NaOH溶液 | 20℃ | 23.5℃ | |
| 50 mL0.5 mol•L-1HCl溶液 | ||||
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 、醛基-CHO、羧基-COOH、-COOR酯基.
、醛基-CHO、羧基-COOH、-COOR酯基.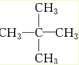 ,名称为2,2-二甲基丙烷.
,名称为2,2-二甲基丙烷.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水和碘化钾反应:Cl2+I-═Cl-+I2 | |
| B. | 碳酸钙与盐酸反应:CO32-+2H+═CO2↑+H2O | |
| C. | 氯气和水反应:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 40K和40Ca原子中的质子数和中子数都不相等 | |
| B. | H2和D2互为同位素 | |
| C. | 互为同位素的原子,它们的原子核内的中子数一定不相等 | |
| D. | 互为同位素的原子,它们原子核内的质子数一定相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com