
【题目】一种三室微生物燃料电池污水净化系统原理如图所示,图中有机废水中有机物可用C6H10O5 表示。有关说法正确的是 ( )

A.该装置为原电池,b为原电池的负极
B.a极区溶液的pH减小,中间室Na+移向左室
C. 当左室有4.48L(标准状况下)CO2生成时,右室产生的N2为0.8mol
D.a电极反应式:C6H10O5-24e-+7H2O===6CO2↑+24H+
【答案】D
【解析】
该原电池中,硝酸根离子得电子发生还原反应,则右边装置中电极b是正极,电极反应式为2NO3-+10e-+12H+=N2↑+6H2O,左边装置电极a是负极,负极上有机物失电子发生氧化反应,有机物在厌氧菌作用下生成二氧化碳,电极反应式为C6H10O5-24e-+7H2O═6CO2↑+24H+,据此分析解答。
A.该原电池中,硝酸根离子得电子发生还原反应,则右边装置中电极b是正极,故A选项错误。
B.a电极为负极,反应式为C6H10O5-24e-+7H2O═6CO2↑+24H+,生成氢离子故pH减小,电解质溶液中阳离子Na+移向正极右室,故B选项错误。
C.当左室有4.48L(标准状况下)CO2生成,即生成0.2mol CO2气体,根据反应式为C6H10O5-24e-+7H2O═6CO2↑+24H+转移0.2×24÷6=0.8mol电子,根据正极电极反应式为2NO3-+10e-+12H+=N2↑+6H2O可得生成N2为0.8×1÷10=0.08mol N2,故C选项错误。
D.a是负极,负极上有机物失电子发生氧化反应,有机物在厌氧菌作用下生成二氧化碳,电极反应式为C6H10O5-24e-+7H2O═6CO2↑+24H+,故D选项正确。
故答案选D。


 全能练考卷系列答案
全能练考卷系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,对可逆反应A(g)+2B(g)![]() 3C(g)的下列叙述中,能说明反应已达到平衡的是( )
3C(g)的下列叙述中,能说明反应已达到平衡的是( )
A.A物质与C物质的反应速率之比为1∶2
B.单位时间内消耗a mol A,同时消耗3a mol C
C.容器内的压强不再变化
D.混合气体的物质的量不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应4CO+2NO2![]() N2+4CO2在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
N2+4CO2在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
A.v(CO)=1.5mol·L-1·min-1B.v(NO2)=0.8mol·L-1·min-1
C.v(N2)=0.3mol·L-1·min-1D.v(CO2)=1.1mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国第二代身份证采用的是具有绿色环保性能的PETG新材料,PETG新材料可以回收再利用,而且对周边环境不构成任何污染.PETG的结构简式如下:
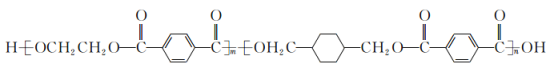
这种材料可采用下图所示的合成路线;
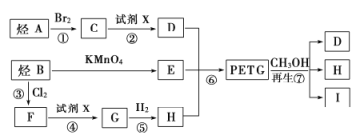
已知;(1)![]()
(2)![]() (R、
(R、![]() 、
、![]() 表示烃基)
表示烃基)
请回答下列问题:
(1)⑦的反应类型是_____________,试剂X为_____________.
(2)写出Ⅰ的结构简式:____________
(3)合成时应控制的单体的物质的量:![]() _____________(用m,n表示).
_____________(用m,n表示).
(4)写出反应②的化学方程式:____________________________________.
(5)与E的分子式相同,且满足下列条件的同分异构体有_____________种.
①能与![]() 溶液反应产生
溶液反应产生![]() ②能发生银镜反应 ③遇
②能发生银镜反应 ③遇![]() 溶液显紫色
溶液显紫色
(6)D和E在催化剂作用下可生产一种聚酯纤维——涤纶,请写出生产该物质的化学方程式:__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,CuS、MnS在水中的沉淀溶解平衡曲线如图所示,下列说法错误的是
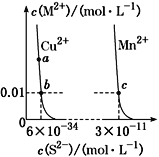
A. 在含有CuS和MnS固体的溶液中c(Cu2+)∶c(Mn2+)=1∶2×10-23
B. 向CuSO4溶液中加入MnS发生反应:
Cu2+(aq)+MnS(s)![]() CuS(s)+Mn2+(aq)
CuS(s)+Mn2+(aq)
C. a点对应的Ksp等于b点对应的Ksp
D. 该温度下,Ksp(CuS)小于Ksp(MnS)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是( )
①溴水中存在化学平衡:Br2+H2O![]() HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
②铁在潮湿的空气中易生锈
③二氧化四氧化二氮的平衡体系,压缩体积后颜色加深
④工业合成氨反应(放热)为加快反应速率,将温度升高到500℃左右
⑤钠与氯化钾共融制备钾:Na(l)+KCl(l)![]() K(g)+NaCl(l)
K(g)+NaCl(l)
A.①④⑤B.①②③C.②③④D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜锌原电池(如图)工作时,下列叙述错误的是( )
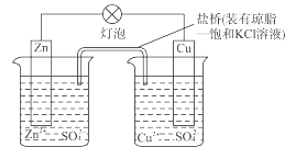
A. 正极反应为:Cu2++2e–= Cu
B. 电池反应为:Zn+Cu2+=Zn2+ +Cu
C. 在外电路中,电子从负极流向正极
D. 盐桥中的K+移向ZnSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,有关物质的电离平衡常数如下:

(1)电解质由强至弱顺序为___(用化学式表示,下同)。
(2)常温下,0.02mol·L-1的CH3COOH溶液的电离度约为___,体积为10 mL pH=2的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者___后者(填“>”、“<”或“=”)。
(3)下列离子CH3COO-、CO32-、HSO3-、SO32-在溶液中结合H+的能力由大到小的顺序为_____。
(4)NaHSO3溶液显酸性的原因_____(离子方程式配适当文字叙述),其溶液中离子浓度由大到小的关系是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物G是合成维生素类药物的中间体,其结构简式如图1所示,G的合成路线如图2所示:
其中A~F分别代表一种有机化合物,合成路线中部分产物及反应条件已略去
已知:-CHO+
请回答下列问题:
(1)G的分子式是__,G中官能团的名称是__;
(2)第①步反应的化学方程式是__;
(3)B的名称(系统命名)是__;
(4)第②~⑥步反应中属于取代反应的有__(填步骤编号);
(5)第④步反应的化学方程式是________;
(6)写出同时满足下列条件的E的所有同分异构体的结构简式__,①只含一种官能团;②链状结构且无﹣O﹣O﹣;③核磁共振氢谱只有2种峰。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com