
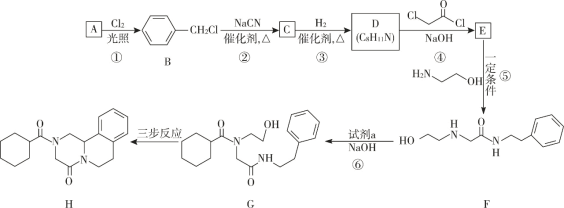
【题目】键线式是表达有机化合物结构的一种方式,如H2N—CH2—CH2—OH 用键线式可以表达为 ![]() 。吡喹酮(H)是一种治疗血吸虫病的药物,合成路线如下图所示:
。吡喹酮(H)是一种治疗血吸虫病的药物,合成路线如下图所示:
已知:I R-Cl+NaCN![]() R-CN+NaCl
R-CN+NaCl
ii 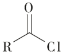 +R′—NH—R"+NaOH
+R′—NH—R"+NaOH![]()
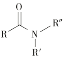 +NaCl+H2O(R、R′表示烃基,R"表示羟基或H)
+NaCl+H2O(R、R′表示烃基,R"表示羟基或H)
(1)A 属于芳香烃,其名称是____________ 。
(2)②的反应类型是_____________ 。
(3)B 的一种同分异构体,含苯环且核磁共振氢谱中出现三组峰,其结构简式为_____________ 。
(4)③中 1 mol C 理论上需要消耗 ___________mol H2 生成 D。
(5)④的化学方程式是_____________ 。
(6) 试剂 a 的结构简式是 ____________________。
(7) G→H 分为三步反应,J 中含有 3 个六元环,写出 I、J 的结构简式________________、__________________。
![]()
【答案】甲苯 取代反应 ![]() 2
2 ![]() +NaOH
+NaOH![]()
![]() +NaCl+H2O
+NaCl+H2O 
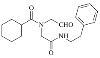
![]()
【解析】
根据A为芳香烃及B的结构得到A为甲苯,根据信息I得到B与NaCN发生取代反应生成C(![]() ),根据D的结构可以得出
),根据D的结构可以得出![]() 和氢气发生加成反应生成
和氢气发生加成反应生成![]() ,
,![]() 和
和![]() 反应生成
反应生成![]() ,
,![]() 和
和![]() 反应生成
反应生成![]() ,根据信息得出
,根据信息得出![]() 和
和![]() 反应生成
反应生成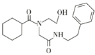 ,
, 发生催化氧化反应得到
发生催化氧化反应得到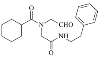 ,
, 发生加成反应生成
发生加成反应生成![]() ,
,![]() 发生脱水生成
发生脱水生成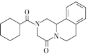 。
。
(1)A属于芳香烃,其名称是甲苯;故答案为:甲苯。
(2)根据信息I得到B与NaCN发生取代反应生成C(![]() );故答案为:取代反应。
);故答案为:取代反应。
(3)B的一种同分异构体,含苯环且核磁共振氢谱中出现三组峰,其结构简式为![]() ;故答案为:
;故答案为:![]() 。
。
(4)③![]() 含有—CN,根据D中的分子式得到1 mol
含有—CN,根据D中的分子式得到1 mol ![]() 理论上含有需要消耗 2mol H2 生成 D。
理论上含有需要消耗 2mol H2 生成 D。
(5)根据题中信息和分析得到④的化学方程式是![]() +NaOH
+NaOH![]()
![]() +NaCl+H2O;故答案为:
+NaCl+H2O;故答案为:![]() +NaOH
+NaOH![]()
![]() +NaCl+H2O。
+NaCl+H2O。
(6)根据反应前后结构式和信息得到试剂 a 的结构简式是![]() ;故答案为:
;故答案为:![]() 。
。
(7) 发生催化氧化反应得到
发生催化氧化反应得到 ,
, 发生加成反应生成
发生加成反应生成![]() ,
,![]() 发生脱水生成
发生脱水生成 ;故答案为:
;故答案为: ;
;![]() 。
。


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:
【题目】三氯化氮(NCl3)是一种消毒剂,可利用氯气与氯化铵溶液反应来制备。已知:三氯化氮的相关性质如下:
物理性质 | 化学性质 |
黄色油状液体,熔点为-40℃,沸点为 71℃,不溶于冷水、易溶于有机溶剂,密度为 1.65 gcm-3 | 95℃时爆炸,热水中发生水解 |
某小组同学选择下列装置(或仪器)设计实验制备三氯化氮并探究其性质:
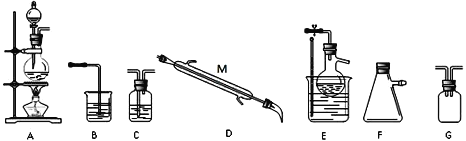
(1)NCl3的电子式为__________________;仪器 M 的名称是______________;
(2)如果气流的方向从左至右,装置连接顺序为A、G、_____________、B。(注明:F仪器使用单孔橡胶塞)
(3)C中试剂是_________________;B装置的作用是________________;
(4)写出E装置中发生反应的化学方程式_______________________________________
(5)当E装置的烧瓶中出现较多油状液体时停止反应。控制水浴加热温度为__________;
(6)已知三氯化氮不具有漂白性,三氯化氮与热水反应的化学方程式为NCl3+4H2O=NH3H2O+3HClO,请设计实验证明该水解反应的产物______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定.已知:Na2SO3(aq)+S(s)![]() Na2S2O3(aq),实验可知该反应较慢。工业上常利用含硫废水生产Na2S2O35H2O,实验室可用如图所示装置(略去部分夹持仪器)模拟生产过程。
Na2S2O3(aq),实验可知该反应较慢。工业上常利用含硫废水生产Na2S2O35H2O,实验室可用如图所示装置(略去部分夹持仪器)模拟生产过程。
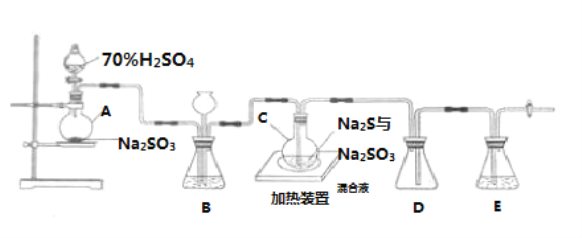
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若_______,则整个装置气密性良好。装置D的作用是______________________________________ 。
(2)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择___________。
a.蒸馏水 b .饱和Na2SO3溶液
c.饱和NaHSO3溶液 d . 饱和NaHCO3溶液
实验中,为使SO2缓慢进入烧瓶C,采用的操作是____________。烧瓶C中反应达到终点的现象是____________________。待C中反应完成后应立即关闭分液漏斗的旋塞,原因是_______________________。
(3)反应终止后,烧瓶C中的溶液经蒸发浓缩、冷却结晶即可析出Na2S2O35H2O,其中可能含有Na2SO3、Na2SO4等杂质,利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作、现象和结论:_______________________________________________。供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语或命名正确的是( )
A.含有10个中子的氧原子的符号:![]() B.乙烯的结构简式:CH2CH2
B.乙烯的结构简式:CH2CH2
C.S2的结构示意图:![]() D.NH4Cl的电子式:
D.NH4Cl的电子式:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阳离子交换膜法电解饱和食盐水具有综合能耗低、环境污染小等优点。生产流程如下图所示:
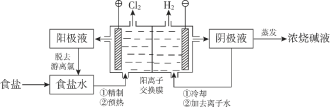
(1)电解饱和食盐水的化学方程式为________。
(2)电解结束后,能够脱去阳极液中游离氯的试剂或方法是________(填字母序号)。
a.Na2SO4b.Na2SO3
c.热空气吹出d.降低阳极区液面上方的气压
(3)食盐水中的I—若进入电解槽,可被电解产生的Cl2氧化为ICl,并进一步转化为IO3—。IO3—可继续被氧化为高碘酸根(IO4—),与Na+结合生成溶解度较小的NaIO4沉积于阳离子交换膜上,影响膜的寿命。
①从原子结构的角度解释ICl中碘元素的化合价为+1价的原因:________。
②NaIO3被氧化为NaIO4的化学方程式为________。
(4)在酸性条件下加入NaClO溶液,可将食盐水中的I-转化为I2,再进一步除去。通过测定体系的吸光度,可以检测不同pH下I2的生成量随时间的变化,如下图所示。已知:吸光度越高表明该体系中c(I2)越大。
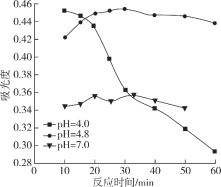
①结合化学用语解释10 min时不同pH体系吸光度不同的原因:________。
②pH=4.0时,体系的吸光度很快达到最大值,之后快速下降。吸光度快速下降的可能原因:________。
③研究表明食盐水中I-含量≤0.2 mgL-1时对离子交换膜影响可忽略。现将1m3含I-浓度为1.47 mgL-1 的食盐水进行处理,为达到使用标准,理论上至少需要0.05 molL-1 NaClO溶液________L。(已知NaClO的反应产物为NaCl,溶液体积变化忽略不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,炽热的铁与水蒸气在一个体积可变的密闭容器中进行反应:3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g),下列条件的改变对反应速率几乎无影响的是
Fe3O4(s)+4H2(g),下列条件的改变对反应速率几乎无影响的是
A. 把铁块换成铁粉 B. 将容器的体积压缩至原体积的一半
C. 压强不变,充入氮气使容器体积增大 D. 体积不变,充入氮气使容器压强增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应速率和限度的说法不正确的是( )
A. 实验室用H2O2分解制O2,加MnO2做催化剂后,反应速率明显加快
B. 在金属钠与足量水反应中,增加水的量能加快反应速率
C. 2SO2+O2![]() 2SO3反应中,SO2的转化率不能达到100%
2SO3反应中,SO2的转化率不能达到100%
D. 实验室用锌和盐酸反应制取氢气,用锌粉比锌粒反应要快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列各组物质属于同素异形体________;属于同位素是________;属于同一种物质是________;属于同系物是________。(写序号)
①红磷与白磷;②12C与14C;③S2与S8;④235U与238U;⑤干冰与二氧化碳;⑥CH4与CH3CH3;⑦ ![]() 与
与 ![]() ;⑧CH3CH=CH2和CH2=CH2。
;⑧CH3CH=CH2和CH2=CH2。
(2)已知A的产量可以用来衡量一个国家的石油化工发展水平,请写出工业上用A制备酒精的化学方程式________。
(3)在一定体积的 18 mol/L的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为 0.9 mol。则浓硫酸的实际体积________ (填“大于”“小于”或“等于”)100 mL。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如 KNO3溶液),则该反应的离子方程式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙均为1L的恒容密闭容器,向甲中充入1molCH4和1molCO2,乙中充入1molCH4和nmolCO2,在催化剂存在下发生反应:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g),测得CH4的平衡转化率随温度的变化如图所示。下列说法正确的是
2CO(g)+2H2(g),测得CH4的平衡转化率随温度的变化如图所示。下列说法正确的是
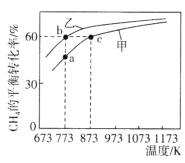
A.该反应的正反应是吸热反应
B.773K时,该反应的平衡常数小于12.96
C.H2的体积分数:![]()
D.873K时,向甲的平衡体系中再充入CO2、CH4各0.4mol,CO、H2各1.2mol,平衡不发生移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com