
【题目】营养平衡与人体健康:
(1)营养均衡有利于身体健康。秋葵是一种大众喜爱的食材,含有蛋白质、维生素A、维生素C、纤维素、阿拉伯果糖和丰富的铁、锌、钙等元素,其中:

①属于糖类的有:阿拉伯果糖、___。
②蛋白质在人体内水解的最终产物为___。
③人体缺乏某种微量元素会发生贫血,这种微量元素是___。
④属于水溶性维生素的是___,缺乏该维生素会引起___。
(2)如图为某品牌酱油标签的一部分。

①氨基酸态氮的含量是酱油质量的重要指标,这些氨基酸是由大豆中的主要营养物质___水解而来。
②配料清单中属于防腐剂的是___。
③小麦中的主要营养物质是___。
(3)了解一些用药常识,有利于自我保健。现有下列药物:碳酸镁、青霉素、阿司匹林、氢氧化铝。
①其中属于解热镇痛的药物是___;
②青霉素作用是___。
③药片常用淀粉作为黏合剂,淀粉水解最终产物是___。
④某胃药的主要成分是AlaMgb(OH)cCO3。常用于冶疗胃酸过多,写出其与胃酸反应的化学方程式:___。
【答案】纤维素 氨基酸 Fe 维生素C 坏血病 蛋白质 苯甲酸钠 淀粉 阿司匹林 消炎 葡萄糖 2AlaMgb(OH)cCO3+(6a+4b)HCl=2aAlCl3+2bMgCl2+(3a+2b+c)H2O+2CO2↑
【解析】
(1)①纤维素属于糖类;
②蛋白质在人体内水解的最终产物为氨基酸;
③人体缺乏铁元素会发生贫血;
④维生素C为水溶性维生素,缺乏维生素C会引起维生素C缺乏病,又称坏血病;
(2)①大豆中富含蛋白质,蛋白质水解生成氨基酸;
②苯甲酸钠是常用的食品防腐剂;
③小麦中的主要营养物质是淀粉;
(3)①阿司匹林属于解热镇痛的药物;
②青霉素作用是消炎;
③淀粉为多糖,水解的最终产物是葡萄糖;
④AlaMgb(OH)cCO3和盐酸反应生成AlCl3、MgCl2、H2O和CO2。
(1)①属于糖类的,除了阿拉伯果糖,还有纤维素;
故答案为:纤维素;
②蛋白质在人体内水解的最终产物为氨基酸;
故答案为:氨基酸;
③人体缺乏Fe元素会发生贫血;
故答案为:Fe;
④维生素C为水溶性维生素,维生素A为脂溶性维生素;缺乏维生素C会引起维生素C缺乏病,又称坏血病;
故答案为:维生素C;坏血病;
(2)①大豆中富含蛋白质,蛋白质水解生成氨基酸;
故答案为:蛋白质;
②苯甲酸钠是常用的食品防腐剂;
故答案为:苯甲酸钠;
③小麦中的主要营养物质是淀粉;
故答案为:淀粉;
(3)了解一些用药常识,有利于自我保健。现有下列药物:碳酸镁、青霉素、阿司匹林、氢氧化铝。
①阿司匹林属于解热镇痛的药物;
故答案为:阿司匹林;
②青霉素作用是消炎;
故答案为:消炎;
③淀粉为多糖,水解的最终产物是葡萄糖;
故答案为:葡萄糖;
④AlaMgb(OH)cCO3是碱式碳酸盐,故能和盐酸反应生成AlCl3、MgCl2、H2O和CO2,化学方程式为2AlaMgb(OH)cCO3+(6a+4b)HCl=2aAlCl3+2bMgCl2+(3a+2b+c)H2O+2CO2↑;
故答案为:2AlaMgb(OH)cCO3+(6a+4b)HCl=2aAlCl3+2bMgCl2+(3a+2b+c)H2O+2CO2↑。


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:
【题目】某学习小组同学为探究同周期元素性质的递变规律,设计了如下实验。
(1)将等质量的钠、镁、铝分别投入到足量的相同浓度的盐酸中,试预测实验结果:上述金属中___(填化学式,下同)与盐酸反应最剧烈,___与盐酸反应生成的气体最多。
(2)向Na2S溶液中通入氯气出现淡黄色浑浊现象,可证明S、Cl元素非金属性强弱顺序为___,反应的离子方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学原理被广泛地应用于生产、生活的许多方面。
I.制备氯气
工业中用电解饱和食盐水的方法制备氯气,其原理如下图所示。
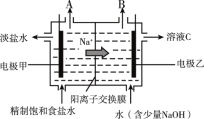
(1)此过程中能量转化形式为_____转化为_____(填“化学能”或“电能”)
(2)电极乙为_____(填“阴极”或“阳极”),A 口生成的气体是_____
(3)电解饱和食盐水的离子方程式是 _____
(4)下列有关氯气的说法中正确的是_____
a.实验室常用排饱和食盐水法收集
b.可使碘化钾溶液变蓝
c.转化为 NaClO、ClO2 等含氯化合物可用于杀菌消毒
II.金属防护
某小组同学为探究电极对金属腐蚀与防护的影响,设计如下实验:将饱和食盐水与琼脂(凝固剂,不参与反应)的混合液置于两个培养皿中,向其中滴入少量酚酞溶液和K3Fe(CN)6溶液,混合均匀。分别将包裹锌片和铜片的铁钉放入两个培养皿中,观察现象如下。

(5)被腐蚀的是包裹_____的铁钉(填“锌片”或“铜片”)
(6)结合电极反应式解释 i 中现象产生的原因_____
(7)结合以上实验,请对铁制零件的使用提出建议_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】解释下列事实所用的方程式不正确的是( )
A.碳酸氢钠在水溶液中的电离:NaHCO3=Na++HCO![]()
B.硫酸酸化的KI淀粉溶液久置后变蓝:4I-+O2 + 4H+ = 2I2+2H2O
C.用热的纯碱溶液清洗油污:CO![]() + 2H2OH2CO3 + 2OH-
+ 2H2OH2CO3 + 2OH-
D.用Na2CO3溶液处理锅炉水垢中的硫酸钙:CO![]() + CaSO4 =CaCO3 + SO
+ CaSO4 =CaCO3 + SO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2018年5月美国研究人员成功实现在常温常压下用氮气和水生产氨,原理如下图所示:
下列说法正确的是( )
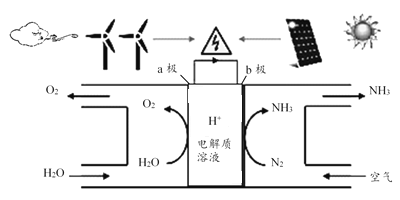
A. 图中能量转化方式只有2种
B. H+向a极区移动
C. b极发生的电极反应为:N2+6H++6e-=2NH3
D. a极上每产生22.4LO2流过电极的电子数一定为4×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )

A.原子半径:W > Z > Y > X
B.最高价氧化物对应水化物的酸性:Z > W
C.4种元素的单质中Z单质的熔、沸点最低
D.W单质能与水反应生成一种具有漂白性的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活、社会密切相关,请根据学过化学知识解答下列问题
(1)由下列物质冶炼相应金属时采用电解法的是___________。
a.Cu2S b.NaCl c.Fe2O3 d.HgS
(2) 银针验毒”在我国有上千年历史,银针主要用于检验是否有含硫元素的有毒物质。其反应原理之一为:4Ag+2H2S+O2=2Ag2S+2H2O。当银针变色后,将其置于盛有食盐水的铝制容器中一段时间后便可复原。原理是形成了原电池,该原电池的负极反应物为:______。
(3)某同学设计一个燃料电池(如下图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。

①通入甲烷的电极为________(填“正极”或“负极”),该电极反应式为___________。
②乙装置工作一段时间后,结合化学用语解释铁电极附近滴入酚酞变红的原因:____________。
③如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将________(填“增大”“减小”或“不变”)。精铜电极上的电极反应式为_________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列用于解释事实的方程式书写不正确的是
A.0.1mol/L氨水的pH约为11.1:NH3·H2O![]() NH4++OH-
NH4++OH-
B.用明矾 [KAl(SO4)2·12H2O]作净水剂:Al3++3H2O![]() Al(OH)3(胶体)+3H+
Al(OH)3(胶体)+3H+
C.用饱和Na2CO3溶液处理水垢中的CaSO4(微溶):Ca2++CO32-=CaCO3↓
D.向K2Cr2O7溶液中滴加少量浓H2SO4,溶液橙色加深:![]() (橙色)+H2O
(橙色)+H2O![]() 2CrO42-(黄色)+2H+
2CrO42-(黄色)+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是在实验室进行氨气快速制备与性质实验的组合装置,部分固定装置未画出。
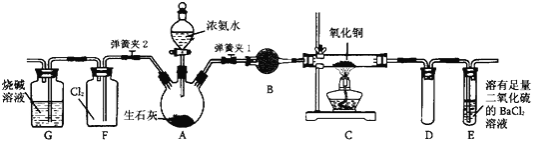
(1)在组装好装置后,若要检验A~E装置的气密性,其操作是首先____,然后微热A,观察到E中有气泡冒出,移开酒精灯或松开双手,E中导管有水柱形成,说明装置气密性良好。
(2)装置B中盛放的试剂是________。
(3)点燃C处酒精灯,关闭弹簧夹2,打开弹簧夹l,从分液漏斗放出浓氨水至浸没烧瓶中固体后关闭分液漏斗,稍候片刻,装置C中黑色固体逐渐变红,装置E中溶液里出现大量气泡,同时还可能产生的现象是________;从E中逸出液面的气体可以直接排入空气,请写出在C中发生反应的化学方程式:________。
(4)当C中固体全部变红色后,关闭弹簧夹1,慢慢移开酒精灯,待冷却后,称量C中固体质量,若反应前固体质量为16 g,反应后称重固体质量减少2.4 g,通过计算确定该固体产物的成分是________(用化学式表示)。
(5)在关闭弹簧夹1后,打开弹簧夹2,残余气体进入F中,很快发现装置F中产生白烟,同时发现G中溶液迅速倒吸流入F中。请写出产生白烟的化学方程式:________,迅速产生倒吸的原因是________。
(6)为了汪明一水合氨是弱碱,甲、乙两同学分别设计以下实验进行探究。
①甲同学用pH试纸测得室温下0.l mol/L氨水pH为10,则认定一水合氨是弱电解质,理由是________。
②乙同学取出10 mL 0.1 mol/L氨水,滴入2滴酚酞试液,显粉红色,再加入NH4Cl晶体少量,观察到的现象是________,则证明一水台氨是弱电解质。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com