
【题目】根据所学知识完成题目:
(1)某课外活动小组同学用图1装置进行实验,试回答下列问题:
①若开始时开关K与a连接,则铁发生电化学腐蚀中的腐蚀.请写出正极反应式: .
②若开始时开关K与b连接时,两极均有气体产生,则N端是电源的极(填正或负),则总反应的离子方程式为 .
(2)该小组同学设想,用如图2所示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧化钠. ①制得的氢氧化钠溶液从出口(填“A”、“B”、“C”或“D”)导出.通过阴离子交换膜的离子数(填“>”、“<”或“=”)通过阳离子交换膜的离子数.
②通电开始后,阴极附近溶液pH会增大,请简述原因: .
【答案】
(1)吸氧;O2+4e﹣+2H2O=4OH﹣;负;2Cl﹣+2H2O ![]() 2OH﹣+H2↑+Cl2↑
2OH﹣+H2↑+Cl2↑
(2)D;<;H+在阴极放电,水的电离平衡正向移动,溶液中OH﹣浓度增大,pH增大(合理即可)
【解析】解:(1)①开关K与a连接,为原电池,NaCl溶液为中性,发生吸氧腐蚀,正极上氧气得电子发生还原反应,电极反应式为O2+4e﹣+2H2O=4OH﹣ , 所以答案是:吸氧;O2+4e﹣+2H2O=4OH﹣;②K与b连接,为电解池,若开始时开关K与b连接时,两极均有气体产生,则Fe作阴极,石墨作阳极,氯离子、氢离子放电,则N为电源负极,电解的总离子反应为2Cl﹣+2H2O ![]() 2OH﹣+H2↑+Cl2↑,所以答案是:2Cl﹣+2H2O
2OH﹣+H2↑+Cl2↑,所以答案是:2Cl﹣+2H2O ![]() 2OH﹣+H2↑+Cl2↑;(2)①阴极上氢离子放电,则NaOH在阴极生成,由图可知,D在阴极附近,制得的氢氧化钠溶液从D出口导出;阳极氢氧根离子放电,因此硫酸根离子向阳极移动,阴极氢离子放电,因此钠离子向阴极移动,所以通过相同电量时,通过阴离子交换膜的离子数小于通过阳离子交换膜的离子数,所以答案是:D;<;②水电离出的氢离子在阴极放电,而氢氧根离子不放电,促进水的电离,导致溶液中氢氧根离子浓度增大,溶液的pH增大, 所以答案是:H+在阴极放电,水的电离平衡正向移动,溶液中OH﹣浓度增大,pH增大(合理即可).
2OH﹣+H2↑+Cl2↑;(2)①阴极上氢离子放电,则NaOH在阴极生成,由图可知,D在阴极附近,制得的氢氧化钠溶液从D出口导出;阳极氢氧根离子放电,因此硫酸根离子向阳极移动,阴极氢离子放电,因此钠离子向阴极移动,所以通过相同电量时,通过阴离子交换膜的离子数小于通过阳离子交换膜的离子数,所以答案是:D;<;②水电离出的氢离子在阴极放电,而氢氧根离子不放电,促进水的电离,导致溶液中氢氧根离子浓度增大,溶液的pH增大, 所以答案是:H+在阴极放电,水的电离平衡正向移动,溶液中OH﹣浓度增大,pH增大(合理即可).


科目:高中化学 来源: 题型:
【题目】下列变化中,由加成反应引起的是
A.乙烯通入酸性高锰酸钾溶液中,高锰酸钾溶液褪色
B.甲烷与氯气混合后,光照黄绿色消失
C.在催化剂存在下,乙烯与水反应生成乙醇
D.丙烯通入溴水中,溴水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mg﹣H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液(加入一定量酸),示意图如图.该电池工作时,下列说法正确的是( ) 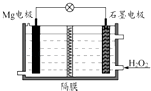
A.电池工作时,石墨周围海水的pH减少
B.电池工作时,溶液中的H+向负极移动
C.电池总反应为Mg+H2O2+2H+═Mg2++2H2O
D.Mg电极是该电池的正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备H2的一种重要方法是:CO(g)+H2O(g)CO2 (g)+H2(g)△H=QkJ/mol.已知该反应的平衡常数K与温度T的关系如图所示.若在一固定容积的密闭容器中,850℃时发生上述反应,测得容器内各物质的浓度 (mol/L)随时间的变化关系如表:已知:850℃时该反应的化学平衡常数K=1.0,请回答下列问题:
时间/min | CO(g) | H2O(g) | CO2(g) | H2(g) |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | c1 | c2 | c3 | c4 |
4 | c1 | c2 | c3 | c4 |

(1)Q0(填“>”、“=”或“<”).
(2)若在850℃时向反应容器中充人H2O(g),K值(填“增大”、“减小”或“不变”).
(3)上表中 c2为mol/L,CO(g)的转化率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据图1中氮元素及其化合物的转化关系,回答问题:

(1)实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为____________________。
(2)若要收集一瓶氨气,请将下列装置补充完整,在图2虚框内画出连接图。____________
(3)下列试剂可用于干燥NH3的是________________________________。
A.浓硫酸 B.碱石灰 C.CuSO4固体 D.P2O5
(4)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO化学方程式为________________________________;
②NO→NO2实验现象是________________________________;
③将32.64g铜与l40mL一定浓度的HNO3反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L。则其中NO、NO2的物质的量比为____________________。
(5)图1中在标准状况下将NO2、NO、O2混合并充满容器,将该容器倒置于水中,气体完全溶解,无气体剩余,若产物也不扩散,则所得溶液的物质的量浓度M,其数值大小范围为___________
A.0<M<l/22.4 B. 1/39.2<M<1/22.4 C.1/39.2<M<1/28 D.1/28<M<1/22.4
(6)图1中X转化为HNO3的化学方程式为:________________________________。
(7)若要将NH3→N2,从原理上看,下列试剂可行的是_______________。
A.O2 B.Na C.NH4Cl D. NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2(T2>T1)时,Y的体积分数(或Y的物质的量分数)与时间的关系如图2所示。则下列结论正确的是( )
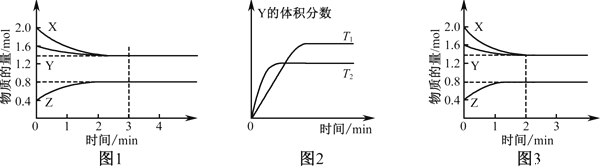
A. 容器中发生的反应可表示为:4X(g)+Y(g)![]() 2Z(g)
2Z(g)
B. 反应进行的前3min内,用X表示的反应速率v(X)=0.3mol/(L·min)
C. 升高温度,反应的化学平衡常数K增大
D. 若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
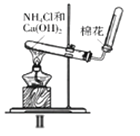
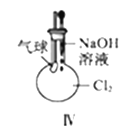
【题目】下列实验装置及说法正确的是( )
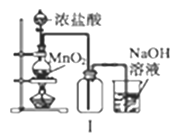
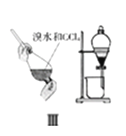
A. Ⅰ图中:实验室制备氯气,若MnO2过量,则浓盐酸可被全部消耗
B. Ⅱ图中:实验室制备氨气,棉花的作用是用来减小空气对流
C. Ⅲ图中:利用CCl4萃取溴,上层为CCl4层
D. Ⅳ图中:若气球干瘪,证明Cl2可与NaOH反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com