
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是( )
A.分子数为NA的CO和C2H4混合气体的体积约为22.4 L
B.标准状况下,4.48 L重水(D2O)中含有的中子数为2NA
C.用MnO2与浓盐酸制取Cl2时,每生成0.5mol Cl2则转移电子数为NA
D.0.1 L 3.0 mol?L﹣1的NH4NO3溶液中含有NH ![]() 的数目为0.3NA
的数目为0.3NA
科目:高中化学 来源: 题型:
【题目】下列关于氦原子电子云图的说法正确的是( )
A.通常用小黑点来表示电子的多少,黑点密度大,电子数目大
B.黑点密度大小,表示单位体积内电子出现的机会多少
C.通常用小黑点来表示电子绕核作高速圆周运动
D.电子云图是对运动无规律性的描述
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关“油”的说法正确的是( )
A.油脂包括矿物油、植物油与动物油
B.油脂的氢化与油脂的皂化都属于加成反应
C.植物油能使碘酒褪色
D.油脂属于高分子化合物,可以发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向18.4g铁和铜组成的合金中加入过量的硝酸溶液,合金完全溶解,同时生成NO2、NO混合气体,再向所得溶液中加入足量的NaOH溶液,生成30.3g沉淀.另取等质量的合金,使其与一定量的氯气恰好完全反应,则氯气的体积在标准状况下为( )
A.7.84L
B.6.72L
C.4.48L
D.无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2CO3、MaHCO3及xNa2CO3·yH2O(过碳酸的)在工农业生产上用途非常广泛。
(1)0.1mol/LNa2CO3溶液加水稀释时,溶液的pH____ (填“增大”、“减小”或“不变”)。
(2)25℃时,H2CO3的电离常数Ka1=5×10-7,Ka=5×10-11,NH3·H2O的电离常数Kb=1.8×10-5,计算下列平衡常数。
①NaHCO3水解反应HCO3-+H2O![]() H2CO3+OH-的平衡常数为K= ________ 。(填数值)
H2CO3+OH-的平衡常数为K= ________ 。(填数值)
②反应HCO3-+NH3·H2O![]() CO32-+NH4++H2O的平衡常数为K=_________。 (填数值)
CO32-+NH4++H2O的平衡常数为K=_________。 (填数值)
(3)一种测定xNa2CO3·yH2O2中y/x值的方法如下:

①滴定CO32-时,终点溶液颜色变化是______。
②滴定H2O2时,MnO4-被还原为Mn2+,反应的离子方程式为_______。
③若消耗盐酸25.00mL,消耗KMnO4溶液19.00mL。y/x的值(列出计算过程)__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘化钡(BaI22H2O)是一种白色粉末,常用于制取其他含碘化合物.一种制备流程如图1: 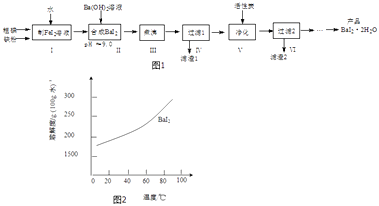
(1)步骤Ⅰ制FeI2溶液时,提高反应速率的可行措施有(填序号).
a.铁粉和碘粉用球磨机磨成细粉
b.增大n(铁粉):n(碘)的配料比
c.适当升高反应温度和搅拌速度
d.向反应器中加水至I2全部溶解
(2)步骤Ⅱ发生反应的化学方程式为;用pH试纸测定溶液pH的方法是
(3)步骤Ⅲ小心“煮沸”约20分钟,可使Fe(OH)2颗粒长大,其目的是;步骤V加入活性炭的目的是 .
(4)从过滤2所得滤液中获得BaI22H2O(溶解度曲线如图2所示)的方法是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.摩尔是表示物质的数量单位
B.1 mol氢的质量是2 g
C.O2的摩尔质量是32 g
D.每摩尔物质都含有阿伏加德罗常数个指定微粒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,正确的是
A. 含金属元素的离子一定都是阳离子
B. 在氧化还原反应中,非金属单质一定是氧化剂
C. 某元素从化合态变为游离态时,该元素一定被还原
D. 金属阳离子被还原不一定得到金属单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定的条件下,下列选项所示的物质间转化均能实现的是( )
A.NH3 ![]() NO
NO ![]() NaNO2
NaNO2
B.Fe2O3 ![]() Fe
Fe ![]() FeCl3
FeCl3
C.SiO2 ![]() H2SiO3(aq)
H2SiO3(aq) ![]() Na2SiO3
Na2SiO3
D.CuCl2(aq) ![]() Cu(OH)2
Cu(OH)2 ![]() Cu2O
Cu2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com