
分析 (1)根据物质的性质和质量守恒定律书写化学方程式;
(2)NH4Fe(SO4)2易水解,故需加入一定量的稀硫酸抑制水解;配制一定物质的量浓度的溶液,还需要容量瓶和胶头滴管;溶液中生成TiO2•xH2O沉淀,固体具有较强的吸附能力,会吸附溶液中的Cl-离子,可通过检验Cl-离子的方法检验沉淀是否被洗净;
(3)因为是用KSCN作指示剂,终点时NH4Fe(SO4)2不再反应,生成血红色的Fe(SCN)3;
(4)根据得失电子守恒,有:1Ti3+~1Fe3+,故n(Fe3+)=n(Ti3+)=n(TiO2)=cV×10-3mol,计算其质量分数.
解答 解:(1)设TiCl4的系数为1,根据元素守恒,TiO2•xH2O的系数为1,HCl的系数为4;再根据O元素守恒,可知H2O的系数为(2+x),反应的化学方程式为:TiCl4+(x+2)H2O?TiO2•xH2O↓+4HCl;
故答案为:TiCl4+(x+2)H2O?TiO2•xH2O↓+4HCl;
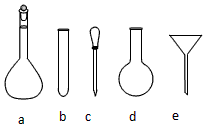
(2)NH4Fe(SO4)2易水解,故需加入一定量的稀硫酸抑制水解;配制一定物质的量浓度的溶液,还需要容量瓶和胶头滴管,则还需要ac,溶液中生成TiO2•xH2O沉淀,固体具有较强的吸附能力,会吸附溶液中的Cl-离子,可通过检验Cl-离子的方法检验沉淀是否被洗净,检验沉淀是否洗净的方法是,取少量洗涤液,检验溶液中溶解的离子是否还存在,
故答案为:抑制NH4Fe(SO4)2水解;ac;取少量最后一次水洗液,滴加AgNO3溶液,不产生白色沉淀,说明Cl-已除净;
(3)Fe3+与Ti3+反应,被还原为Fe2+,加入KSCN不显红色,当达到滴定终点时,再加入NH4Fe(SO4)2,溶液中Fe3+过量,会变成红色半分钟内不变,
故答案为:溶液变为红色且半分钟内不变;
(4)根据得失电子守恒,有:Ti3+~Fe3+,故n(Fe3+)=n(Ti3+)=n(TiO2)=cV×10-3mol,其质量分数为:$\frac{cV×1{0}^{-3}mol×Mg/mol}{Wg}$×100%=$\frac{cVM}{10W}%$,
故答案为:$\frac{cVM}{10W}%$.
点评 本题考查物质的制备、检验和滴定方法,题目难度中等,注意掌握化学基本实验基本操作方法,明确中和滴定操作方法及误差分析方法,试题侧重考查学生的分析、理解能力及化学实验、化学计算能力.


 应用题作业本系列答案
应用题作业本系列答案 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 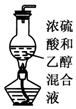 实验室制乙烯 | |
| B. | 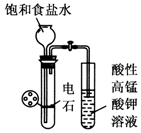 实验室制乙炔并验证乙炔能发生氧化反应 | |
| C. | 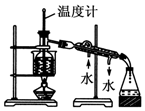 实验室中分馏石油 | |
| D. | 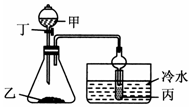 若甲为硫酸,乙为贝壳粉,丙为苯酚钠溶液,验证硫酸、碳酸、苯酚酸性的强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把溴水滴加到淀粉KI溶液中 | |
| B. | 把Cl2通入FeCl2溶液中 | |
| C. | 把绿豆大的钾投入少量水中 | |
| D. | 把一段打磨过的镁带放入少量冷水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
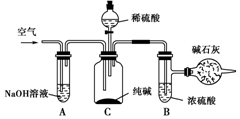 工业纯碱中常含有NaCl、Na2SO4等杂质,可用如图所示的装置测定工业纯碱中有效成分的含量.
工业纯碱中常含有NaCl、Na2SO4等杂质,可用如图所示的装置测定工业纯碱中有效成分的含量.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
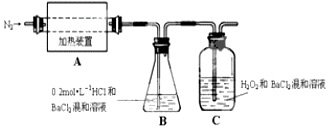
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
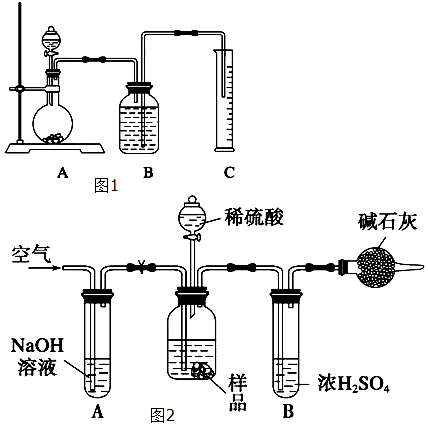
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 | B. | 2 | C. | 3 | D. | 不能确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com