

用FeCl3酸性溶液脱除H2S后的废液,通过控制电压电解得以再生。某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1mol/L的FeCl2溶液,研究废液再生机理。记录如下(a、b、c代表电压数值):
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| I | x≥a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| II | a>x≥b | 电极附近出现黄色,无气泡产生 | 有Fe3+、无Cl2 |
| III | b>x>0 | 无明显变化 | 无Fe3+、无Cl2 |
(1)用KSCN检验出Fe3+的现象是_______________________。
(2)I中,Fe3+产生的原因可能是Cl—在阳极放电,生成的Cl2将Fe2+氧化。写出有关反应:
____________________________________________________。
(3)由II推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有_________性。
(4)II中虽未检验出Cl2,但Cl—在阳极是否放电仍需进一步验证。电解pH=1的NaCl溶液做对照实验,记录如下:
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| IV | a>x≥c | 无明显变化 | 有Cl2 |
| V | c>x≥b | 无明显变化 | 无Cl2 |
①NaCl的浓度是_________mol/L
②IV中检测Cl2的实验方法______________________________________________。
③与II对比,得出的结论(写出两点):_____________________________________________。
(5)能量之间可以相互转化:电解食盐水制备Cl2是将电能转化为化学能,而原电池可将
化学能转化为电能。设计两种类型的原电池,探究其能量转化效率。
限选材料:ZnSO4(aq),FeSO4(aq),CuSO4(aq);铜片,铁片,锌片和导线。
完成原电池的装置示意图(见图15),并作相应标注。
要求:在同一烧杯中,电极与溶液含相同的金属元素。
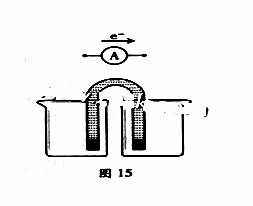
铜片为电极之一,CuSO4(aq)为电解质溶液,只在一个烧杯中组装原电池乙,工作一段时间后,可观察到负极 。
根据牺牲阳极的阴极保护法原理,为减缓电解质溶液中铁片的腐蚀,在(5)的材料中应选 作阳极
科目:高中化学 来源: 题型:
在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g)⇌zC(g)平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.20mol/L.下列有关判断正确的是( )
|
| A. | x+y>z | B. | 平衡向逆反应方向移动 |
|
| C. | B的转化率降低 | D. | C的体积分数升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是
A.钠与水反应:Na+2H2O=Na++2OH-+H2↑
B.硅酸钠溶液与醋酸溶液混合: +
+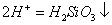
C.0.01mol/LNH4Al(SO4)2溶液与0.02mol/LBa(OH)2溶液等体积混合:
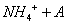 1
1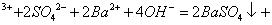 A1
A1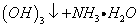
D.向次氯酸钙溶液通入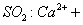
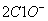 +
+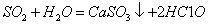
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解下列物质的溶液,一段时间后,再加入一定质量的另一种物质(括号内),溶液能与原来溶液完全相同的是( )
A.CuCl2[CuO] B.NaOH[Na2O] C.NaCl[HCl] D.CuSO4[Cu(OH)2]
查看答案和解析>>
科目:高中化学 来源: 题型:
在体积恒定的密闭容器中发生反应N2O4(g)  2NO2(g);ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
2NO2(g);ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
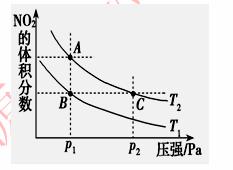
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A点深,C点浅
C.由状态B到状态A,可以用升温的方法
D.A、C两点气体的平均相对分子质量:A>C
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
①1mol氧元素 ②0.25mol氯离子 ③0.5mol 氢分子
④氢氧化钠的摩尔质量是40g/mol
⑤0.1mol水分子中含有NA个质子和NA个电子
⑥0.25mol 氨气在标准状况下体积约为5.6升。
A. 全部正确 B.②③④⑤⑥ C.①②③④⑥ D.①③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
下列应用或事实与胶体的性质没有关系的是( )
A.在河流入海口处易形成三角州 B.用石膏或盐卤点制豆腐
C.尿毒症患者做“血液透析”
D.在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)写出下列化学反应的离子方程式
①氢氧化钡溶液和硫酸溶液反应
②碳酸钙和足量稀盐酸反应
(2)根据下列离子方程式,各写一个符合条件的化学方程式
①Zn+2H+==Zn2++H2↑
②HCO3-+ H+==CO2↑+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
NA代表阿伏加德罗常数,下列说法不正确的是 ( )
A.含有NA个氦原子的氦气在标准状况下的体积约为11.2 L
B.25℃ 1.01×105 Pa,64 g SO2中含有的原子数为3NA
C.0℃ 101千帕,11.2L氮气所含的原子数目为NA
D.17g氨气所含电子数目为10NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com