
已知下列三个热化学方程式
①H2(g)+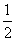 O2(g)===H2O(g) ΔH1=-241.8 kJ·mol-1
O2(g)===H2O(g) ΔH1=-241.8 kJ·mol-1
②C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
③C(s)+H2O(g)===CO(g)+H2(g) ΔH=131 kJ·mol-1
写出碳燃烧生成CO和CO燃烧的热化学方程式。
科目:高中化学 来源: 题型:
(1)将 (某一元酸)溶液与
(某一元酸)溶液与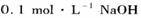 溶液等体积混合,测得混合溶液中
溶液等体积混合,测得混合溶液中 ,则此溶液中
,则此溶液中 ;
; 此溶液中由水电离出的
此溶液中由水电离出的
 溶液中由水电离出的
溶液中由水电离出的 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(2)将等体积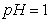 的盐酸和醋酸,加入适量水,
的盐酸和醋酸,加入适量水, 都升高了1,则加水后溶液体积V(醋酸)____V(盐酸)(填“>”、“<”或“=”)。
都升高了1,则加水后溶液体积V(醋酸)____V(盐酸)(填“>”、“<”或“=”)。
(3)常温下,某酸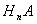 (A为酸根)与某碱
(A为酸根)与某碱 溶液恰好完全反应生成正盐,该溶液
溶液恰好完全反应生成正盐,该溶液 。写出该正盐的化学式____,该盐中____离子一定能水解,其水解离子方程式为_______。
。写出该正盐的化学式____,该盐中____离子一定能水解,其水解离子方程式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中既是氧化还原反应,又是吸热反应的是( )
A.铝与稀盐酸反应
B.灼热的炭与二氧化碳反应
C.甲烷在空气中燃烧
D.Ba(OH)2·8H2O与NH4Cl反应
查看答案和解析>>
科目:高中化学 来源: 题型:
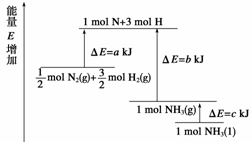
化学反应N2+3H2
 2NH3的能量变化如下图所示,该反应的热化学方程式是( )
2NH3的能量变化如下图所示,该反应的热化学方程式是( )
A.N2(g)+3H2(g)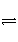
 2NH3(l) ΔH=2(a-b-c) kJ·mol-1
2NH3(l) ΔH=2(a-b-c) kJ·mol-1
B.N2(g)+3H2(g)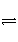
 2NH3(g) ΔH=2(b-a) kJ·mol-1
2NH3(g) ΔH=2(b-a) kJ·mol-1
C.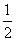 N2(g)+
N2(g)+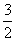 H2(g)
H2(g)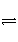
 NH3(l) ΔH=(b+c-a) kJ·mol-1
NH3(l) ΔH=(b+c-a) kJ·mol-1
D.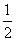 N2(g)+
N2(g)+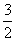 H2(g)
H2(g)
 NH3(g) ΔH=(a+b) kJ·mol-1
NH3(g) ΔH=(a+b) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知723 K时,2SO2(g)+O2(g)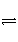
 2SO3(g) ΔH=-Q1。在相同条件下,向一密闭容器中通入1 mol SO2和0.5 mol O2,达到平衡时放出的热量为Q2,则Q1、Q2满足的关系是
2SO3(g) ΔH=-Q1。在相同条件下,向一密闭容器中通入1 mol SO2和0.5 mol O2,达到平衡时放出的热量为Q2,则Q1、Q2满足的关系是
( )
A.Q2=Q1/2 B.Q2<Q1/2 C.Q2>Q1/2 D.不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解下列溶液一段时间后再加入一定量的某种纯净物(方括号内的物质),能使溶液恢复到原来的成分和浓度的是( )
A.AgNO3[AgNO3] B.NaOH[H2O] C.KCl[KCl] D.CuSO4[Cu(OH)2]
查看答案和解析>>
科目:高中化学 来源: 题型:
按图甲装置进行实验,若图乙中横坐标x表示通过电极的电子的物质的量。下列叙述正确的是( )
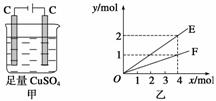
A.F表示反应生成Cu的物质的量
B.E表示反应实际消耗H2O的物质的量
C.E表示反应生成O2的物质的量
D.F表示反应生成H2SO4的物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
有4组同一族元素所形成的不同物质,在101 kPa时测定它们的沸点(℃)如下表所示:
| 第一组 | He -268.8 | (a) -249.5 | Ar -185.8 | Kr -151.7 |
| 第二组 | F2 -187.0 | Cl2 -33.6 | (b) 58.7 | I2 184.0 |
| 第三组 | (c) 19.4 | HCl -84.0 | HBr -67.0 | HI -35.3 |
| 第四组 | H2O 100.0 | H2S -60.2 | (d) -42.0 | H2Te -1.8 |
下列各项判断正确的是( )
A.a、b、c的化学式分别为Ne2、Br2、HF
B.第二组物质的氧化性顺序为b>Cl2
C.第三组与第四组相比较,化合物的稳定性顺序为HBr>d
D.第四组物质中H2O的沸点最高,是因为H2O分子内存在氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
进行如下实验:在A锥形瓶中放入10 g绿豆粒大的碳酸钙,在B锥形瓶中放入5 g粉末状的碳酸钙,分别加入50 mL 1 mol·L-1的盐酸。下图中(图中:x表示时间;y表示锥形瓶中碳酸钙减少的质量),能正确表示实验结果的是( )
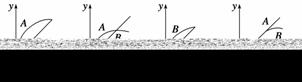
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com