
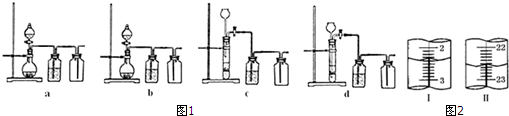
���� ��1������������ܶȴ��ڿ������ռ�����ĵ���Ӧ�ý����ܳ������̣ܶ�
��2������ϴ�ӵõ������ᱵ������ϴ�Ӹɾ��ķ��������ݳ���������ܸ����е��Ȼ��������ʵ����������ӵĴ��������
��3������ȷ�����ɵ����ᱵ������ȫ��ɣ�������������m1�IJ�ֵС��0.001g��
��4�����������·�Ӧ����Ӧ�ﻹӦ���������ӣ������л�Ҫˮ��Ȼ����ݻ��ϼ����������ƽ�÷�Ӧ��
��5����������һ�����ʵ���Ũ�ȵ���Һ�����ж�ʹ��������
��6�����ݵζ��ܹ��켰ͼʾ�ζ�����Һ��������ĵĸ��������Һ�����Ȼ����ݷ�Ӧ����ʽ�����������г���Ʒ���ȵı���ʽ��
��7��H2SO3��H2CO3�����ڶ�Ԫ�ᣬҪ��ͨ���Ƚ϶��ߵ�pH����֤���ߵ�����ǿ��������ʹ���ߵ�Ũ����ͬ���������ڱȽ�pH������������ʵ���Ũ�Ȳ���ȣ����Ը�ʵ����Ʋ���ȷ��Ҫ��������ǿ�������Բ��ö��ַ�������������ˮ��ԭ������Խ����Ӧ��ǿ���ξ�Խ��ˮ�⣩��Ҳ�������ý�ǿ������ȡ�������������飮
��� �⣺��1�����ڶ���������ܶȴ��ڿ���������ռ�������������ĵ���Ӧ�ý����ܳ������̣ܶ���b��ȷ��
�ʴ�Ϊ��b��
��2������ϴ�ӵõ������ᱵ������ϴ�Ӹɾ��ķ��������ݳ���������ܸ����е��Ȼ�������������Ϊ�������ϴ�ӹ��˳�����Һ�еμ���������Һ���������ɣ�����������ϴ����
�ʴ�Ϊ�������ϴ�ӹ��˳�����Һ�еμ���������Һ���������ɣ�����������ϴ����
��3���жϲ�����������m1g�ܹ���Ϊʵ��ⶨֵ�������ʽ��������Ʒ���ȣ������ظ���ɡ���ȴ����������ɺ������������m1�IJ�ֵС��0.001g��
�ʴ�Ϊ���ظ���ɡ���ȴ������������������m1�IJ�ֵС��0.001g��
��4������������ӵ���SԪ��Ϊ+4�ۣ���Ӧ���Ϊ+6�۵���������ӣ����ϼ�����2�ۣ����������������Ԫ�صĻ��ϼ�Ϊ+7�ۣ���Ӧ���Ϊ+2�۵������ӣ����ϼ۽���5�ۣ�������������ӵ�ϵ��Ϊ5������������ӵ�ϵ��Ϊ2��Ȼ�����ù۲취��ƽ�ɵã�5SO32-+2MnO4-+6H+=5SO42-+2Mn2++3H2O��
�ʴ�Ϊ��5SO32-+2MnO4-+6H+=5SO42-+2Mn2++3H2O��
��5����������һ�����ʵ���Ũ�ȵ���Һ�����У���Ҫʹ�õ������У�һ���ݻ�������ƿ�����������ʱ�õ����������ܽ������Ҫ���ձ��н��У�����ʱ��Ҫʹ�ý�ͷ�ιܣ�������Ҫ�������У�a������ƿ��b����������d���ձ���e����ͷ�ιܣ�һ�㲻��Ҫ��Ϊc���ζ��ܣ�
�ʴ�Ϊ��c��
��6���ζ��ܵ�ÿ��С�̶�Ϊ0.10mL������ͼ2��ʾ��ͼI��ʾ������Ϊ2.40mL��ͼII��ʾ��ĩ����Ϊ22.60mL���ζ��ܹ����ĵĸ��������Һ�����Ϊ����22.60-2.40��mL=20.20mL�����ĸ�����ص����ʵ���Ϊ��cmol/L��0.0202L=0.0202cmol��AmL��Ʒ��Һ��ȫ��Ӧ���ĸ�����ص����ʵ���Ϊ��0.0202cmol��$\frac{AmL}{VmL}$=$\frac{0.0202cA}{V}$mol�����ݷ�Ӧ5SO32-+2MnO4-+6H+=5SO42-+2Mn2++3H2O��֪��mg��Ʒ�к����������Ƶ����ʵ���Ϊ��$\frac{0.0202cA}{V}$mol��$\frac{5}{2}$=$\frac{0.0505cA}{V}$mol��
����Ʒ���ȵļ���ʽΪ��$\frac{126g/mol��\frac{0.0505cA}{V}mol}{mg}$��100%��
�ʴ�Ϊ��2.40mL��$\frac{126g/mol��\frac{0.0505cA}{V}mol}{mg}$��100%��
��7��H2SO3��H2CO3�����ڶ�Ԫ�ᣬҪ��ͨ���Ƚ϶��ߵ�pH����֤���ߵ�����ǿ��������ʹ���ߵ�Ũ����ͬ������SO2��CO2��������ˮ��ı�����Һ��Ũ����Ȼ����ȣ���Ϊ���ߵ��ܽ�Ȳ�ͬ�������Ը�ʵ����Ʋ���ȷ��Ҫ��������ǿ�������Բ��ö��ַ��������磺�����٣�������ͬ���ʵ���Ũ�ȵ�NaHSO3��NaHCO3��Һ������ȼƣ���pH��ֽ��������Һ��pH��ǰ�ߵ�pHС�ں��ߣ�֤��H2SO3����ǿ��H2CO3�������ڣ���SO2��������ͨ��NaHCO3��Na2CO3����Һ������KMnO4��Һ��Ʒ����Һ������ʯ��ˮ��Ʒ����Һ����ɫ���ҳ���ʯ��ˮ����ǣ�֤��H2SO3����ǿ��H2CO3�ȣ�
�ʴ�Ϊ������ȷ��SO2��CO2��������ˮ��ı�����Һ��Ũ�Ȳ���ȣ��������ڱȽ�pH��
���� ���⿼��������ʵ�鷽������ƣ���Ŀ�Ѷ��еȣ��漰�к͵ζ������㡢����һ�����ʵ���Ũ�ȵ���Һ��������ѧʵ��װ���жϡ��������ʷ�������������۵�֪ʶ������֪ʶ��϶ࡢ�ۺ��Խ�ǿ����ֿ���ѧ���ķ�����������������ѧʵ���������������ջ�ѧʵ�������������Ϊ���ؼ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��� | B�� | ��С | C�� | ���� | D�� | ��ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�߶����¿�һ��ѧ�Ծ��������棩 ���ͣ�ѡ����
����Ԫ�ذ��������������ڡ��ǵȣ���ͼΪ����Ԫ���⻯��a��b��c��d������������ʾ��ͼ�����й�������Ԫ�ص�˵����ȷ��
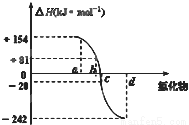
A������18e-�������⻯����ֻ���ڼ��Լ�
B���⻯��ķе��С��H2O��H2S��H2Se��H2Te
C��a����Ӧ���⻯����H2O
D��ÿ1mol H2S�ֽ������20KJ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�߶����¿�һ��ѧ���������棩 ���ͣ�ʵ����
ij������ȤС���H2O2�ķֽ�������������ʵ��̽����
��1���±��Ǹ�С���о�Ӱ��������⣨H2O2���ֽ����ʵ�����ʱ�ɼ���һ�����ݣ�
��10 mL H2O2��ȡ150 mL O2�����ʱ��
Ũ�� ʱ�䣨�룩 ��Ӧ���� | 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 |
���������������� | ���� ����Ӧ | ���� ����Ӧ | ���� ����Ӧ | ���� ����Ӧ |
�������������� | 360 | 480 | 540 | 720 |
����MnO2���������� | 10 | 25 | 60 | 120 |
��С������Ʒ���ʱ��������Ũ�ȡ�a��___________b��___________�����ضԹ�������ֽ����ʵ�Ӱ�졣
�ڴ�����Ӱ��H2O2�ֽ����ʵ�����a��b����ѡһ����˵�������ضԸ÷�Ӧ���ʵ�Ӱ�죺_____________��
��2����������ͬ��������С��ͬ��MnO2�ֱ���뵽5 mL 5%��˫��ˮ�У����ô����ǵ�ľ�����ԡ��ⶨ������£�
���� ��MnO2�� | ������� | �۲��� | ��Ӧ��������ʱ�� |
��ĩ״ | ��ϲ��� | ���ҷ�Ӧ�������ǵ�ľ����ȼ | 3.5���� |
��״ | ��Ӧ���������Ǻ�����ľ��δ��ȼ | 30���� |
��д��H2O2������Ӧ�Ļ�ѧ����ʽ��______________________��
��ʵ����˵���������õĴ�С��________________�йء�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�߶����¿�һ��ѧ���������棩 ���ͣ�ѡ����
��ӦCO��g����2H2��g�� 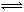 CH3OH��g�������е������仯�������ͼ��ʾ�����ߢ�����ߢ�ֱ��ʾ��ʹ�ô�����ʹ�ô�������������������ж���ȷ����
CH3OH��g�������е������仯�������ͼ��ʾ�����ߢ�����ߢ�ֱ��ʾ��ʹ�ô�����ʹ�ô�������������������ж���ȷ����
A���÷�Ӧ�Ħ�H����91 kJ/mol B������������÷�Ӧ�Ħ�H��С
C����Ӧ�������������������������� D������÷�Ӧ����Һ̬CH3OH����H���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
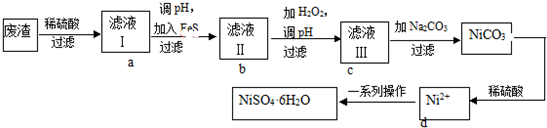
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
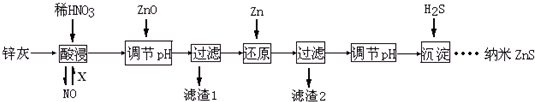
| A�� | ���ʱFeO��ϡHNO3��Ӧ�����ӷ���ʽΪ3FeO+10H++NO${\;}_{3}^{-}$�T3Fe3++NO��+5H2O | |
| B�� | �������β��ѭ�����ã������X���������O2 | |
| C�� | ����2�еijɷֺ�Zn��Fe | |
| D�� | ����Һ��Zn2+Ũ��ΪС��1.0��10-5mol•L-1ʱ�������Ϊ�������ȫ����ҪʹZn2+������ȫ����Һ��S2-Ũ��Ӧ����1.6��10-19mol•L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 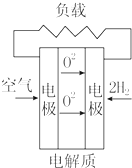 ����������ȼ�ϵ�� | B�� | 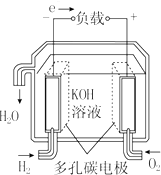 ����ȼ�ϵ�� | ||
| C�� | 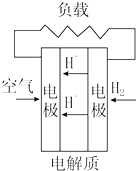 ���ӽ���Ĥȼ�ϵ�� | D�� | 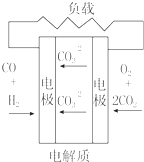 ������ȼ�ϵ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
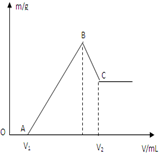 ��0.1molMg��Al���������100mL4mol/L�������У�Ȼ���ٵμ�1mol/L��NaOH��Һ���ڵμ�NaOH��Һ�Ĺ����У���������m��NaOH��Һ�����V�ı仯��ͼ��ʾ��
��0.1molMg��Al���������100mL4mol/L�������У�Ȼ���ٵμ�1mol/L��NaOH��Һ���ڵμ�NaOH��Һ�Ĺ����У���������m��NaOH��Һ�����V�ı仯��ͼ��ʾ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com