
| A�� | ����٣�������������ܽ����� | |
| B�� | ����ڣ��漰�����ӷ�ӦΪFeS2+14Fe3++8H2O�T15Fe2++2SO42-+16H+ | |
| C�� | ����ۣ�����Һ���ȵ��н϶�����������������Ƚ�Һ�����ɣ��ɵô����̷� | |
| D�� | ����ܣ���Ӧ�������Ʋ�����ʹ�����л���Fe��OH��3 |
���� ���Ʊ��̷����̿�֪����������Ҫ�ɷ֣�Fe3O4��Fe2O3��FeO�����������ᣬ��Һ��Fe2+��Fe3+������ڷ���FeS2+7Fe2��SO4��3+8H2O=15FeSO4+8H2SO4�������Ϊ����Ũ������ȴ�ᾧ�����̷����̷��백ˮ�������ɷ���������ԭ��Ӧ����Fe��OH��3���Դ������
��� �⣺A�����̷����������Ϊ��������ӣ�����٣�������������ܽ���������A��ȷ��
B������ڷ���FeS2+7Fe2��SO4��3+8H2O=15FeSO4+8H2SO4�����ӷ�ӦΪFeS2+14Fe3++8H2O�T15Fe2++2SO42-+16H+����B��ȷ��
C�������Ϊ����Ũ������ȴ�ᾧ�����̷���������ʱ�̷�����ʧȥ�ᾧˮ����C����
D������ܣ���Ӧ�������Ʋ������̷��백ˮ�������ɷ���������ԭ��Ӧ����Fe��OH��3����D��ȷ��
��ѡC��
���� ���⿼����������ᴿ��Ϊ��Ƶ���㣬�����Ʊ������з����ķ�Ӧ���������뷽����ʵ�鼼�ܵ�Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬ע��ѡ��CΪ�����ѵ㣬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
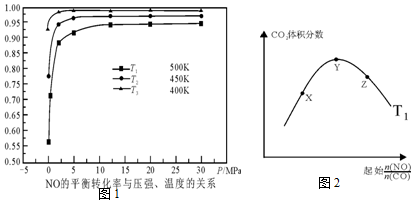
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڢ����ӷ���ʽΪNa++NH3��H2O+CO2�TNaHCO3��+NH4+ | |
| B�� | �ڢõ��ľ�����Na2CO3•10H2O | |
| C�� | A������CO2��B������NH3 | |
| D�� | �ڢ�����������Ҫ�������ܽ⡢�������ᾧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ���� | B�� | ��ϩ | C�� | ���� | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �й����ǵ�˵������ȷ���ǣ�������
�й����ǵ�˵������ȷ���ǣ�������| A�� | �����ܷ���������Ӧ | |
| B�� | �������ڵ��� | |
| C�� | ������һ�������£��ܷ����ӳɺ�ȡ����Ӧ | |
| D�� | �����������ǻ�Ϊͬ���칹�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ��һ��10���¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
��I������ij��Һ���Ƿ�SO42-����ȷ����˳���ǣ�ȡ����δ֪��Һ������____________________�������� �����ټ���_____________�������� ����֤��ԭ��Һ����SO42-��BaSO4��NaCl������Һ�ڷ���������漰�����ˡ�ϴ�ӳ���������֤����ֽ�ϵ�BaSO4�����Ѿ�ϴ���ķ�����_______________��
��������A��B�����л����Һ��������A��B���ܣ������������ѧ��Ӧ���ڳ�ѹ�£�A�ķе�Ϊ35�棬B�ķе�Ϊ200�档�ش��������⣺
��1����������A��B�Ļ������õķ����� ����Ҫ�IJ��������оƾ��ơ��¶ȼơ�ţ�ǹܡ�������ƿ������ �� ��ÿ��1�֣���
��2��Ӧ������������������ȵõ��������� ��
��3����ȼ�ƾ���ǰ�����һ�������� ��
������ͼ�������Լ�ƿ��ǩ�ϵ����ݣ�

��1������������ʵ���Ũ���� mol��L-1��
��2��ij��ѧ��ȤС������������ʵ�ʵ��̽��ʱ����Ҫ240 mL 4.6 mol��L-1��ϡ���ᣬ����Ҫȡ mL�ĸ����ᡣ�������������ϡ�͵�ʵ�����Ϊ ��
��3����������������240 mL 4.6 mol��L-1��ϡ���ᣬʵ�������У�
��50 mL��Ͳ ��100 mL��Ͳ ��������ƽ �ܲ�����
��250 mL����ƿ ��ͷ�ι� ���ձ� ����ƿ
ʵ��ʱʹ��ѡ���������Ⱥ�˳��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ��һ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�ٽ�������ˮ�Ϳɼ������ǡ�����ͭ��δ��̼��Ʒ�δ��
���÷�Һ©��������ͺ�ˮ�Ļ���
��ϡ��Ũ����ʱ����Ũ�������ձ�������ע��ˮ�в����Ͻ��裻
���ò�����պȡ��Һ����pH��ֽ���룬�����Һ��pH��
������һ�����ʵ���Ũ�ȵ���Һ����Ҫ�IJ�������ֻ������ƿ���ձ���
����250mL�ձ��У�����216mLˮ��24g NaOH���壬����10% NaOH��Һ��
A. �٢ڢܢ� B. �٢ܢݢ� C. �٢ۢܢ� D. �ڢۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
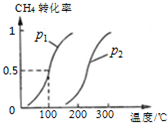 ���飬�״��������ǻ�����Ʒ����Ҫԭ�ϣ�
���飬�״��������ǻ�����Ʒ����Ҫԭ�ϣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
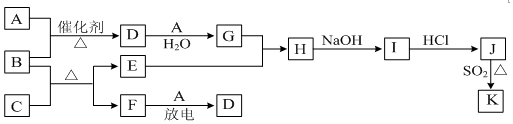
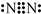
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com