
| 温度 | 平衡时NH3的 物质的量mol |
| T1 | 1.2 |
| T2 | 1.0 |
分析 根据该反应△H<0,温度升高,平衡逆向移动,则氨气的含量会减小由表中数据可知,T1<T2;根据平均速率v(NH3)=$\frac{△c}{△t}$,K=$\frac{c(NH{\;}_{3}){\;}^{2}}{c(N{\;}_{2})c(H{\;}_{2}){\;}^{3}}$计算.
解答 解:该反应△H<0,温度升高,平衡逆向移动,则氨气的含量会减小,由表中数据可知,T1<T2;若经过10min反应达到平衡,则平均速率v(NH3)=$\frac{\frac{1.0mol}{2L}}{10min}$=0.05mol/(L•min);根据反应方程式:N2(g)+3H2(g)═2NH3,该温度下,达到平衡状态时各组分的浓度为:c(NH3)=0.5ol/L,c(H2)=$\frac{3.5mol-1.5mol}{2L}$=1mol/L,c(N2)=$\frac{2mol-0.5mol}{2L}$=0.75mol/L,平衡常数为:K=$\frac{c(NH{\;}_{3}){\;}^{2}}{c(N{\;}_{2})c(H{\;}_{2}){\;}^{3}}$=$\frac{(0.5){\;}^{2}}{(0.75)×(1){\;}^{3}}$=0.33,
故答案为:<; 0.05;0.33.
点评 本题主要考查了反应速率、平衡常数的计算以及平衡移动原理,难度不大,注意基本公式的应用.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | CuCl2[CuCl2溶液] | B. | AgNO3[Ag2O] | C. | NaCl[HCl溶液] | D. | CuSO4[CuSO4] |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 化学式 | 电离平衡常数(25℃) |
| HCN | K=5.0×10-10 |
| H2CO3 | K1=4.4×10-7,K2=4.7×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 Ag+(aq)+Cl-(aq),银离子与氨水结合,降低了溶液中银离子的浓度,使上述平衡正向移动,促使AgCl溶解.
Ag+(aq)+Cl-(aq),银离子与氨水结合,降低了溶液中银离子的浓度,使上述平衡正向移动,促使AgCl溶解.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 难溶电解质 | AgCl | AgBr | AgI | Ag2SO4 | Ag2CrO4 |
| Ksp | 1.8×10-10 | 5.4×10-13 | 8.5×10-17 | 1.4×10-5 | 1.12×10-12 |
| A. | 由溶度积常数不能判断相应物质的溶解性大小 | |
| B. | 将等体积的4×10-3 mol/L的AgNO3溶液和4×10-3mol/L K2CrO4溶液混合,有Ag2CrO4沉淀产生 | |
| C. | 向AgCl的悬浊液中滴加饱和NaBr溶液不能得到黄色AgBr | |
| D. | 向100 mL 0.02mol/L的NaSO4溶液中加入100mL0.02mol/L的AgNO3溶液,有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
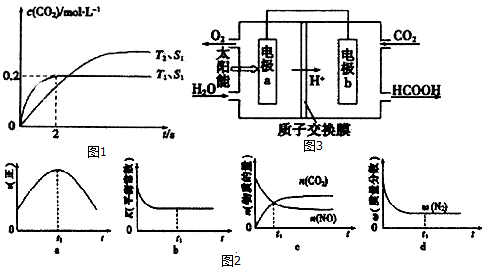
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
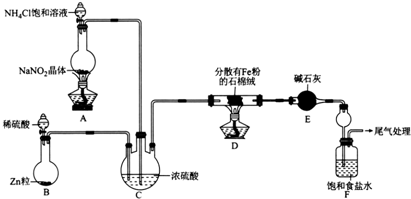
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用HCl溶液代替蒸馏水洗涤AgCl,可以减少沉淀损失 | |
| B. | 将BaSO4固体加入到饱和Na2CO3溶液中,充分反应后过滤、洗涤;往滤渣中滴加稀盐酸,有气体产生,则证明此条件下Ksp(BaSO4)>Ksp(BaCO3) | |
| C. | 向水中加入NaHCO3或NaHSO4固体后,水的电离程度均增大 | |
| D. | 对于乙酸乙酯的水解反应,加入稀硫酸可提高反应速率和乙酸乙酯的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a=4 | |
| B. | S2O32-是还原剂 | |
| C. | 将Y均匀分散到水中形成的体系具有丁达尔效应 | |
| D. | 每有3 mol Fe2+参加反应,反应中转移的电子总数为5 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com