



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ijѧ��Ҫ��50 mL NaOH��Һ��CO2����ȡ��Na2CO3��Һ����֪CO2������ͨ��NaOH��Һ�����м�������NaHCO3��������������
ʵ�����������Լ�����δ֪Ũ�ȵ�NaOH��Һ�� ��37�������ᡡ ��37�������ᡡ ��14�������ᡡ �ݴ���ʯ�ޱ���NaHCO3��Һ
ʵ������������������Ͳ���ձ�����Ƥ�ܣ��������ܣ���Һ©�����ձ���ϴ��ƿ���ƾ��ơ�
��֪�±��и������ڳ���ʱ���ܽ�ȣ�g/100 g H2O��
| Na2CO3 | NaHCO3 | NaCl | Na2SO4 | NaHSO4 | NaOH |
| 15.9 | 8.4 | 35 | 35.5 | 20 | 40 |
��ʵ���������ͼ���������⣬��Ӧ�У��������� ��������װ����������
ʵ��Ϊ��֤�Ƶ�Na2CO3�Ĵ��ȣ�Ӧѡ�õ�ҩƷ�������⣬��Ӧ��Ҫ���������� ��
��Ҫ����ʵ�鲽�裬ֱ���Ƶô�̼������Һ������������������������������
���ݸ������ܽ�ȱ�������֤�����ƹ����в����о�����������������������Һ�к�NaOH���������������ֵ�Ƕ��٣�д�����㲽��ͱ�Ҫ������˵������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
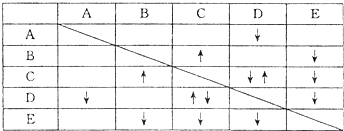
(8��)ʵ������NaHSO4 ,Ba(OH)2, NH3 • H2O NaHCO3��KAl(SO4)2������ɫ��Һ������ͨ������֮������Ӧ���������м��𡣲������ʼ�ķ�Ӧ�������±���
���С�����ʾ�����������ʣ���
����ʾ���ɳ�����
����������Ϣ���ش��������⣺
(1)B��E�Ļ�ѧʽ�ֱ�Ϊ_______��___________��
(2)д��A�ĵ��뷽��ʽ___________________________����
(3)C��D����Һ��Ӧ�����ӷ���ʽΪ___________________________��
(4)����0.1 mol���ʵ�D��Һ�еμ�E��Һ�������ɳ��������ʵ���֮�����Ϊ_________mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012�����ʡ֣���и�����һ������Ԥ�⻯ѧ�Ծ��������棩 ���ͣ������
(8��)ʵ������ NaHSO4 ,Ba(OH)2, NH3 ? H2O NaHCO3��KAl(SO4)2������ɫ��Һ������ͨ������֮������Ӧ���������м��𡣲������ʼ�ķ�Ӧ�������±���
���С� ����ʾ�����������ʣ���
����ʾ�����������ʣ��� ����ʾ���ɳ�����
����ʾ���ɳ�����
����������Ϣ���ش��������⣺
(1)B��E�Ļ�ѧʽ�ֱ�Ϊ_______��___________��
(2) д��A�ĵ��뷽��ʽ___________________________����
(3) C��D����Һ��Ӧ�����ӷ���ʽΪ___________________________��
(4) ����0.1 mol���ʵ�D��Һ�еμ�E��Һ�������ɳ��������ʵ���֮�����Ϊ_________mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�����ʡ֣���и�����һ������Ԥ�⻯ѧ�Ծ��������棩 ���ͣ������
(8 ��)ʵ������ NaHSO4 ,Ba(OH)2, NH3 • H2O NaHCO3��KAl(SO4)2 ������ɫ��Һ������ͨ������֮������Ӧ���������м��𡣲������ʼ�ķ�Ӧ�������±���
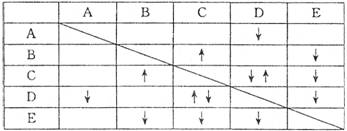
���С� ����ʾ�����������ʣ���
����ʾ�����������ʣ��� ����ʾ���ɳ�����
����ʾ���ɳ�����
����������Ϣ���ش��������⣺
(1)B��E�Ļ�ѧʽ�ֱ�Ϊ_______��___________��
(2) д��A�ĵ��뷽��ʽ___________________________����
(3) C��D����Һ��Ӧ�����ӷ���ʽΪ___________________________��
(4) ����0.1 mol���ʵ�D��Һ�еμ�E��Һ�������ɳ��������ʵ���֮�����Ϊ_________mol��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com