
����Ŀ����������ת����ϵ(���ַ�Ӧ��������������ȥ)��A��B��C��D�о�����ͬһ��Ԫ�أ��ش��������⣺

��1����B����ʹƷ����Һ��ɫ�����壬д��D��Ũ��Һ��Cu�ڼ�������·�Ӧ�Ļ�ѧ����ʽ_______________________________��
��2����A��N2����
��Bת��ΪC������_______________________________��
��д������Fe��D��ϡ��Һ��Ӧ����ԭ����ֻ��B�������ӷ���ʽ_______________________________��
��3����A����ʹʪ��ĺ�ɫʯ����ֽ���������壬��
������O2 �ڸ��¡������������·�Ӧ����B���˻�ѧ����ʽΪ
_______________________________��
��д��ʵ�����ù�����ȡA����Ļ�ѧ����ʽ_______________________________��
����Ҫ�ռ�B���壬�����ռ�װ���к��ʵ���(�����)______________��

��1.92gͭͶ��һ����D��Ũ��Һ�У�ͭ��ȫ�ܽ⣬���ռ���672mL����(��״��)����Ӧ������D �����ʵ���Ϊ_____________��
���𰸡� Cu��2H2SO4(Ũ)![]() CuSO4��SO2����2H2O ��ɫ�����Ϊ����ɫ 3Fe��8H����2NO3�� === 3Fe2����2NO����4H2O 4NH3+5O2
CuSO4��SO2����2H2O ��ɫ�����Ϊ����ɫ 3Fe��8H����2NO3�� === 3Fe2����2NO����4H2O 4NH3+5O2 ![]() 4NO+6H2O 2NH4Cl��Ca(OH)2
4NO+6H2O 2NH4Cl��Ca(OH)2![]() CaCl2��2NH3����2H2O C��E 0.09mol
CaCl2��2NH3����2H2O C��E 0.09mol
���������������⣺
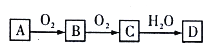
��1����B����ʹƷ����Һ��ɫ������������������Ӧ������֪BΪ����������A������������ȼ�����ɶ�����������������������������CΪ������������������ˮ��Ӧ����DΪ���ᡣŨ������Cu�ڼ�������·�Ӧ�Ļ�ѧ����ʽΪCu��2H2SO4(Ũ)![]() CuSO4��SO2����2H2O����2����A��N2��������������Ӧ����BΪһ��������һ��������������Ӧ����CΪ��������������������ˮ��Ӧ����DΪ�����һ����������Bת��ΪC������Ϊ����ɫ�����Ϊ����ɫ���ڹ���Fe��ϡ���ᷴӦ����ԭ����ֻ��NO�������ӷ���ʽΪ3Fe��8H����2NO3�� = 3Fe2����2NO����4H2O����3����A����ʹʪ��ĺ�ɫʯ����ֽ���������弴��������ٰ�����O2 �ڸ��¡������������·�Ӧ����NO��ˮ ����Ӧ�Ļ�ѧ����ʽΪ4NH3+5O2
CuSO4��SO2����2H2O����2����A��N2��������������Ӧ����BΪһ��������һ��������������Ӧ����CΪ��������������������ˮ��Ӧ����DΪ�����һ����������Bת��ΪC������Ϊ����ɫ�����Ϊ����ɫ���ڹ���Fe��ϡ���ᷴӦ����ԭ����ֻ��NO�������ӷ���ʽΪ3Fe��8H����2NO3�� = 3Fe2����2NO����4H2O����3����A����ʹʪ��ĺ�ɫʯ����ֽ���������弴��������ٰ�����O2 �ڸ��¡������������·�Ӧ����NO��ˮ ����Ӧ�Ļ�ѧ����ʽΪ4NH3+5O2 ![]() 4NO+6H2O����ʵ�����ù����Ȼ�狀��������Ƽ�����ȡ������ͬʱ�����Ȼ��ƺ�ˮ����Ӧ�ĵĻ�ѧ����ʽΪ2NH4Cl��Ca(OH)2
4NO+6H2O����ʵ�����ù����Ȼ�狀��������Ƽ�����ȡ������ͬʱ�����Ȼ��ƺ�ˮ����Ӧ�ĵĻ�ѧ����ʽΪ2NH4Cl��Ca(OH)2![]() CaCl2��2NH3����2H2O����BΪһ��������һ������������ˮ����ˮ��Ӧ������Ⱦ�����壬�ܶȱȿ���С������Ҫ�ռ�NO���壬�����ռ�װ����A��B������ɿ�����Ⱦ������������Ӧ�������ϣ�C��ˮ���ռ������ϣ�DΪ��ˮ���ռ�������Ӧ�ö̽������������ϣ�EΪ��ˮ���ռ��ҵ���Ӧ�ý����������ϣ��ʺ��ʵ���CE����һ��������������Ӧ����C Ϊ��������������������ˮ��Ӧ����DΪ���ᣬ 1.92gͭͶ��һ����Ũ�����У�ͭ��ȫ�ܽ⣬���ռ���672mL����(��״��)��672ml����Ӧ����NO2 ��NO�Ļ������ʵ�����
CaCl2��2NH3����2H2O����BΪһ��������һ������������ˮ����ˮ��Ӧ������Ⱦ�����壬�ܶȱȿ���С������Ҫ�ռ�NO���壬�����ռ�װ����A��B������ɿ�����Ⱦ������������Ӧ�������ϣ�C��ˮ���ռ������ϣ�DΪ��ˮ���ռ�������Ӧ�ö̽������������ϣ�EΪ��ˮ���ռ��ҵ���Ӧ�ý����������ϣ��ʺ��ʵ���CE����һ��������������Ӧ����C Ϊ��������������������ˮ��Ӧ����DΪ���ᣬ 1.92gͭͶ��һ����Ũ�����У�ͭ��ȫ�ܽ⣬���ռ���672mL����(��״��)��672ml����Ӧ����NO2 ��NO�Ļ������ʵ�����![]() ��0.03mol����Ӧ����������ͭ��n(NO3-)=2n(Cu2+)=
��0.03mol����Ӧ����������ͭ��n(NO3-)=2n(Cu2+)=![]() �����ݵ�ԭ���غ��֪����Ӧ������Ũ��������ʵ���Ϊ0.03mol+0.06mol=0.09mol��
�����ݵ�ԭ���غ��֪����Ӧ������Ũ��������ʵ���Ϊ0.03mol+0.06mol=0.09mol��


 �㽭��У��ʦ���ϵ�д�
�㽭��У��ʦ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���ṹ��ʽ��д������ǣ� ��
A.CH3��CH2��3CH3
B.CH3C��CH3��2CH2CH3
C.CH3��CH2��2C��CH3��3
D.CH3CH��CH3��3CH2CH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ͼױ���Ƚϣ����������в���ȷ���ǣ� ��
A.�����ڷ�����
B.����ʹKMnO4������Һ��ɫ
C.�����ڿ�����ȼ��
D.���ܷ���ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӵļ����ܴﵽԤ��Ŀ������ ��
A. ����![]() ���ȵμ���ˮ���ٵμ�KSCN��Һ������죬����Fe2+
���ȵμ���ˮ���ٵμ�KSCN��Һ������죬����Fe2+
B. ����NH4+���ȵμ�NaOH��Һ�����ȣ���ʪ����ɫʯ����ֽ���飬����죬����NH4+
C. ����Cl�����ȵμ�AgNO3��Һ���ٵμ����ᣬ���а�ɫ����������Cl��
D. ����![]() ���μ����ᣬ�����ɵ�����ͨ��Ʒ����Һ����Ʒ����Һ��ɫ������
���μ����ᣬ�����ɵ�����ͨ��Ʒ����Һ����Ʒ����Һ��ɫ������![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ���仯�������������������й㷺��Ӧ�ã�
��1��ͭ�ɲ������·����Ʊ�������ͭ��Cu2S+O2 ![]() 2Cu+SO2
2Cu+SO2
ʪ����ͭ��CuSO4+Fe�TFeSO4+Cu
�������ַ����У�ͭԪ�ؾ��������������ԭ������ͭ���ʣ�
��2��ӡˢ��·����ʹ�õ�ͭ��Ҫ�������ã�����һ����FeCl3��Һ����ӡˢ��·���Ʊ�CuCl22H2O��ʵ����ģ����չ������£�![]()
��֤�����������FeCl3��Һ�����ķ����� ��
�ڲ���2�����ӵ������������˵��� ��
A��HNO3B��H2O2C��KMnO4
�۲���3��Ŀ����ʹ��Һ��pH���ߵ�4.2����ʱFe3+��ȫ��������ѡ�õġ��Լ�1���� �� ��д��һ�ּ��ɣ�
������ũ��CuCl2��Һʱ��Ҫ�μ�Ũ���ᣬĿ�������û�ѧ����ʽ����ϼ�Ҫ������˵�������پ���ȴ���ᾧ�����ˣ��õ�CuCl22H2O��
����������H2O2��ϡ���Ṳͬ����ӡˢ��·���Ʊ�����ͭʱ�����Ȼ�ѧ����ʽ�ǣ�
Cu��s��+H2O2��l��+H2SO4��nq���TCuSO4��aq��+2H2O��l����H1=��320kJ/mol
��֪��2H2O��l���T2H2O��l��+O2��g����H2=��196kJ/mol
H2��g��+ ![]() O2��g���TH2O��l����H3=��286kJ/mol
O2��g���TH2O��l����H3=��286kJ/mol
��ӦCu��s��+H2SO4��aq���TCuSO4��aq��+H2��g���ġ�H= ��
��3����ʵ�ַ�ӦCu+H2SO2�TCuSO4+H2 �� ������Ϊ��ʵ�ָ�ת����װ���е������ڣ�����缫���ϣ��Cu����C����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У����ø������������Һ������ǣ� ��
A.��ϩ����Ȳ
B.��ϩ����
C.��������
D.�����ױ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȼ�ղ���������β���У������Ĵ�����Ⱦ����Ҫ�ǣ� ��
A.����������
B.���������
C.��������
D.��ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������Ȼ�ѧ����ʽ�У��йء�H�ıȽ���ȷ���ǣ� �� ��CH4��g��+2O2��g���TCO2��g��+2H2O��g����H1CH4��g��+2O2��g���TCO2��g��+2H2O��l����H2
��NaOH��aq��+ ![]() H2SO4��Ũ���T
H2SO4��Ũ���T ![]() Na2SO4��aq��+H2O��l����H3
Na2SO4��aq��+H2O��l����H3
NaOH��aq��+CH3COOH��aq���TCH3COONa��aq��+H2O��l����H4 ��
A.��H1����H2����H3����H4
B.��H1����H2����H3����H4
C.��H1=��H2����H3����H4
D.��H1����H2����H3����H4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NAΪ�����ӵ�����������������ȷ���ǣ� ��
A.1L 0.5molL��1��ˮ������NH4+��Ϊ0.5NA
B.1mol Fe������������Ӧת�Ƶĵ�����Ϊ2 NA
C.��״���£�33.6LCO2Լ����1.5NA������
D.1 mol ![]() �к�̼̼˫����Ϊ3 NA
�к�̼̼˫����Ϊ3 NA
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com