
·ÖĪö £Ø1£©ÓÉ¢ŁN2£Øg£©+2O2£Øg£©=2NO2£Øg£©”÷H=-67.7kJ•mol-1
¢ŚN2H4£Øg£©+O2£Øg£©=N2£Øg£©+2H2O£Øg£©”÷H=-534.0kJ•mol-1
¢Ū2NO2£Øg£©?N2O4£Øg£©”÷H=-52.7kJ•mol-1
øł¾ŻøĒĖ¹¶ØĀÉæÉÖŖ¢Ś”Į2-¢Ł-¢ŪµĆ2N2H4£Øg£©+N2O4£Øg£©=3N2£Øg£©+4H2O£Øg£©£¬”÷H=£Ø-534.0kJ•mol-1£©”Į2-£Ø-67.7kJ•mol-1£©-£Ø-52.7kJ•mol-1£©=-947.6 kJ•mol-1£¬ÓÉ“Ė·ÖĪö½ā“š£»
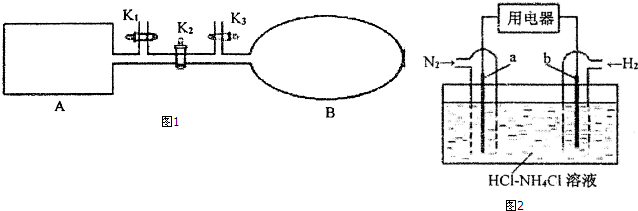
£Ø2£©¢Ł·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±£¬ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬Ę½ŗāŹ±ø÷ÖÖĪļÖŹµÄĪļÖŹµÄĮ攢ÅØ¶ČµČ²»ŌŁ·¢Éś±ä»Æ£»
¢ŚŃ¹ĒæÖ®±ČµČÓŚĪļÖŹµÄĮæÖ®±Č£¬Ę½ŗāŹ±»ģŗĻĘųĢåĪļÖŹµÄĮæĪŖ1mol”Į0.8=0.8mol£¬Ōņ£ŗ
2NO2£Øg£©?N2O4£Øg£©
ĘšŹ¼Įæ£Ømol£©£ŗ1 0
×Ŗ»ÆĮæ£Ømol£©£ŗx 0.5x
Ę½ŗāĮæ£Ømol£©£ŗ1-x 0.5x
ĖłŅŌ1-x+0.5x=0.8£¬½āµĆx=0.4£¬
Ōņv£ØN2O4£©=$\frac{\frac{0.2mol}{aL}}{3s}$=$\frac{1}{15a}$mol/£ØL£®s£©£¬K=$\frac{\frac{0.2}{a}}{£Ø\frac{0.6}{a}£©^{2}}$=$\frac{5a}{9}$£»øł¾ŻµČŠ§Ę½ŗā·ÖĪö£»ČōĘ½ŗāŗóĻņAÖŠŌŁ³äČė0.6molN2O4£¬µČŠ§ĪŖŌŚŌĘ½ŗā»ł“”ÉĻŌö“óŃ¹Ēæ£¬Ę½ŗāÕżĻņŅĘ¶Æ£»
£Ø3£©¢ŁĒāĘųÓÉ0¼Ū±ä³É+1¼Ū£¬»ÆŗĻ¼ŪÉżøß·¢ÉśŃõ»Æ·“Ó¦£¬bŹĒøŗ¼«£»
¢ŚµŖĘųŌŚÕż¼«»ńµĆµē×Ó£¬ĖįŠŌĢõ¼žĻĀÉś³ÉNH4+£¬µē¼«·“Ó¦Ź½ĪŖ£ŗN2+8H++6e-=2NH4+£®
½ā“š ½ā£ŗ£Ø1£©ÓÉ¢ŁN2£Øg£©+2O2£Øg£©=2NO2£Øg£©”÷H=-67.7kJ•mol-1
¢ŚN2H4£Øg£©+O2£Øg£©=N2£Øg£©+2H2O£Øg£©”÷H=-534.0kJ•mol-1
¢Ū2NO2£Øg£©?N2O4£Øg£©”÷H=-52.7kJ•mol-1
øł¾ŻøĒĖ¹¶ØĀÉæÉÖŖ¢Ś”Į2-¢Ł-¢ŪµĆ2N2H4£Øg£©+N2O4£Øg£©=3N2£Øg£©+4H2O£Øg£©£¬
”÷H=£Ø-534.0kJ•mol-1£©”Į2-£Ø-67.7kJ•mol-1£©-£Ø-52.7kJ•mol-1£©=-947.6 kJ•mol-1£¬
¼“ČČ»Æѧ·½³ĢŹ½ĪŖ2N2H4£Øg£©+N2O4£Øg£©=3N2£Øg£©+4H2O£Øg£©”÷H=-947.6 kJ•mol-1£¬
¹Ź“š°øĪŖ£ŗ2N2H4£Øg£©+N2O4£Øg£©=3N2£Øg£©+4H2O£Øg£©”÷H=-947.6 kJ•mol-1£»
£Ø2£©¢ŁBŹĒŅ»øöĘųĢåŃ¹Ēæ²»±äµÄČŻĘ÷£¬ĖłŅŌµ±·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±£¬»ģŗĻĘųĢåµÄŃÕÉ«ŗĶĘųÄŅĢå»ż²»ŌŁøı䣬
¹Ź“š°øĪŖ£ŗĘųÄŅ²»ŌŁ±äŠ”»ņŃÕÉ«²»ŌŁ±ä»Æ£»
¢ŚŃ¹ĒæÖ®±ČµČÓŚĪļÖŹµÄĮæÖ®±Č£¬Ę½ŗāŹ±»ģŗĻĘųĢåĪļÖŹµÄĮæĪŖ1mol”Į0.8=0.8mol£¬Ōņ£ŗ
2NO2£Øg£©?N2O4£Øg£©
ĘšŹ¼Įæ£Ømol£©£ŗ1 0
×Ŗ»ÆĮæ£Ømol£©£ŗx 0.5x
Ę½ŗāĮæ£Ømol£©£ŗ1-x 0.5x
ĖłŅŌ1-x+0.5x=0.8£¬½āµĆx=0.4£¬
Ōņv£ØN2O4£©=$\frac{\frac{0.2mol}{aL}}{3s}$=$\frac{1}{15a}$mol/£ØL£®s£©£¬K=$\frac{\frac{0.2}{a}}{£Ø\frac{0.6}{a}£©^{2}}$=$\frac{5a}{9}$£»“ņæŖK2£¬ŌņĻąµ±ÓŚŹĒŌŚµČĪĀµČŃ¹Ź±µÄĘ½ŗā£¬Ņņ“ĖĘ½ŗāŹ±µČŠ§µÄ£®ÓÉÓŚ“ĖŹ±·“Ó¦ĪļµÄĪļÖŹµÄĮæŹĒBÖŠµÄ¶ž±¶£¬ĖłŅŌ“ņæŖK2Ö®Ē°£¬ĘųĒņBĢå»żĪŖ£ØaL+0.3aL£©”Ā2=0.65aL£¬ČōĘ½ŗāŗóĻņAÖŠŌŁ³äČė0.6molN2O4£¬µČŠ§ĪŖŌŚŌĘ½ŗā»ł“”ÉĻŌö“óŃ¹Ēæ£¬Ę½ŗāÕżĻņŅĘ¶Æ£¬ÖŲŠĀµ½“ļĘ½ŗāŗó£¬Ę½ŗā»ģŗĻĘųÖŠNO2µÄĢå»ż·ÖŹż¼õŠ”£¬
¹Ź“š°øĪŖ£ŗ$\frac{1}{15a}$mol/£ØL£®s£©£»$\frac{5a}{9}$£»0.65a£» ¼õŠ”£»
£Ø3£©¢ŁĒāĘųÓÉ0¼Ū±ä³É+1¼Ū£¬»ÆŗĻ¼ŪÉżøß·¢ÉśŃõ»Æ·“Ó¦£¬ŹĒøŗ¼«£¬¹Ź“š°øĪŖ£ŗb£»
¢ŚµŖĘųŌŚÕż¼«»ńµĆµē×Ó£¬ĖįŠŌĢõ¼žĻĀÉś³ÉNH4+£¬µē¼«·“Ó¦Ź½ĪŖ£ŗN2+8H++6e-=2NH4+£¬¹Ź“š°øĪŖ£ŗN2+8H++6e-=2NH4+£®
µćĘĄ ±¾Ģāæ¼²é»ÆŃ§Ę½ŗā¼ĘĖć£¬Éę¼°µČŠ§Ę½ŗāĪŹĢā£¬½ĻŗƵÄæ¼²éѧɜ·ÖĪö½ā¾öĪŹĢāÄÜĮ¦£¬¹Ų¼üŹĒµČŠ§Ę½ŗāĶ¾¾¶µÄ½ØĮ¢£¬ÄѶČÖŠµČ£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

 £®
£® £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ū | B£® | ¢Ł¢Ś | C£® | ¢Ś¢Ū | D£® | Č«²æÕżČ· |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | °ŃCaO·ÅČėĖ®ÖŠ£ŗCaOØTCa2++O2- | |
| B£® | ¼ÓČČNaHSO4ÖĮČŪ»Æ£ŗNaHSO4ØTNa++H++SO42- | |
| C£® | °ŃAl2£ØSO4£©3·ÅČėĖ®ÖŠ£ŗAl2£ØSO4£©3ØTAl3++SO42- | |
| D£® | °ŃNaCl·ÅČėĖ®ÖŠ£ŗNaClØTNa++Cl- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na+ 1s22s22p6 | B£® | N3+ 1s22s22p6 | C£® | F?1s22s22p6 | D£® | O2?1s22s22p6 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £»
£» £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
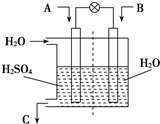 ÓŠČĖÉčĻėÓĆĶ¼ĖłŹ¾×°ÖĆ£¬ŌĖÓƵē»ÆѧŌĄķ½«CO2”¢SO2×Ŗ»ÆĪŖÖŲŅŖ»Æ¹¤ŌĮĻ£®
ÓŠČĖÉčĻėÓĆĶ¼ĖłŹ¾×°ÖĆ£¬ŌĖÓƵē»ÆѧŌĄķ½«CO2”¢SO2×Ŗ»ÆĪŖÖŲŅŖ»Æ¹¤ŌĮĻ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
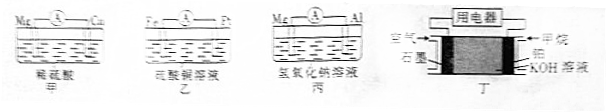
| ×°ÖĆŠņŗÅ | øŗ¼« | ŃōĄė×ÓŅĘĻņ £ØĢīµē¼«²ÄĮĻĆū³Ę£© |
| ¼× | ||
| ŅŅ | £® |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com