
��12�֣���Na+Ũ��Ϊ0.9mol/L��ij������Һ�У������ܺ����±��е����������ӣ�
������ | K+��Ag+��Mg2+��Ba2+ |
������ | NO3-��CO32-��SiO32-��SO42- |
ȡ����Һ100mL��������ʵ�飨��������ڱ�״���²ⶨ����
��� | ʵ������ | ʵ���� |
�� | �����Һ�м�������ϡHCl | ������ɫ�������ų�1.12L���� |
�� | ����ķ�Ӧ���Һ���ˣ��Գ���ϴ�ӡ����������أ��������ù������� | ��������Ϊ3.6g |
�� | �ڢ����Һ�еμ�BaC12��Һ | ���������� |
�Իش��������⣺
��1��ʵ��I��ȷ��һ�������ڵ������� ��
��2��ʵ��I�����ɳ��������ӷ���ʽΪ ��
��3��ͨ��ʵ��I����ͱ�Ҫ���㣬��д�±��������ӵ�Ũ�ȣ��ܼ�����ģ���д��������һ�������ڵ������0��������ȷ���Ƿ���ڵ������������
������ | NO3- | CO32- | SiO32- | SO42- |
c/mol��L-1 |
|
|
|
|
��4���ж�K+�Ƿ���ڣ�������������СŨ�ȣ���������˵������ ��
��12�֣�
��1��Ag+��Mg2+��Ba2+ ��3�֣�
��2��SiO32- + 2H+ === H2SiO3������SiO32-+ 2H+ + H2O === H4SiO4���� ��2�֣�
��3����4�֣�
������ | NO3- | CO32- | SiO32- | SO42- |
c/mol/L | �� | 0.5 | 0.6 | 0 |
��4�����ڣ�����СŨ��Ϊ1.3mol/L ��3�֣�
��������
���������������֪��ҺΪ������Һ�������Һ�к��е����ӱ����ܴ������森��ʵ����֪������Һ��һ������CO32-����ΪCO32?��Ag+��Mg2+��Ba2+������Ӧ�����ܹ��棬�����ɰ�ɫ�����ж���Һ��һ������SiO32-����ʵ����֪��Һ�в���SO42-������ȷ��NO3-�Ƿ���ڡ�
��1����ʵ����֪����������ϡ�������ɰ�ɫ�������ڱ�״���·ų����壬�����Һ��һ������CO32-��SiO32-����һ��û��Ag+��Mg2+��Ba2+��
��2��ʵ��I�����ɳ���ΪH2SiO3�����ɳ��������ӷ���ʽΪ��SiO32- + 2H+ === H2SiO3������SiO32-+ 2H+ + H2O === H4SiO4����
��3��NO3?����ȷ���Ƿ���ڣ���ʵ����֪��Һ�в���SO42-��CO32?��Ũ��Ϊ1.12L��22.4L/mol��0.1L=0.5mol?L?1������ķ�Ӧ���Һ���ˣ��Գ���ϴ�ӡ����������أ����ù���ΪSiO2����SiO32?��Ũ��Ϊ3.6g��60g/mol��0.1L=0.6mol?L?1��
��4�����ݵ���غ�2c��CO32-��+2c��SiO32-��=2��0.5mol/L+2��0.6mol/L=2.2mol/L��0.9mol/L�������Һ��һ������K+������Ũ������Ϊ1.3mol?L?1��
���㣺���⿼�����ӷ�Ӧ�����ӹ��桢���ӷ���ʽ����д����ѧ���㡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡ��ɽ�и���9�¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й�ͭпԭ���(��ͼ)��������ȷ����
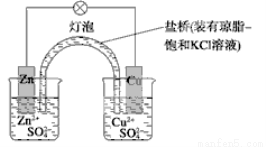
A��������ӦΪZn��2e��===Zn2+ B��ȡ�����ţ�ԭ����Կɹ���
C�������·�У����Ӵ��������� D����ط�ӦΪZn��Cu2+===Zn2+��Cu
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡ��ɽ�е���У����������һѧ�ڻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���������μ����ֽ��Ҳ���ϸ��ӡ�ijѧϰС����Mg(NO3)2Ϊ�о�������ͨ��ʵ��̽�����ȷֽ�IJ���������4�ֲ��룬���в��������ǣ� ��
A��Mg(NO3)2��NO2��O2 B��MgO��NO2��O2
C��Mg3N2��O2 D��MgO��NO2��N2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡ��У������ѧ�ڵ�һ���������ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
��16�֣���1��С���������о��¶ȶԷ�Ӧ���ʵ�Ӱ�족ʵ��ʱ����ȡ����ֻ�Թܣ�������4mL 0.01mol/L��KMnO4������Һ��2mL 0.1mol/L H2C2O4���Ҷ��ᣩ��Һ����A�Թ�������ˮ�У�B�Թ�������ˮ�У���¼��Һ��ɫ�����ʱ�䡣
����Ҫ�� ���ữKMnO4��Һ����ɫ����ʱ��tA tB���>������=����<������
��д���÷�Ӧ�����ӷ���ʽ ��
��2��ʵ������ƿ������ɳ���Ҷ�����Ʒ��С�����������Ӧ��ԭ�����ⶨ�京��������Ϊ��
������250 mL��Һ��ȷ����5.0g�Ҷ�����Ʒ�����250mL��Һ��
�ڵζ���ȷ��ȡ25.00mL������Һ����ƿ�У����������ữ����0.1000 mol��L-1 KMnO4��Һװ�� �����ʽ����ʽ�����ζ��ܣ����еζ���������ʵ���з��֣��յ�������KMnO4��Һʱ����ҺѸ�ٱ���Ϻ�ɫ������ƿҡ��һʱ����Ϻ�ɫ������ʧ���ټ����μ�ʱ���Ϻ�ɫ�ͺܿ���ɫ�ˡ������ԭ�� ����____ ��֤���ﵽ�ζ��յ㡣
�ۼ��㣺���ظ���������2�Σ���¼ʵ���������¡�
��� | �ζ�ǰ������mL�� | �ζ��������mL�� |
1 | 0.00 | 20.10 |
2 | 1.00 | 20.90 |
3 | 0.00 | 22.10 |
������KMnO4��Һ��ƽ�����Ϊ mL����֪H2C2O4����Է�������Ϊ90�������Ʒ�Ĵ���Ϊ ��
�������������в����ᵼ�²ⶨ���ƫ�ߵ���__________��
A δ�ñ�Ũ�ȵ�����KMnO4��Һ��ϴ�ζ���
B �ζ�ǰ��ƿ������ˮ
C �ζ�ǰ�ζ��ܼ��첿�������ݣ��ζ���������ʧ
D��С�Ľ���������KMnO4��Һ������ƿ��
E���۲����ʱ���ζ�ǰ���ӣ��ζ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡ��У������ѧ�ڵ�һ���������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A�����Ĵ�������һ������Ĺ̵���ʽ
B����ҵұ�������������AlCl3����
C�������ۼ���FeCl3��CuCl2�����Һ�У���ַ�Ӧ��ʣ��Ĺ����в�һ������
D���ü��ȷֽ�ķ����ɽ�NH4Cl�����Ca(OH)2����Ļ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ������ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����������ʵ������ͬһԭ�����͵���
A��Ũ�������ˮ����ɫ�Լ�ƿ����
B�����ƺ��������ƹ��峤�ڱ�¶�ڿ����б���
C�����������Ͳ���������Ũ����
D��SO2��Na2SO3��Һ����ʹ��ˮ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ������ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ǿ������ҺX�п��ܺ���Na+��K+��NH4+��Fe2+��A13+��CO32����SO32����SO42����
C1���е������֣�ijͬѧΪ��ȷ����ɷ֣�ȡX��Һ��������ʵ�飬ʵ����̼��������£�
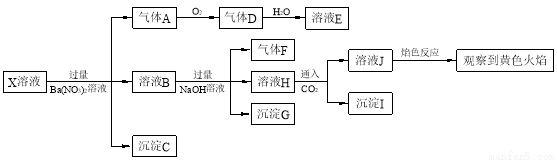
���н�����ȷ����
A��X�в���ȷ���������� A13+��Na+��K+��C1��
B������F����������ֱ����������D
C������Cһ����BaSO4�� ����Gһ����Fe(OH)3 ������Iһ����Al(OH )3
D��X�п϶�����Na+��Fe2+��A13+��NH4+��SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ������ѧ�ڵڶ����¿�������ѧ�Ծ��������棩 ���ͣ�ѡ����
��2molNaHCO3��һ������Na2O2�����ϣ��ڼ��ȵ�������ʹ�䷴Ӧ�����ⶨ��Na2O2ʣ�࣬��������ù�������ʵ�����n��Ϊ
A��1mol��n��2mol B��1mol��n��4mol C��2mol��n��4mol D��n��4mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��ɽ��ʡ�����и�����ѧ������������ѧ�Ծ���A���������棩 ���ͣ������
��5�֣���һ�����ĩ���ܺ���Na2CO3��NaCl��Na2SO4��CuCl2��Ba(NO3)2��K2CO3��K2SO4�е�һ�ֻ��֣��ְ����в������ʵ�顣
��1�����÷�ĩ����ˮ����ɫ��Һ�Ͱ�ɫ������
��2�����˳��ij����м���ϡ���ᣬ�в��ֳ����ܽ⣬ͬʱ������ɫ���塣
��3��ȡ��Һ����ɫ��Ӧ����֤����Һ�к�Na+������K+��
�����������ƶϣ�
��1���û������һ������ ��һ�������� ��
��2�����ܺ��� ����Ҫ�������Ƿ���ڣ�����β��� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com