
下列有关物质的性质与应用相对应的是
A.二氧化锰具有强氧化性,可用作H2O2分解的氧化剂
B.K2FeO4具有还原性,可用于自来水的杀菌消毒
C.Fe3+具有氧化性,可溶解印刷线路板上的金属铜
D.SO2具有漂白性,能使紫色KMnO4溶液褪色
科目:高中化学 来源:2017届河北省高三上学期9月月考化学试卷(解析版) 题型:选择题
如图W、X、Y、Z为四种物质,若箭头表示能一步转化的常见反应,其中能实现图示转化关系的是( )
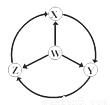
选项 | W | X | Y | Z |
A | S | SO2 | SO3 | H2SO4 |
B | Na | Na2O2 | NaOH | NaCl |
C | Fe | FeCl3 | Fe(OH)2 | FeCl2 |
D | Al | AlCl3 | NaAlO2 | Al2(SO4)3 |
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三暑假阶段性考试化学试卷(解析版) 题型:选择题
下列反应中的氨与反应4NH3 + 5O2 → 4NO + 6H2O中的氨作用相同的是( )
A.2Na + 2NH3 → 2NaNH2 + H2↑ B.2NH3 + 3CuO → 3Cu + N2 +3H2O
C.NH3+HCl=NH4Cl D.3SiH4 + 4NH3 → Si3N4 + 12H2
查看答案和解析>>
科目:高中化学 来源:2017届广西省桂林市高三上第二次月考化学试卷(解析版) 题型:填空题
高锰酸钾在不同的条件下发生的反应如下:
① MnO4-+5e-+8H+ ═ Mn2++4H2O
② MnO4-+3e-+2H2O ═ MnO2↓+4OH-
③ MnO4-+e- ═ MnO42- (溶液绿色)
⑴ 从上述三个半反应中可以看出高锰酸根离子被还原的产物受溶液的____________影响。
⑵ 将SO2通入高锰酸钾溶液中,发生还原反应的离子反应过程为 __________→___________。
⑶ 将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色。下列说法正确的是________。
a.氧化性:PbO2 > KMnO4 b.还原性:PbO2 > KMnO4 c.该反应可以用盐酸酸化
⑷ 将高锰酸钾逐滴加入到强碱性硫化钾溶液中发生如下反应,其中K2SO4和S的物质的量之比为3∶2,完成下列化学方程式(横线上填系数,括号内填物质),并用单线桥法表示电子的转移情况。
① _______KMnO4+_______K2S+_______( ) ═ ________K2MnO4+________K2SO4+________S↓+________( )。
② 若生成6.4g单质硫,反应过程中转移电子数为____________。
⑸ 已知在酸性溶液中,下列物质氧化KI时,自身发生如下变化:
MnO4-→Mn2+; Fe3+→Fe2+; IO3-→I2; HNO3→NO
如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是________。
a.MnO4- b.Fe3+ c.IO3- d.HNO3
查看答案和解析>>
科目:高中化学 来源:2017届广西省桂林市高三上第二次月考化学试卷(解析版) 题型:选择题
NA代表阿伏伽德罗常数的值。下列说法正确的是
A.标准状况下,22.4LCl2与足量的铁粉反应,转移的电子数为3NA
B.含23g钠元素的Na2O和Na2O2混合物中阴离子数目介于0.5NA和NA之间
C.在0℃、101kPa条件下,11.2L丁烷中含极性共价键数目为5NA
D.5NH4NO3 4N2↑+2HNO3 +9H2O中氧化产物比还原产物每多14g,转移电子数为15NA
4N2↑+2HNO3 +9H2O中氧化产物比还原产物每多14g,转移电子数为15NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一上第一次质检化学试卷(解析版) 题型:计算题
向50mL Na2SO4和Na2CO3的混合溶液中加入过量的BaCl2溶液,得到14.51g白色沉淀,向白色沉淀中加入过量的稀HNO3,充分反应后,沉淀减少到4.66g,并有气体产生。
(1)原混合溶液中Na2SO4的物质的量浓度是多少?
(2)产生的气体在标准状况下的体积是多少?
(3)原溶液中Na+物质的量浓度是多少?
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一上第一次质检化学试卷(解析版) 题型:选择题
把NaOH和Na2CO3混和物配制成100mL溶液,其中c(Na+)=0.5mol/L。在该溶液中加入过量盐酸反应完全后,将溶液蒸干后所得固体质量为
A、2.93 g B、5.85 g C、6.56g D、无法确定
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高二上9月月考化学卷(解析版) 题型:填空题
常温下,用0.1000 mol/L NaOH溶液分别滴定20.00 mL 0.1000 mol/L HCl溶液和20.00 mL 0.1000 mol/L CH3COOH溶液,得到2条滴定曲线,如下图所示。
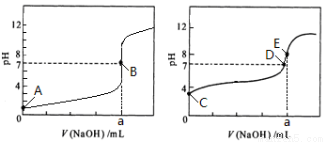
图1 图2
(1)CH3COOH的电离方程式是 ;
(2)由A、C点判断,滴定HCl溶液的曲线是 (填“图1”或“图2”),图像中a = mL;
(3)用NaOH溶液滴定CH3COOH时选用 做指示剂,当V(NaOH)=10.00 mL时,滴定CH3COOH所得溶液中的物料守恒式是 ;
(4)D点所示溶液中c(Na+) c(CH3COO-)(填“﹥”、“﹤”、“﹦”);
(5)E点对应的溶液pH﹥7,原因是 (用离子方程式表示),溶液中离子浓度由大到小的顺序为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上9月月考化学卷(解析版) 题型:选择题
Mg—AgCl电池是一种以海水为电解质溶液的水激活电池。下列叙述错误的是
A.负极反应式为Mg-2e-=Mg2+
B.正极反应式为Ag++e-=Ag
C.电池放电时Cl一由正极向负极迁移
D.负极会发生副反应 Mg+2H2O=Mg(OH)2+H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com