
| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |
分析 ①海水中盐类物质沸点高;
②铝热反应可冶炼高熔点金属;
③可能生成AgCl沉淀干扰硫酸根离子检验;
④浊液中加入足量MgCl2溶液,Ca(OH)2转化为更难溶Mg(OH)2.
解答 解:①海水中盐类物质沸点高,则用蒸馏的方法将海水淡化,故正确;
②铝热反应可冶炼高熔点金属,可用金属铝与V2O5在高温下冶炼矾,铝作还原剂,常温下不反应,故错误;
③可能生成AgCl沉淀干扰硫酸根离子检验,应先加盐酸无现象,再加氯化钡溶液检验溶液中是否含有SO42-,故错误;
④浊液中加入足量MgCl2溶液,Ca(OH)2转化为更难溶Mg(OH)2,充分反应后过滤,除去Ca(OH)2,故正确;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,涉及混合物分离提纯、铝热反应、离子检验及沉淀转化等,把握物质的性质、反应原理为解答的关键,注意实验的评价性分析,题目难度不大.


 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①② | B. | 只有①③ | C. | 只有②③ | D. | 只有①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
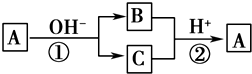 A是一种常见的单质,B、C为常见的化合物,A、B、C均含有元素X,它们有如图所示的转化关系(部分产物及反应条件已略去).下列说法正确的是( )
A是一种常见的单质,B、C为常见的化合物,A、B、C均含有元素X,它们有如图所示的转化关系(部分产物及反应条件已略去).下列说法正确的是( )| A. | 反应①和②互为可逆反应 | B. | X元素可能为铝 | ||
| C. | X元素可能是金属,也可能是非金属 | D. | 反应①和②一定为氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 升高温度,v(正)、v(逆)都增大,但v(正)增的更大 | |
| B. | 增大压强,v(正)、v(逆)都增大,但v(正)增的更大 | |
| C. | 增大A的浓度,v(正)会增大,但v(逆)会减小 | |
| D. | 采用适当催化剂(正),v(正)、v(逆)同时增大,而且增大的倍数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu溶于稀硝酸HNO3:Cu+2H++NO3-=Cu2++NO2↑+H2O | |
| B. | 在NaHSO4溶液中加Ba(OH)2至中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O | |
| C. | 向等物质的量浓度的NaOH和Na2CO3的混合液中加入稀盐酸:2OH-+CO32-+4H+=CO2↑+2H2O | |
| D. | 苏打溶液中加入稀HCl:CO32-+2H+=CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
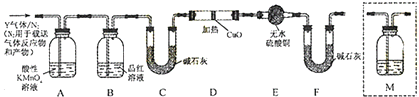
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com