
【题目】三硫代碳酸钠(Na2CS3)常用作杀菌剂、沉淀剂。某小组设计实验探究三硫代碳酸钠的性质并测定其溶液的浓度。
实验1:探究Na2CS3的性质
步骤 | 操作及现象 |
① | 取少量Na2CS3 固体溶于蒸馏水配制成溶液并分成两等份 |
② | 向其中一份溶液中滴加几滴酚酞试液,溶液变红色 |
③ | 向另一份溶液中滴加酸性KMnO4溶液,紫色褪去 |
(1)H2CS3是________酸(填“强”或“弱”)。
(2)已知步骤③的氧化产物是SO42-,写出该反应的离子方程式________________________。
实验2:测定Na2CS3溶液的浓度,按如图所示连接好装置,取100mLNa2CS3溶液置于三颈烧瓶中,打开仪器d的活塞,滴入足量2.0mol/L稀H2SO4,关闭活塞。
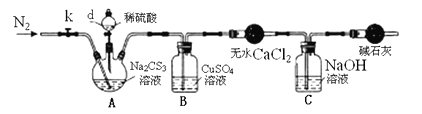
已知:Na2CS3 + H2SO4=Na2SO4 + CS2 + H2S↑。CS2和H2S均有毒。CS2不溶于水,沸点46℃,与CO2某些性质相似,与NaOH作用生成Na2COS2和H2O。
(3)盛放无水CaCl2的仪器的名称是____________。
(4)反应结束后打开活塞k,再缓慢通入热N2一段时间,其目的是___________________。
(5)为了计算Na2CS3溶液的浓度,对B中混合物进行过滤、洗涤、干燥、称重,得19.2g固体,则A中Na2CS3的物质的量浓度为____________________。
(6)分析上述实验方案,还可以通过测定C中溶液质量的增加值来计算Na2CS3溶液的浓度,若反应结束后将通热N2改为通热空气,计算值________(填“偏高”、“偏低”或“无影响”)。
【答案】弱 5CS32-+24MnO4-+52H+=5CO2↑+15SO42-+24Mn2++26H2O 干燥管 将装置中残留的H2S、CS2全部排入后续装置中,使其被完全吸收 2.0mol/L 偏高
【解析】
“有弱才水解”——依据酚酞变红色,判断H2CS3是弱酸。书写步骤③的离子方程式,要明确介质为酸性,所以C变为CO2,用H+配电荷守恒;反应结束后打开活塞k,再缓慢通入热氮气一段时间,显然是为了将装置中的残留的H2S、CS2等气体排入吸收装置,防止污染环境。
(1)根据溶液中滴加几滴酚酞试液,溶液变红色,说明Na2CS3为强碱弱酸盐,则H2CS3是弱酸;
(2)向Na2CS3溶液中滴加酸性KMnO4溶液,紫色褪去,氧化产物为SO42-,还原产物为Mn2+;则离子方程式为:5CS32-+24MnO4-+52H+=5CO2↑+15SO42-+24Mn2++26H2O;
(3)盛放无水CaCl2的仪器的名称是干燥管;
(4)装置中残留着一部分生成物,不将其完全排入后续装置会影响实验结果,通入惰性的热N2可将装置中残留的H2S、CS2全部排入后续装置中,使其被完全吸收;
(5)根据反应Na2CS3 + H2SO4=Na2SO4 + CS2 + H2S↑可知n(Na2CS3)=n(H2S),硫化氢与硫酸铜溶液反应生成硫化铜沉淀,n(CuS)=19.2g÷96g/mol=0.2mol,则A中Na2CS3的物质的量浓度为0.2mol/0.1L=2mol/L;
(6)空气中含有二氧化碳,能与氢氧化钠溶液反应生成碳酸钠,增加了C的重量,使实验结果偏高。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列关于甲、乙、丙、丁四种有机物说法正确的是
A.  与 NaOH的水溶液共热,反应后生成的醇能被氧化为醛
与 NaOH的水溶液共热,反应后生成的醇能被氧化为醛
B. CH3Cl中加入NaOH的水溶液共热,再滴入AgNO3溶液,可检验该物质中含有的卤素原子
C. 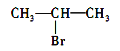 发生消去反应得到两种烯烃
发生消去反应得到两种烯烃
D. CH3Cl、 、
、 中加入 NaOH的醇溶液共热,然后加入稀硝酸呈酸性,再滴入AgNO3溶液,均有沉淀生成
中加入 NaOH的醇溶液共热,然后加入稀硝酸呈酸性,再滴入AgNO3溶液,均有沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用CH4与Cl2发生取代反应制取副产品盐酸的设想在工业上已成为现实,某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如图所示。根据要求填空:
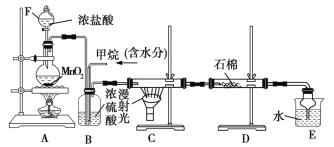
(1)实验室制取Cl2的化学反应方程式为__________。
(2)设V(Cl2)/V(CH4)=x,若理论上欲获得最多的HCl,则x的取值范围为____。
(3)B装置有三种功能:①控制气体流速;②将气体混合均匀;③___________。
(4)D装置中的石棉上吸附着KI饱和溶液及KI粉末,其作用是___________________。
(5)E装置的作用是____(填字母,双选)。
A.收集气体 B.吸收Cl2
C.防止倒吸 D.吸收HCl
(6)E装置制得的盐酸中还含有有机物,将两者分离的最佳方法为________。
(7)该装置还存在缺陷,原因是没有进行尾气处理,尾气的主要成分是____(填字母,双选)。
A.CH4 B.CH3Cl C.CH2Cl2 D.CHCl3 E.CCl4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钠常作漂白剂、杀菌剂、消毒剂。过氧化钠保存不当容易吸收空气中CO2而变质。
(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入__________溶液,充分振荡后有白色沉淀,证明Na2O2已经变质。
(2)该课外活动小组为了粗略测定过氧化钠的纯度,他们称取a g样品,并设计用下图装置来测定过氧化钠的质量分数。

①A中发生反应离子方程式为_____________________。
②将仪器连接好以后,必须进行的第一步操作是_____________________。
③B装置出来的气体是否需要干燥_________________。(填“是”或“否”)
④写出装置C中发生的所有反应的化学方程式_____________,______________。
⑤D中NaOH溶液的作用_______________________。
⑥实验结束时,读取实验中生成气体的体积时,不合理的是_______________。
a.直接读取气体体积,不需冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中水的体积
⑦读出量筒内水的体积后,折算成标准状况下氧气的体积为V mL,则样品中过氧化钠的质量分数为__________________。
⑧实验完成后E到F之间导管内残留水的体积会使测量结果__________。(填“偏大”、“偏小”或“不影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲配制480mL0.2mol·L-1的NaOH溶液。
(1)通过计算可知,应用托盘天平称量_____克NaOH固体。
(2)本实验所需要的玻璃仪器除量筒、胶头滴管、烧杯外还有_____。
(3)从下面选出所需的操作并写出正确的顺序_____(填字母)。
A.洗涤 B.冷却 C.量取 D.称量 E.定容 F.转移溶液 G.稀释 H.溶解
(4)在实验过程中出现如下情况对所配溶液的浓度有何影响(填“偏高”或“偏低”或“无影响”)。
①定容时加蒸馏水不慎超过了刻度_____;
②容量瓶不干燥,有一定的水分_____;
③定容时仰视观察到液面刚好到达刻度线_____。
(5)该NaOH溶液与2.24L氯气(STP)下恰好完全反应,需氢氧化钠溶液_____mL。
(6)用18mol·L-1的硫酸配制100mL1.0 mol·L-1硫酸,实验时应选用的仪器是_____(填编号)。
A.100mL量筒 B.托盘天平 C.玻璃棒 D.50mL容量瓶
E.10mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数的数值为NA,则下列说法正确的是( )
A. 常温常压下,11.2 L甲烷中含有的氢原子数为2NA
B. 标准状况下,0.3 mol二氧化硫中含有的氧原子数为0.3×6.02×1023
C. 标准状况下,2.7 g Al与足量的盐酸反应,生成H2的体积是22.4L
D. 常温下,1 L 0.1 mol·L-1MgCl2溶液中含Cl-数为0.2moL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示物质相互转换关系:

试回答:
(1)写出B的化学式____________、C溶液是______________。
(2)写出由E转变成F发生反应的化学方程式_______________。
(3)鉴别G溶液中阳离子的操作方法及实验现象:__________________。
(4)向G溶液中加入A的离子方程式____________________。
(5)写出D溶液中加入AgNO3得到白色沉淀的离子方程式__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ca(ClO)2与浓盐酸反应会生成Cl2,该反应的化学方程式为Ca(ClO)2+4HCl(浓)===CaCl2+2Cl2↑+2H2O
(1)浓盐酸在反应中显示出来的性质是_____(填写字母)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)产生0.3 mol Cl2,则转移的电子的物质的量为______mol。
(3)用双线桥法表示该氧化还原反应中电子转移的方向和数目_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三种气体X、Y、Z的相对分子质量关系为Mr(X) < Mr(Y)= 0.5Mr(Z),下列说法正确的是()
A.原子数目相等的三种气体,质量最大的是Z
B.相同条件下,同质量的三种气体,气体密度最小的是X
C.若一定条件下,三种气体体积均为2.24 L,则它们的物质的量一定均为0.1 mol
D.同温下,体积相同的两容器分别充2gY气体和1gZ气体,则其压强比为2:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com