
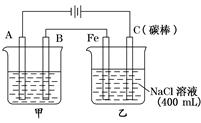
 ,则乙池中阳极放出的气体在标准状况下的体积为
,则乙池中阳极放出的气体在标准状况下的体积为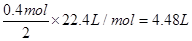 ;产生OH-有0.4mol,若此时乙池剩余液体为400 mL,则电解后得到碱液的物质的量浓度为
;产生OH-有0.4mol,若此时乙池剩余液体为400 mL,则电解后得到碱液的物质的量浓度为 。
。

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题
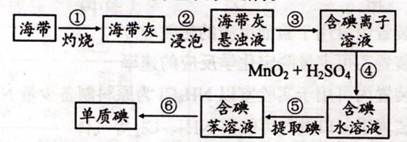
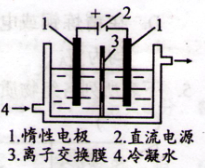
| 实验操作 | 实验现象及结论 |
| | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.溶液的浓度变为0.08 mol·L-1 | B.阳极上产生112 mL O2(标准状况) |
| C.转移的电子数是1.204×1023 | D.反应中有0.02 mol的Ag被氧化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
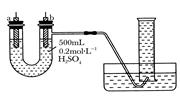
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电解池中的闭合回路仅是由电子的定向运动形成的 |
| B.电子由电源的负极流向电解池的阳极,从电解池的阴极流向电源的正极 |
| C.在电解质溶液中,阴离子向阴极移动,阳离子向阳极移动 |
| D.相同时间内阳离子在阴极得到的电子与阴离子在阳极失去的电子数相等 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
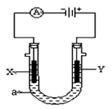
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.装置甲中对于铁闸门的保护用的是“牺牲阳极的阴极保护法”,焊接在铁闸上的金属R可以是锡块 |
| B.装置乙中对于铁闸门的保护采用的是“外加电流的阴极保护法”,铁闸门应与直流电源的负极相连 |
| C.装置丙可实现电解精炼铜,电极A的材料用纯铜,电极B的材料用粗铜 |
| D.装置丁可实现镀铜,铜片接在电源的正极,待镀金属接在电源的负极,X溶液应用含有待镀金属阳离子的溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Na2S4+3NaBr。闭合开关K时,b极附近先变红色。下列说法正确的是
Na2S4+3NaBr。闭合开关K时,b极附近先变红色。下列说法正确的是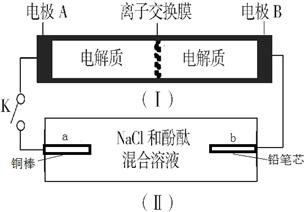
| A.当有0.01 mol Na+通过离子交换膜时,b电极上析出标准状况下的气体112 mL |
B.负极反应为4Na 4e-=4Na+ 4e-=4Na+ |
| C.闭合K后,b电极附近的pH变小 |
| D.闭合K后,a电极上有产生氢气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com