
25 ℃时,下列各组离子在指定溶液中一定能大量共存的是
A.0.1 mol·L-1NH4HCO3溶液:K+、Na+、SO42-、OH-
B.能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3-
C.0.1 mol·L-1CH3COONa溶液:Mg2+、H+、Cl-、SO42-
D.Kw/c(H+)=0.1 mol·L-1的溶液:Na+、K+、SiO32-、NO3-
科目:高中化学 来源:2014-2015四川省邛崃市高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列化合物中,阳离子半径与阴离子半径比值最小的是
A.NaF B.NaCl C.MgI2 D.KBr
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东茂名市高三第二次高考模拟考试理综化学试卷(解析版) 题型:填空题
(15分)二甲醚具有优良的燃烧性能,被称为21世纪的“清洁能源”,以下为其中一种合成二甲醚的方法:在一定温度、压强和催化剂作用下,在同一反应器中进行如下反应:
①CO2(g)+3H2(g) CH3OH(g) +H2O(g) △H1=-49.1 kJ·mol-1
CH3OH(g) +H2O(g) △H1=-49.1 kJ·mol-1
②2CH3OH(g) CH3OCH3(g)+H2O(g) △H2=-24.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-24.5 kJ·mol-1
③CO2(g)+H2(g) CO(g)+H2O(g) △H3=+ 41.2 kJ·mol-1
CO(g)+H2O(g) △H3=+ 41.2 kJ·mol-1
(1)写出CO2(g)加H2(g)转化为CH3OCH3(g)和H2O(g)的热化学方程式是 。
(2)一定条件下,原料气中n(H2)/n(CO2)比值和温度对CO2转化率影响的实验数据如下图。
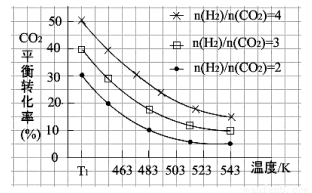
①温度为T1 K时,在1 L反应容器中投入2mol CO2 和8mol H2进行反应,试计算达到平衡时CO2的浓度为 。
②结合数据图,归纳CO2平衡转化率受外界条件影响的变化规律:
a 。
b 。
(3)为研究初始投料比与二甲醚产率关系,在一定温度和压强下,投入一定物质的量的H2、CO、CO2进行试验,实验发现二甲醚的平衡产率随原料气中n(CO)/〔n(CO)+n(CO2)〕比值增大而增大,试分析其原因 。
(4)下图是科学家现正研发的,以实现反应①在常温常压下进行的装置。
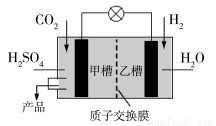
写出甲槽的电极反应 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三第二次模拟考试化学试卷(解析版) 题型:选择题
利用I2O5可消除CO污染,反应为5CO(g)+I2O5(s) 5CO2(g)+I2(s);ΔH。不同温度(T1、T2)下,向装有足量I2O5固体的2 L恒容密闭容器中通入2 mol CO,测得CO2气体体积分数φ(CO2)随时间t变化曲线如图所示。下列说法正确的是
5CO2(g)+I2(s);ΔH。不同温度(T1、T2)下,向装有足量I2O5固体的2 L恒容密闭容器中通入2 mol CO,测得CO2气体体积分数φ(CO2)随时间t变化曲线如图所示。下列说法正确的是
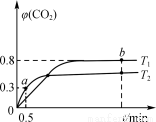
A.T1<T2,ΔH>0
B.T1温度下,该反应的平衡常数为1 024
C.T2温度下,0~0.5 min内,CO的平均反应速率为0.3 mol·L-1·min-1
D.T1温度下,若向装有足量I2固体的2 L恒容密闭容器中通入10 mol CO2,达到平衡时,φ(CO2)=0.8
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三第二次模拟考试化学试卷(解析版) 题型:选择题
下列各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是
物质 组别 | 甲 | 乙 | 丙 |
A | SO2 | Ba(OH)2 | NaHCO3 |
B | Na2O2 | H2O | CO2 |
C | Na2SiO3 | NaOH | HCl |
D | Al | H2SO4 | NaOH |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市河北区高三总复习质量检测一化学试卷(解析版) 题型:填空题
(18分)Ⅰ.有机物A的结构简式为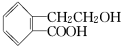 ,它可通过不同化学反应分别制得B、C和D三种物质。
,它可通过不同化学反应分别制得B、C和D三种物质。

(1)B中含氧官能团的名称是________。
(2)A →C的反应类型是________;A~D中互为同分异构体的是________。
(3)由A生成B的化学方程式是______________________________________。
Ⅱ.某芳香族化合物H常用作防腐剂,H可利用下列路线合成:
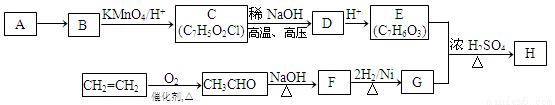
已知:①A是相对分子质量为92的烃;
②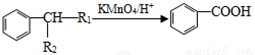
③ (-R1、-R2表示氢原子或烃基);
(-R1、-R2表示氢原子或烃基);
④D的核磁共振氢谱表明其有两种不同化学环境的氢(两种不同位置的氢原子),且峰面积之比为1:1。
回答下列问题:
(1)A的分子式为___________。
(2)同时符合下列条件的E的同分异构体共有____________种。
①分子中含有苯环
②能发生银镜反应
③能与FeCl3溶液发生显色反应
(3)检验F中含氧官能团的试剂为____________(填试剂名称),由F→G的反应类型为______。
(4)H的结构简式为_____________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市河北区高三总复习质量检测一化学试卷(解析版) 题型:选择题
生活中的一些问题常涉及到化学知识,下列叙述不正确的是
A.维生素C具有还原性,在人体内起抗氧化作用
B.“加碘食盐”、“含氟牙膏”、“富硒营养品”、“高钙牛奶”、“加铁酱油”等等,这里的碘、氟、硒指的是分子,钙、铁则分别是钙离子和铁离子
C.日本大地震后,防疫人员在震区周围撒石灰,进行环境消毒,防止灾后出现疫情
D.为防止中秋月饼等富脂食品氧化变质,常在包装袋中放入硫酸亚铁
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省常德市高三模拟考试理综化学试卷(解析版) 题型:填空题
2015年3月,全国“两会”代表委员就我国“雾霾”治理积极建言献策。科学家研究表明氮氧化物与悬浮在大气中的盐粒子相互作用时能产生“二次雾霾”,涉及的反应有:
2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) K1 (Ⅰ)
NaNO3(s)+ClNO(g) K1 (Ⅰ)
2NO(g)+Cl2(g) 2ClNO(g) K2 (Ⅱ)
2ClNO(g) K2 (Ⅱ)
回答下列问题:
(1)写出反应(Ⅰ)的平衡常数表达式K1 = 。
(2)恒温恒容条件下,反应(Ⅱ)达到平衡的标志是 。
a.体系压强保持不变
b.混合气体颜色保持不变
c.NO和ClNO的物质的量相等
d.每消耗0.1 mol NO的同时消耗0.05 mol Cl2
(3)为研究不同条件对反应(Ⅱ)的影响,恒温时向2 L密闭容器中加入 0.2 mol NO和0.1mol Cl2:
①在恒容条件下反应10 min达到平衡,测得10 min内v(ClNO)=7.5×10-3 mol·L-1·min-1,
则NO的平衡转化率α1= 。
②在恒压条件下建立平衡时NO的转化率为α2,则α2 α1(填“>”“<”
或“=”),平衡常数K2 (填“增大”、“减小”或“不变”)。
(4)工业上可通过电解NO制备NH4NO3,其工作原理如图所示,阴极反应式为 ;为使电解产物全部转化为NH4NO3,需补充气体物质A,A的化学式是_________。

(5)NO2可助偏二甲肼(C2H8N2)燃烧,产生的巨大能量能把火箭送入太空。已知6.0g液态偏二甲肼与液态NO2完全反应生成N2、CO2、H2O(g)放出225.0kJ的热量。写出该反应的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省邛崃市高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列离子的检验不能达到预期目的是
A.向待测液里加入NaOH溶液,加热,将湿润的红色石蕊试纸放在试管口变蓝,则待测液中肯定含有NH4+
B.用铂丝蘸取待测液在火焰上灼烧,若火焰呈黄色,则表明待测液中肯定含有Na+
C.向待测液里加入过量硝酸无现象,再加入硝酸银溶液,若无沉淀生成,则表明待测液中肯定不含Cl-
D.向待测液里加入BaCl2溶液,若产生白色沉淀,再加入过量稀硝酸白色沉淀不溶解,则表明待测液中肯定含有SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com