
| A.混合溶液中由水电离出的c(OH一)=1×10—8mol·L-。 |
| B.c(Na+)=c(X一)+c(HX)=0.2 mol·L- |
| C.c(Na+)一c(X一)=9.9×10-7mol·L- |
| D.c(OH一)一c(HX)=c(H+)=1×lO一6mol·L一 |
 HX+OH?,c(HX)=C(OH?)-c(H+)= 1×10-6mol·L-1—1×10-8mol·L-1=9.9×10-7mol·L-1,c(Na+)一c(X一)=c(HX)=9.9×10-7mol·L-1,正确;D、pH=8,则c(H+)= 1×10-8mol,错误。
HX+OH?,c(HX)=C(OH?)-c(H+)= 1×10-6mol·L-1—1×10-8mol·L-1=9.9×10-7mol·L-1,c(Na+)一c(X一)=c(HX)=9.9×10-7mol·L-1,正确;D、pH=8,则c(H+)= 1×10-8mol,错误。

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
| V2O5 |
| △ |
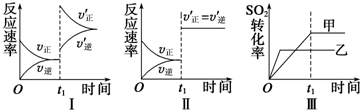
| A.图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响 |
| B.图Ⅱ表示的是t1时刻加入催化剂后对反应速率的影响 |
| C.图Ⅲ表示的是催化剂对化学平衡的影响,且甲的催化效率比乙高 |
| D.图Ⅲ表示的是压强对化学平衡的影响,且乙的压强较高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.强电解质的水溶液中不存在溶质分子,弱电解质的水溶液中存在溶质分子和离子 |
| B.强电解质的水溶液导电性强于弱电解质的水溶液 |
| C.强电解质都是离子化合物,弱电解质都是共价化合物 |
| D.强电解质易溶于水,弱电解质难溶于水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 酸 | c(一元酸) /mol·L–1 | c(NaOH) /mol·L–1 | 混合溶液的pH |
| HX | 0.1 | 0.1 | pH = x |
| HY | 0.1 | 0.1 | pH = 7 |
| HZ | 0.1 | 0.1 | pH = 9 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温下,0.1 mol·L-1 CH3COOH溶液的pH=1 |
| B.铅蓄电池在放电过程中,负极质量增加,正极pH减少 |
| C.反应CO2(g)+C(s)=2CO(g)在低温下不能自发进行,则其△H>0 |
| D.常温下,向AgCl浊液中加入少量NaCl饱和溶液,则c(Ag+)、Ksp(AgCl)均减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.pH=5的H2S溶液中,c(H+)= c(HS-)=1×10—5 mol·L—1 |
| B.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 |
| C.pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合: c(Na+)+ c(H+)= c(OH-)+c( HC2O4-) |
| D.pH相同的①CH3COO Na②NaHCO3③NaClO三种溶液的c(Na+):①>②>③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.生成了一种强酸弱碱盐 | B.弱酸溶液和强碱溶液反应 |
| C.强酸溶液和弱碱溶液反应 | D.一元强酸溶液和一元强碱溶液反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com