
 N2(g)+2CO2(g) △H=-a kJ·mol-1。
N2(g)+2CO2(g) △H=-a kJ·mol-1。
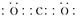 (1分)
(1分) N2(g)+4CO2(g) △H="-a+b-2c" kJ·mol-1。 (3分,方程式及状态2分,焓变1 分)
N2(g)+4CO2(g) △H="-a+b-2c" kJ·mol-1。 (3分,方程式及状态2分,焓变1 分)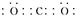 。
。 N2(g)+2CO2(g) △H=-a kJ·mol-1 ①
N2(g)+2CO2(g) △H=-a kJ·mol-1 ①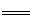 CO2(g) △H=-c kJ·mol-1 ③
CO2(g) △H=-c kJ·mol-1 ③ N2(g)+4CO2(g) △H="-a+b-2c" kJ·mol-1。
N2(g)+4CO2(g) △H="-a+b-2c" kJ·mol-1。 N2(g)+2CO2(g)
N2(g)+2CO2(g) 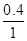 ×100%=40%;0~15min NO的平均速率v(NO)=
×100%=40%;0~15min NO的平均速率v(NO)=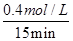 =0.027mol/(L·min)。化学平衡常数K=
=0.027mol/(L·min)。化学平衡常数K=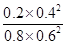 =0.14。
=0.14。 N2(g)+2CO2(g)
N2(g)+2CO2(g) 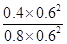 =0.625>0.14,所以逆向移动;化学平衡常数只和温度有关,温度不变,平衡常数不变,所以化学平衡常数还是
=0.625>0.14,所以逆向移动;化学平衡常数只和温度有关,温度不变,平衡常数不变,所以化学平衡常数还是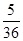 L/mol或0.14 L/mol。
L/mol或0.14 L/mol。

科目:高中化学 来源:不详 题型:填空题
 CH3OH(g) ΔH1=-90 kJ·mol-1
CH3OH(g) ΔH1=-90 kJ·mol-1 CO2(g)+H2(g)ΔH2=-41 kJ·mol-1
CO2(g)+H2(g)ΔH2=-41 kJ·mol-1
 CO2(g)+H2(g)的平衡常数K=0.32,在该温度下,已知c始(CO)=1 mol·L-1,c始(H2O)=1 mol·L-1,某时刻经测定CO的转化率为10%,则该反应________(填“已经”或“没有”)达到平衡,原因是_________________________________________________
CO2(g)+H2(g)的平衡常数K=0.32,在该温度下,已知c始(CO)=1 mol·L-1,c始(H2O)=1 mol·L-1,某时刻经测定CO的转化率为10%,则该反应________(填“已经”或“没有”)达到平衡,原因是_________________________________________________查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO2(g) + H2(g),反应过程中各物质的浓度如右图t1前所示变化。若保持温度不变,t2时再向容器中充入CO、H2各1mol,平衡将 移动(填“向左”、 “向右”或“不”)。t2时,若改变反应条件,导致H2浓度发生如右图t2后所示的变化,则改变的条件可能是 (填符号)。
CO2(g) + H2(g),反应过程中各物质的浓度如右图t1前所示变化。若保持温度不变,t2时再向容器中充入CO、H2各1mol,平衡将 移动(填“向左”、 “向右”或“不”)。t2时,若改变反应条件,导致H2浓度发生如右图t2后所示的变化,则改变的条件可能是 (填符号)。


查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3CH2OH(g)+3H2O(g) ΔH1
CH3CH2OH(g)+3H2O(g) ΔH1 CO(g)+3H2(g) ΔH2
CO(g)+3H2(g) ΔH2| A.增大压强 | B.加催化剂 | C.增大CO2的浓度 | D.及时分离体系中的乙醇 |
 CO2(g)+H2(g) ΔH3
CO2(g)+H2(g) ΔH3 H1、
H1、 H3表示)。
H3表示)。
 H2________0(填“>”、“=”或“<”)。某温度下,向容积为1 L的密闭容器中加入1 mol甲烷和1mol水蒸气,经过5h反应达到平衡状态,此时测得CH4的浓度变为0.5 mol/L。该温度下,反应(ii)的平衡常数K=__________________,反应开始至达到平衡时氢气的反应速率v(H2)=_________。
H2________0(填“>”、“=”或“<”)。某温度下,向容积为1 L的密闭容器中加入1 mol甲烷和1mol水蒸气,经过5h反应达到平衡状态,此时测得CH4的浓度变为0.5 mol/L。该温度下,反应(ii)的平衡常数K=__________________,反应开始至达到平衡时氢气的反应速率v(H2)=_________。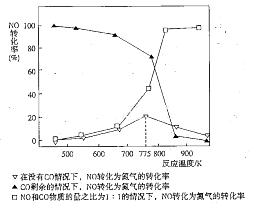
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
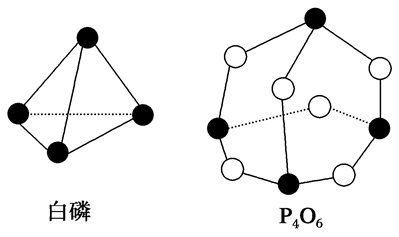
| A.-1638kJ/mol | B.+1638kJ/mol |
| C.-126kJ/mol | D.+126kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 H2(g)+CO2(g) ΔH2;
H2(g)+CO2(g) ΔH2; CO(g)+H2(g) ΔH3;
CO(g)+H2(g) ΔH3; 2CO(g)+4H2O(g)
2CO(g)+4H2O(g)查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
| 键能/kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
 ”表示硅晶体中的一个原子,请在立方体的顶点用“
”表示硅晶体中的一个原子,请在立方体的顶点用“ ”表示出与之紧邻的硅原子。
”表示出与之紧邻的硅原子。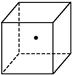
 Si(s)+4HCl(g),该反应的反应热ΔH= kJ/mol。
Si(s)+4HCl(g),该反应的反应热ΔH= kJ/mol。 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
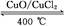 2Cl2+2H2O
2Cl2+2H2O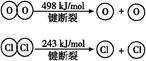
| A.反应A的ΔH>-115.6 kJ/mol |
| B.断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为32 kJ |
| C.H2O中H—O键比HCl中H—Cl键弱 |
| D.由Ⅱ中的数据判断氯元素的非金属性比氧元素强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2NH3(g) ?H=bkJ/mol,其化学平衡常数K与温度的关系如下:
2NH3(g) ?H=bkJ/mol,其化学平衡常数K与温度的关系如下:| 温度/℃ | 200 | 300 | 400 |
| K | 1.0 | 0.86 | 0.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com