
| 周期/族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ○ |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
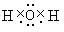 .
.分析 由元素在周期表中位置,可知①为C、②为N、③为O、④为F、⑤为Na、⑥为Mg、⑦为Al、⑧为Si、⑨为P、⑩为S、⑪为Cl、⑫为Ar.
(1)同周期自左而右元素非金属性增强、同主族自上而下元素非金属性减弱,稀有气体的化学性质最稳定;
(2)上述元素的最高价氧化物的对应水化物中高氯酸的酸性最强;能形成的两性氢氧化物是氢氧化铝;
(3)同周期自左而右原子半径减小;③形成的氢化物为H2O,分子中O原子与H原子之间形成1对共用电子对;
(4)⑥、⑩的最高价氧化物分别为氧化镁、Cl2O7,前者属于离子化合物,后者为非金属氧化物,属于共价化合物;
(5)同周期自左而右金属性减弱,可以利用金属与水的反应进行验证.
解答 解:由元素在周期表中位置,可知①为C、②为N、③为O、④为F、⑤为Na、⑥为Mg、⑦为Al、⑧为Si、⑨为P、⑩为S、⑪为Cl、⑫为Ar.
(1)同周期自左而右元素非金属性增强、同主族自上而下元素非金属性减弱,故F元素非金属性最强,稀有气体Ar的最外层为稳定结构,化学性质最稳定,
故答案为:F;Ar;
(2)上述元素的最高价氧化物的对应水化物中HClO4的酸性最强;Al元素能形成的两性氢氧化物--氢氧化铝,
故答案为:HClO4;Al;
(3)同周期自左而右原子半径减小,故从⑤到⑪的元素中Cl原子半径最小,③形成的氢化物为H2O,分子中O原子与H原子之间形成1对共用电子对,电子式为: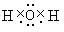 ,
,
故答案为:Cl;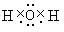 ;
;
(4)⑥、⑩的最高价氧化物分别为氧化镁、Cl2O7,前者属于离子化合物,后者为非金属氧化物,属于共价化合物,
故答案为:离子;共价;
(5)同周期自左而右金属性减弱,故Na比Mg更活泼,可以利用金属与水的反应进行验证:取少量金属钠和金属镁,都投入冷水中,金属钠和冷水剧烈反应,生成无色气体,钠迅速消失. 而镁和冷水几乎不反应,无明显现象,证明了金属钠比金属镁活泼,
故答案为:Na;取少量金属钠和金属镁,都投入冷水中,金属钠和冷水剧烈反应,生成无色气体,钠迅速消失. 而镁和冷水几乎不反应,无明显现象,证明了金属钠比金属镁活泼.
点评 本题考查元素周期表与元素周期律,比较基础,熟练掌握元素周期表的结构,注意金属性与非金属性强弱比较实验事实.


科目:高中化学 来源: 题型:解答题
 以下元素均为短周期元素:
以下元素均为短周期元素:| 元素代号 | 相关信息 |
| M | 非金属元素,其气态氢化物的水溶液呈碱性 |
| A | A的单质能与冷水剧烈反应,得到强碱性溶液 |
| B | B的原子最外层电子数是其内层电子数的三倍 |
| C | 在第三周期元素中,C的简单离子半径最小 |
| D | A、B、D组成的36电子的化合物X是常用消毒剂的主要成分 |
| E | 所有有机物中都含有E元素 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | |||
| z | W | Q |
| A. | Y元素气态氢化物的稳定性大于X元素的气态氢化物 | |
| B. | 形成的简单离子半径:W>Q>Z>X | |
| C. | Q的最高价氧化物对应的水化物酸性最强 | |
| D. | X的最高价氧化物对应的水化物与其氢化物形成的化合物中含有离子键和共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向10mL浓度为0.1mol•L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中水的电离程度始终增大 | |
| B. | 0.01mol•L-1CH3COOH溶液中水的电离程度小于0.01mol•L-1盐酸中水的电离程度 | |
| C. | 将0.01mol•L-1盐酸与pH=12的氨水等体积混合,所得溶液中由水电离出的c(OH-)<1×10-7mol•L-1 | |
| D. | 将0.01mol•L-1的CH3COOH溶液与pH=12的氨水等体积混合,所得溶液中由水电离出的c(OH-)>1×10-7mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
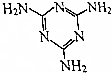 三聚氰胺的结构式如图所示,尿素[CO(NH2)2]在一定条件下发生分解反应可制得三聚氰胺和CO2等物质,下列说法不正确的是( )
三聚氰胺的结构式如图所示,尿素[CO(NH2)2]在一定条件下发生分解反应可制得三聚氰胺和CO2等物质,下列说法不正确的是( )| A. | 三聚氰胺的分子式为C3H6N6 | |
| B. | 氰胺的结构简式为H2N-C≡N | |
| C. | 尿素分解制三聚氰胺时,除生成CO2外,还会生成NH3 | |
| D. | 三聚氰胺属于高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  设计铜锌原电池 | B. |  制备氢氧化亚铁并观察其颜色 | ||
| C. | 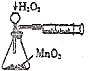 定量测定H2O2的分解速率 | D. | 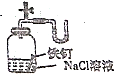 证明铁生锈与空气有关 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com