
ŌŚČŻ»żĪŖ2 LµÄ ĆܱÕČŻĘ÷ÖŠ£¬±£³ÖĢåĻµÄŚĪĀ¶Č800 ”ę²»±ä£¬½«Ņ»¶ØĮæµÄNOŗĶO2»ģŗĻ·¢Éś·“Ó¦£ŗ
ĆܱÕČŻĘ÷ÖŠ£¬±£³ÖĢåĻµÄŚĪĀ¶Č800 ”ę²»±ä£¬½«Ņ»¶ØĮæµÄNOŗĶO2»ģŗĻ·¢Éś·“Ó¦£ŗ
2NO£«O22NO2£¬ĘäÖŠNOµÄĪļÖŹµÄĮæ(n)Ėꏱ¼ä(t)µÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾”£Ēė»Ų“šĻĀĮŠĪŹĢā”£
£Ø1£©30 sŹ±·“Ó¦“ļµ½Ę½ŗā£¬ÓĆO2±ķŹ¾“ļµ½Ę½ŗā¹ż³ĢµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ
________£¬Ķ¼ĻńÖŠĒśĻß______ __(Ń”Ģī”°¢ń”±»ņ”°¢ņ”±)±ķŹ¾NO2µÄ±ä»Æ”£ÓÉĶ¼ĻńÖŠĒśĻßŗĶŹż¾Ż±ä»Æ£¬ÄÜ·ń¼ĘĖćøĆĪĀ¶ČĻĀµÄĘ½ŗā³£Źż£ŗ____________(Ģī”°ÄÜ”±»ņ”°²»ÄÜ”±)”£
__(Ń”Ģī”°¢ń”±»ņ”°¢ņ”±)±ķŹ¾NO2µÄ±ä»Æ”£ÓÉĶ¼ĻńÖŠĒśĻßŗĶŹż¾Ż±ä»Æ£¬ÄÜ·ń¼ĘĖćøĆĪĀ¶ČĻĀµÄĘ½ŗā³£Źż£ŗ____________(Ģī”°ÄÜ”±»ņ”°²»ÄÜ”±)”£
£Ø2£©ČōÉżøß·“Ó¦ĢåĻµµÄĪĀ¶Č£¬Ź¹·“Ó¦ÖŲŠĀ“ļµ½Ę½ŗā£¬“ĖŹ±ĢåĻµÖŠn(NO)£½n(NO2)£¬ŌņøĆ·“Ó¦ŹĒ________ČČ·“Ó¦(Ń”Ģī”°Īü”±»ņ”°·Å”±)”£
£Ø3£©ŌŚ800 ”ꏱ£¬ČōĖõŠ”ČŻĘ÷µÄĢå»ż£¬“ļŠĀĘ½ŗāŹ±n(NO)________(Ń”Ģī”°>”±”¢”°£½”±»ņ”°<”±)0.07 mol£¬NOµÄ×Ŗ»ÆĀŹ________(Ń”Ģī”°Ōö“ó”±”¢”°²»±ä”±»ņ”°¼õŠ””±)”£
£Ø4£©ÉĻŹö800 ”ꏱµÄ·“Ó¦“ļµ½Ę½ŗāŹ±²āµĆ·Å³öČČĮæa kJ”£ŹŌŠ“³öŌŚ“ĖĢõ¼žĻĀNOÓėŃõĘų·“Ó¦µÄČČ»Æѧ·½³ĢŹ½________________________________________ __________________________”£
__________________________ӣ
 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¶Ō“¦ÓŚĘ½ŗāדĢ¬µÄ·“Ó¦2A£Øg£©+B(g) 2C(g) ”÷H<0£¬ĻĀ
2C(g) ”÷H<0£¬ĻĀ
ĮŠŠšŹöÕżČ·µÄŹĒ
A£®Ōö“óAÅØ¶ČµÄĖ²¼ä£¬VÕż Ōö“ó£¬VÄę²»±ä B£®ÉżøßĪĀ¶Č£¬VÕż ¼õŠ”£¬VÄęŌö“ó
C£®Ōö“óŃ¹Ēæ. VÕż Ōö“ó£¬VÄę ¼õŠ” D£®¼ÓČė“߻ƼĮ£¬VÕż”¢VÄę ¶¼Ōö“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓĆCOŗĻ³É¼×“¼£ØCH3OH£©
µÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖCO(g)+2H2(g) CH3OH(g) £¬”÷H£¼0
CH3OH(g) £¬”÷H£¼0
°“ÕÕĻąĶ¬µÄĪļÖŹµÄĮæĶ¶ĮĻ£¬²āµÄCOŌŚ²»Ķ¬ĪĀ¶ČĻĀµÄĘ½ŗā×Ŗ»ÆĀŹÓėŃ¹ĒæµÄ¹ŲĻµČēÓŅĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕż
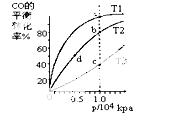 Č·µÄŹĒ( )
Č·µÄŹĒ( )
A£®Ę½ŗā³£Źż£ŗK(a)£¾K(c) K(b)£½K(d)
B£®Õż·“Ó¦ĖŁĀŹ£ŗv(a)£¾v(c) v(b)£¾v(d)
C£®Ę½¾łÄ¦¶ūÖŹĮæ£ŗM(a)£¼M(c) M(b)£¾M(d)
D£®Ę½ŗāŹ±aµćŅ»¶ØÓŠn(CO)£ŗn(H2)£½1:2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚŅ»¶ØĪĀ¶ČĻĀµÄÄ³ČŻ»ż²»±äµÄĆܱÕČŻĘ÷ÖŠ£¬½ØĮ¢ĻĀĮŠ»ÆŃ§Ę½ŗā£ŗC(s)£«H2O(g)  CO(g)£«H2(g)²»ÄÜČ·¶ØÉĻŹöæÉÄę·“Ó¦ŌŚŅ»¶ØĢõ¼žĻĀŅŃ“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŹĒ
CO(g)£«H2(g)²»ÄÜČ·¶ØÉĻŹöæÉÄę·“Ó¦ŌŚŅ»¶ØĢõ¼žĻĀŅŃ“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŹĒ
A£®ĢåĻµµÄŃ¹Ēæ²»ŌŁ·¢Éś±ä»Æ
B£®vÕż(CO)£½vÄę(H2O)
C£®Éś³Én mol COµÄĶ¬Ź±Éś³Én mol H2
D£®1 mol H—H¼ü¶ĻĮѵÄĶ¬Ź±¶ĻĮŃ2 mol H—O¼ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻņŅ»ČŻ»żĪŖ1L µÄĆܱÕČŻĘ÷ÖŠ¼ÓČėŅ»¶ØĮæµÄX”¢Y£¬
·¢Éś»Æѧ·“Ó¦aX(g)£«2Y(s)  bZ(g) ”÷H£¼0”£ĻĀĶ¼ŹĒČŻĘ÷ÖŠX”¢ZµÄĪļÖŹµÄĮæÅضČĖꏱ¼ä±ä»ÆµÄĒśĻß”£
bZ(g) ”÷H£¼0”£ĻĀĶ¼ŹĒČŻĘ÷ÖŠX”¢ZµÄĪļÖŹµÄĮæÅضČĖꏱ¼ä±ä»ÆµÄĒśĻß”£
øł¾ŻŅŌÉĻŠÅĻ¢ÅŠ¶Ļ£¬ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
A£®ÓĆX±ķŹ¾0~ 10minÄŚøĆ·“Ó¦µÄĘ½¾łĖŁĀŹĪŖv(X)£½0.045mol/£ØL·min£©
10minÄŚøĆ·“Ó¦µÄĘ½¾łĖŁĀŹĪŖv(X)£½0.045mol/£ØL·min£©
B£®»Æѧ·½³ĢŹ½ÖŠa:b£½ 1:3£¬
C£®ĶĘ²āŌŚµŚ7minŹ±ĒśĻß±ä»ÆµÄŌŅņæÉÄÜŹĒŌö¼ÓXµÄÅضČ
D£®ĶĘ²āøĆ·“Ó¦“¦ÓŚ»ÆŃ§Ę½ŗāדĢ¬µÄŹ±¼äŹĒ10min--13min¼°µŚ20min ŗó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijĶ¬Ń§ĻėÓĆŹµŃéÖ¤Ć÷øßĆĢĖį¼ŲČÜŅŗµÄ×ĻŗģÉ«ŹĒMnO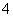 µÄŃÕÉ«£¬¶ų²»ŹĒK£«µÄŃÕÉ«”£ĖūÉč¼ĘµÄŹµŃé²½ÖčČēĻĀ£¬ÄćČĻĪŖĻĀŹöŹµŃé²½ÖčŅ»¶ØƻӊŅāŅåµÄŹĒ£Ø””””£©
µÄŃÕÉ«£¬¶ų²»ŹĒK£«µÄŃÕÉ«”£ĖūÉč¼ĘµÄŹµŃé²½ÖčČēĻĀ£¬ÄćČĻĪŖĻĀŹöŹµŃé²½ÖčŅ»¶ØƻӊŅāŅåµÄŹĒ£Ø””””£©
A.½«øßĆĢĖį¼Ų¾§Ģå¼ÓČČ·Ö½ā£¬ĖłµĆ¹ĢĢåÖŹĮæ¼õÉŁ
B.¹Ū²ģĀČ»Æ¼ŲČÜŅŗƻӊŃÕÉ«£¬±ķĆ÷ČÜŅŗÖŠK£«ĪŽÉ«
C.ŌŚĀČ»Æ¼ŲČÜŅŗÖŠ¼ÓČėŹŹĮæŠæ·ŪÕńµ“£¬¾²ÖĆĪ“¼ūĆ÷ĻŌ±ä»Æ£¬±ķŹ¾ŠæÓėK£«²»·“Ó¦
D.ŌŚøßĆĢĖį¼ŲČÜŅŗÖŠ¼ÓČėŹŹĮæŠæ·ŪÕńµ“£¬¾²ÖĆŗó¼ū×ĻŗģÉ«ĶŹČ„£¬±ķĆ÷MnO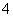 ĪŖ×ĻŗģÉ«
ĪŖ×ĻŗģÉ«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ä³ŃŠ¾æŠ”×éĪŖĢ½¾æČõĖįŠŌĢõ¼žĻĀĢś·¢Éśµē»ÆѧøÆŹ“ĄąŠĶµÄÓ°ĻģŅņĖŲ£¬½«»ģŗĻ¾łŌȵĊĀÖĘĢś·ŪŗĶĢ¼·ŪÖĆӌ׶ŠĪĘæµ×²æ£¬ČūÉĻĘæČū(ČēĶ¼1)”£“Ó½ŗĶ·µĪ¹ÜÖŠµĪČė¼øµĪ“×ĖįČÜŅŗ£¬Ķ¬Ź±²āĮæČŻĘ÷ÖŠµÄŃ¹Ēæ±ä»Æ”£
£Ø1£©ĒėĶź³ÉŅŌĻĀŹµŃéÉč¼Ę±ķ(±ķÖŠ²»ŅŖĮōæÕ øń)£ŗ
øń)£ŗ
| ±ąŗÅ | ŹµŃéÄæµÄ | Ģ¼·Ū/g | Ģś·Ū/g | “×Ėį/% |
| ¢Ł | ĪŖŅŌĻĀŹµŃé×÷²ĪÕÕ | 0.5 | 2.0 | 90.0 |
| ¢Ś | “×ĖįÅØ¶ČµÄÓ°Ļģ | 0.5 | 36.0 | |
| ¢Ū | 0.2 | 2.0 | 90.0 |
£Ø2£©±ąŗÅ¢ŁŹµŃé²āµĆČŻĘ÷ÖŠŃ¹ĒæĖꏱ¼ä±ä»ÆČēĶ¼2”£t2Ź±£¬ČŻĘ÷ÖŠŃ¹ĒæĆ÷ĻŌŠ”ÓŚĘšŹ¼Ń¹Ē棬ĘäŌŅņŹĒĢś·¢ÉśĮĖ øÆŹ“£¬ĒėŌŚĶ¼3ÖŠÓĆ¼żĶ·±ź³ö·¢ÉśøĆøÆŹ“Ź±µē×ÓĮ÷¶Æ·½Ļņ£»“ĖŹ±£¬Ģ¼·Ū±ķĆę·¢ÉśĮĖ (”°Ńõ»Æ”±»ņ”°»¹Ō”±)·“Ó¦£¬Ęäµē¼«·“Ó¦Ź½ŹĒ ”£
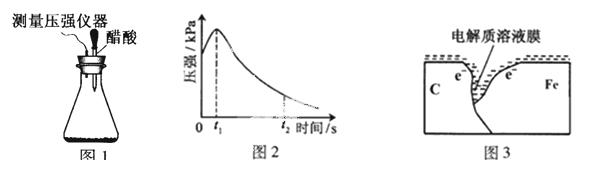
£Ø3£©øĆŠ”×é¶ŌĶ¼2ÖŠ0”«t1Ź±Ń¹Ēæ±ä“óµÄŌŅņĢį³öĮĖČēĻĀ¼ŁÉč£¬ĒėÄćĶź³É¼ŁÉ趞£ŗ
¼ŁÉčŅ»£ŗ·¢ÉśĪöĒāøÆŹ“²śÉśĮĖĘųĢ壻
¼ŁÉ趞£ŗ  £»
£»
””
£Ø4£©ĪŖŃéÖ¤¼ŁÉčŅ»£¬Ä³Ķ¬Ń§Éč¼ĘĮĖ¼ģŃéŹÕ¼ÆµÄĘųĢåÖŠŹĒ·ńŗ¬ÓŠH2µÄ·½°ø”£ĒėÄćŌŁÉč¼ĘŅ»øöŹµŃé·½°øŃéÖ¤¼ŁÉčŅ»£¬Š“³öŹµŃé²½ÖčŗĶ½įĀŪ”£
| ŹµŃé²½ÖčŗĶ½įĀŪ(²»ŅŖĒ󊓾ßĢå²Ł×÷¹ż³Ģ)£ŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²¤²ĖÓŖŃų·įø»£¬ĖŲÓŠ”°Źß²ĖÖ®Ķõ”±Ö®³Ę£¬ŹĒŅ»ÖÖøߊ§µÄ²¹Ģś¼Į”£³¤ĘŚŅŌĄ“Ćń¼äĮ÷“«”°²¤²Ė²»ÄÜÓė¶¹øÆĶ¬Ź³”±”¢”°²¤²Ėøł±Č²¤²Ė¾„ŗĶŅ¶øüÓŠÓŖŃų”±µČĖµ·Ø”£Ä³Ń§Š£»ÆѧŠĖȤŠ”×éµÄĶ¬Ń§ÄāĶعżŹµŃéĢ½¾æŅŌĻĀĪŹĢā£ŗ
¢Ł²¤²ĖŹĒ·ńŗ¬ÓŠ·įø»µÄĢś£æ
¢Ś²¤²ĖŹĒ·ńŗ¬ÓŠ²ŻĖįĄąĪļÖŹ£æ
¢Ū²¤²ĖøłÖŠĢśµÄŗ¬ĮæŹĒ·ń±Č²¤²Ė¾„ŗĶŅ¶ÖŠµÄøߣæ
ĶعżÉĻĶų²éŃÆ£¬»ńµĆŅŌĻĀ׏ĮĻ£ŗ²ŻĖįÓÖĆūŅŅ¶žĖį£¬ĘäĖįŠŌ±ČŅŅĖįÉŌĒ棬²ŻĖį¼°ĘäŃĪ¾ßÓŠ½ĻĒæµÄ»¹ŌŠŌ£¬ĘäÖŠ²ŻĖįøĘ²»ČÜÓŚĖ®”£
ĖūĆĒÉč¼ĘµÄŹµŃé²½ÖčČēĻĀ£ŗ
¢ń.
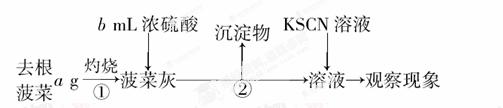
¢ņ.Č”²¤²Ėøła g£¬Ź¹ÓĆĻąĶ¬ŅĒĘ÷”¢ŹŌ¼Į£¬ÖŲø“IÖŠŹµŃ飬¹Ū²ģŹµŃéĻÖĻó”£
¢ó.½«²¤²ĖŌŚÉŁĮææŖĖ®ÖŠÖó·Š2”«3 min£¬ĄäČ“ŗóĀĖČ„²¤²Ė£¬µĆĀĖŅŗ”£ĻņĀĖŅŗÖŠ¼ÓČė×ćĮæCa(OH)2ČÜŅŗ£¬Č»ŗóŌŁ¼ÓČė×ćĮæŹŌ¼ĮX£¬¹Ū²ģĻÖĻó”£
Ēė»Ų“šŅŌĻĀĪŹĢā£ŗ
(1)²Ł×÷¢ŁÖŠŹ¹ÓƵÄŅĒĘ÷³żČż½Å¼Ü”¢¾Ę¾«µĘ”¢²£Į§°ōĶā»¹ŠčŅŖ________£¬²Ł×÷¢ŚµÄĆū³ĘŹĒ________”£
(2)æÉŅŌĖµĆ÷²¤²ĖøłÖŠFeŌŖĖŲŗ¬ĮæŅŖ±Č²¤²Ė¾„ŗĶŅ¶ÖŠ¶ąµÄĻÖĻóŹĒ________”£
(3)²¤²ĖÖŠµÄFeŹĒ£«2¼Ū»¹ŹĒ£«3¼Ū£æ________”£
(4)Ķعż²½Öč¢óæÉŅŌČ·¶Ø²¤²ĖÖŠŗ¬ÓŠ²ŻĖįĄąĪļÖŹ”£ÓÉÓŚĀĖŅŗÖŠŗ¬ÓŠCO32££¬¹ŹŠč¼ÓČėŹŌ¼ĮXÅųżCO32£µÄøÉČÅ”£ŌņXŹĒ________(Š“»ÆѧŹ½)£¬¼ÓČėŹŌ¼ĮXŗó¹Ū²ģµ½µÄĻÖĻóŹĒ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓĆNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£Źż£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®ÓĆŗ¬0.1mol FeCl3µÄČÜŅŗÓė×ćĮæ·ŠĖ®·“Ó¦ÖʵƵÄFe(OH)3½ŗĢåÖŠ½ŗĮ£ŹżĪŖ0.1NA
B£®46g NO2ŗĶN2O4µÄ»ģŗĻĘųĢåÖŠŗ¬NŌ×Ó×ÜŹżĪŖNA
C£®±ź×¼×“æöĻĀ£¬5.6L CCl4ŗ¬ÓŠµÄ·Ö×ÓŹżĪŖ0.25NA
D£®µČĪļÖŹµÄĮæµÄNH4£«ŗĶOH£ŗ¬µē×ÓŹż¾łĪŖ10NA
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com