
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温下是一种无色气体 |
| B.在一定条件下可分解成SO2 |
| C.易溶于水,但不溶于浓H2SO4 |
| D.能与SO2发生氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:判断题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.二氧化硫通入足量KOH溶液中SO2+2OH- 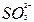 +H2O +H2O |
B.往澄清石灰水中通入足量二氧化硫SO2+Ca2++2OH- CaSO3↓+H2O CaSO3↓+H2O |
C.往二氧化硫的水溶液中滴加少量NaOH溶液H2SO3+OH-  +H2O +H2O |
D.亚硫酸中滴加双氧水生成硫酸H2SO3+2H++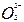  2H++ 2H++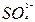 +2H2O +2H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 不同质量铵盐/g | 25.00 | 50.00 | 75.00 | 100.00 |
| 浓硫酸增加的质量/g | 相同 | 相同 | 1.70 | 0 |
| A.12.15% | B.21.50% | C.14.56% | D.无法确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com