
| 晶体类型 | 原子晶体 | 离子晶体 | 分子晶体 |
| A. | 氮化硅 | 磷酸 | 单质硫 |
| B. | 单晶硅 | 碳酸氢铵 | 水银 |
| C. | 金刚石 | 烧碱 | 冰 |
| D. | 铁 | 尿素 | 冰醋酸 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据构成晶体的微粒确定晶体类型,原子晶体的构成微粒是原子,分子晶体的构成微粒是分子,离子晶体的构成微粒是阴阳离子.
解答 解:A.磷酸的构成微粒是分子,所以磷酸属于分子晶体,故A错误;
B.单晶硅的构成微粒是原子,所以属于原子晶体,碳酸氢铵的构成微粒是阴阳离子,所以属于离子晶体,水银的构成微粒是金属阳离子和自由电子,属于金属晶体,故B错误;
C.金刚石的构成微粒是原子,所以属于原子晶体,烧碱的构成微粒是阴阳离子,所以属于离子晶体,冰的构成微粒是分子,所以属于分子晶体,故C正确;
D.铁的构成微粒是金属阳离子和自由电子,所以属于金属晶体,尿素的构成微粒是分子,属于分子晶体,冰醋酸的构成微粒是分子,属于分子晶体,故D错误;
故选C.
点评 本题考查了晶体类型的判断,明确晶体的构成微粒是解本题关键,注意尿素属于分子晶体,为易错点.


科目:高中化学 来源: 题型:解答题

| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
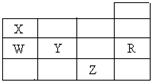
| A. | 常压下五种元素的单质中,Z单质的沸点最高 | |
| B. | Y、Z的阴离子电子层结构都与R原子的相同 | |
| C. | W的氢化物的稳定性比X的氢化物的稳定性高 | |
| D. | Y元素的非金属性比W元素的非金属性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
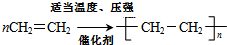 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放热183 kJ | B. | 放热91.5 kJ | C. | 吸热183 kJ | D. | 吸热91.5 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯分子中3个碳原子都是sp3杂化 | |
| B. | 丙烯分子存在非极性键 | |
| C. | 丙烯分子有6个σ键,1个π键 | |
| D. | 丙烯分子中3个碳原子在同一直线上 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 硼(B)及其化合物在化学中有重要的地位.请回答下列问题:
硼(B)及其化合物在化学中有重要的地位.请回答下列问题: [B(OH)4]-+H+.
[B(OH)4]-+H+.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
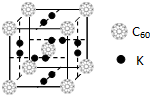 碳元素是构成物质种类最多的一种元素,许多物质与我们的生活息息相关.
碳元素是构成物质种类最多的一种元素,许多物质与我们的生活息息相关. ,该物质的K原子和C60分子的个数比为3:1.
,该物质的K原子和C60分子的个数比为3:1.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 燃烧反应都是放热反应 | |
| B. | 对于可逆反应:aA(g)+bB(g)?bC(g)+dD(g),如果正反应放热,逆反应一定吸热 | |
| C. | 氢气燃烧生成水是一个放热的化学反应,说明1 mol H2的能量高于1 mol H2O的能量 | |
| D. | 只有放热的氧化还原反应才可以设计为原电池 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com